| класс веществ
| реактив
| уравнение реакции
| признак реакции
|
| алкены
| Br2 (водный раствор)
KMnO4 (водный раствор)
| СnH2n + Br2 → СnH2nBr2
При мягком окислении алкенов водным раствором KMnO4 (реакция Вагнера) образуются двухатомные спирты:
3СnH2n + 2KMnO4 + 4Н2О → 2MnO2 + 2KOH +
+ 3CnH2n(ОН)2
| алкены обесцвечивают бромную воду.
алкены обесцвечивают раствор перманганата калия
|
|
алкины
|
Br2 (водный раствор)
Ag[(NH3)2]OH (аммиачный раствор оксида серебра (I))
Cu[(NH3)2]Cl (аммиачный раствор)
KMnO4 (раствор)
|
СnH2n–2 + 2Br2 → СnH2n–2Br4
СН3–С≡СН + Ag[(NH3)2]OH → СН3–С≡С–Ag↓ +
+ 2NH3 + H2O
СН3–С≡СН + Cu[(NH3)2]Cl → СН3–С≡С–Cu↓ + NH3
+ NH4Cl
Алкины легко окисляются различными окислителями, в частности перманганатом калия. При этом раствор обесцвечивается, что служит указанием на наличие тройной связи. При окислении обычно происходит расщепление тройной связи, и образуются карбоновые кислоты и/или углекислый газ в кислой среде. В нейтральной и щелочной средах – соли карбоновых кислот.
5СН3–С≡С–СН3 + 6KMnO4 + 9H2SO4 →10CH3COOH +
+ 6MnSO4 + 3K2SO4 + 14H2O
5СН≡С–СН3 + 8KMnO4 + 12H2SO4 → 5CH3COOH +
+ 5СО2 + 8MnSO4 + 4K2SO4 + 12Н2О
3СН≡СН + 8KMnO4 → 8MnO2 + 2KOH +
+ 3KOOC–COOK + 2Н2О
|
алкины обесцвечивают бромную воду.
осадок
красный осадок
обесцвечивают раствор перманганата калия
|
| алифатические спирты:
одноатомные
многоатомные
|
CuO
Cu(OH)2
|
СnH2n +1 СН2OH + CuO → СnH2n +1CHO + H2O + Cu
комплексообразование
|
запах альдегида, черный цвет проволоки меняется на красный
Качественной реакцией на многоатомные спирты, содержащие группы −ОН при соседних атомах углерода, является ярко синее окрашивание при действии свежеосажденного гидроксида меди (II)
|
|
фенол
|
Br2 (водный раствор)
FeCl3
|
ОН Br
  │ │ │ │
 
 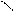 + 3Br2 → ↓ + 3HBr
Br Br + 3Br2 → ↓ + 3HBr
Br Br
|
При действии на фенол бромной воды образуется осадок белого цвета 2,4,6-трибромфенол
Еще одной качественной реакцией на фенолы является их взаимодействие с раствором хлорида железа (III), в результате которого образуется комплексное соединение фиолетового цвета.
|
| альдегиды
| Сu(OH)2 (свежеприготовленный в щелочном растворе)
[Ag(NH3)2]OH (Ag2O в аммиачном растворе)
| RCHO + 2Cu(OH)2 → RCOOH + Cu2O↓ + 2H2O
RCHO + 2[Ag(NH3)2]OH → RCOONH4 + 2Ag↓ + 4NH3↑ + H2O
| При окислении альдегидов гидроксидом меди(II) последний превращается в желтый гидроксид меди (I), который при нагревании разлагается с образованием оксида меди (I) красного цвета
реакция «серебряного зеркала»
|
| предельные карбоновые кислоты (растворы)
непредельные карбоновые кислоты
| индикатор
NaHCO3 (пищевая сода)
Br2 (водный раствор)
KMnO4 (раствор)
|
RCOOH + NaHCO3 → RCOONa + CO2↑ + H2O
СО2 + Са(ОН)2 = СаСО3↓ + Н2О
R−CH=CH−RCOOH + Br2 → R−CHBr−CHBr−RCOOH
| изменение цвета индикатора (лакмус на красный, метилоранжевый на красный, фенолфталеин остается бесцветным)
выделение углекислого газа, вызывающего помутнение известковой воды
обесцвечивают бромную воду
обесцвечивают раствор перманганата калия
|
| углеводы:
глюкоза
крахмал
|
свежеосажденный Cu(OH)2 в щелочном растворе
[Ag(NH3)2]OH (Ag2O в аммиачном растворе)
I2
|
Комплексообразование
RCHO + Ag2O → RCOOH + 2Ag↓
|
синий раствор глюконата меди
реакция «серебряного зеркала»
синее (фиолетовое) окрашивание
|
| низшие алифатические амины
| индикатор
|
| изменение цвета индикатора в щелочной среде
лакмус меняет цвет на синий;
фенолфталеин на малиновый
метилоранжевый на желтый
|
| ароматические амины
анилин
|
Br2 (водный раствор)
|
C6H5NH2 + 3Br2 → C6H5Br3NH2↓ + 3HBr
|
белый осадок
|
| белки
| Азотная концентрированная кислота (ксантопротеиновая реакция)
Свежеприготовленный гидроксид меди (II) (биуретовая реакция)
|
| Желтое окрашивание
Синефиолетовое окрашивание
|

 │ │
│ │



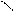 + 3Br2 → ↓ + 3HBr
Br Br
+ 3Br2 → ↓ + 3HBr
Br Br