РАСТВОРИМОСТЬ МАЛОРАСТВОРИМЫХ СОЛЕЙ
Поместим в воду хлорид серебра в количестве, большем, чем это необходимо для получения насыщенного раствора. Тогда между осадком и ионами в насыщенном растворе установится гетерогенное равновесие.
AgCl(TB) = Ag+(водн) + Сl-(водн)
В выражение К для гетерогенного равновесия твердые вещества не включаются. Тогда
К =CAg+ • СС1- = ПРAgCl
Константа равновесия такого типа называется произведением растворимости ПР или константой растворимости KS. Как любая константа равновесия величина ПР зависит от температуры и не зависит от концентрации. Итак,
© произведение концентраций ионов малорастворимого вещества в его насыщенном растворе при постоянной температуре есть величина постоянная, называемая произведением растворимости.
Если вместо хлорида серебра взять другую малорастворимую соль — иодид свинца РbI2, установится равновесие:
РbI2 = Pb2+ + 2I-
Значит, ПРPbl2 = Cpb2+• C2I -.
Произведения растворимости малорастворимых веществ приводятся в таблицах. Надоиметь в виду, что в разных источниках значения ПР могут значительно различаться.
Величину ПР можно рассчитать, если экспериментально определить растворимость вещества в воде.(Способы решения задач могут быть различны).
Пример 1.
Насыщенный раствор CaF2 при 25°С содержит 0,00168 г соли в 100 см3 раствора. Рассчитать ПРСaF2.
Решение. Найдем молярную концентрацию насыщенного раствора фторида кальция. Молярная масса М (CaF2) = 78 г/моль.
CM = (0,00168 • 1000)/(78 • 100) = 2,15 • 10-4 моль/дм3
Фторид кальция диссоциирует по схеме:
CaF2 = Са+ + 2F-
1 моль соли дает 1 моль ионов Са2+ и 2 моль фторид-ионов. Значит,CСа2+ = 2,15 • 10-4 моль/дм3, а CF- = 4,30 • 10-4 моль/дм3. Тогда
ПРСаF2 = 2,15 • 10-4 • (4,30 • 10-4)2 = 3,97 • 10-11.
Пример 2.
После выпаривания воды из 15,0 г раствора ортофосфата серебра Ag3PO4 получено 0,0001 г безводной соли. Определите ПP(Ag3PO4).
Решение. На первых порах лучше начинать с уравнения диссоциации соли:
Ag3PO4 = 3Ag+ + PO3-4
Теперь можно записать выражение для произведения растворимости:
ПР(Ag3PO4) = [Ag+]3[PO3-4]
Для вычисления ПР нужны молярные концентрации ионов. Найдем молярность исходного раствора. Вам понятно, что для малорастворимых веществ плотность их растворов спокойно может быть принята равной 1 г/ мл? Молярная масса Ag3PO4 равна 419 г / моль и молярность раствора C (Ag3PO4)= 0,0001/(0,015• 419) = 1,6• 10-6М. Отсюда [Ag +]= 3 1,6 •10-5 = 4,8• 10-8 М, [РО3-4] = 1,6 • 10-5 М. Теперь находим произведение растворимости:
ПР(Ag3PO4) = [Ag+]3[PO3-4] = (4,8 • 10-6)3 • (1,6• 10 -5) = 1,8 • 10 -18
Ответ. ПP(Ag3PO4)=l,8 10-18.
Пример 3.
Растворимость Ag3PO4 (Мч=418,58) в воде при 20 °С равна 0,0065 г/л. Рассчитайте значение произведения растворимости.
Решение. Растворимость Ag3PO4 равна
 моль/л
моль/л
При диссоциации 1 моль Ag3PO4 образуется 3 моль ионов Ag+ и 1 моль ионов 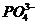 , поэтому концентрация иона
, поэтому концентрация иона 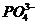 равна растворимости Ag3PO4, а концентрация иона Ag+ в 3 раза больше, т, е.
равна растворимости Ag3PO4, а концентрация иона Ag+ в 3 раза больше, т, е.
C 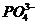 = 1,6 • 10-5 моль/л; CAg+=3 • 1,6 • 10-5 моль/л.
= 1,6 • 10-5 моль/л; CAg+=3 • 1,6 • 10-5 моль/л.
Произведение растворимости Ag3PO4 равно
ПР== (4,8• 10-5)3 1,6• 10-5= 110,6• 10-15• 1,6• 10-5= 1,77• 10-18
Исходя из величины произведения растворимости, можно рассчитать растворимость любого вещества.(Способы решения задач могут быть различны).
Пример 4.
Рассчитать растворимость BaSO4 и концентрации ионов [Ва2+] и [SO42-] в насыщенного растворе сульфата бария.
Решение.
Значение K S(BaSO4 ) = 1,1 • 10 -10. Растворимость BaSO4 обозначим за S моль/л. Очевидно, что для электролита распадающегося на два иона (бинарного электролита):
 [Ва2+ ] = [SO2- 4 ] = S, S= √ Ks(BaSO4)=1 • 10-5
[Ва2+ ] = [SO2- 4 ] = S, S= √ Ks(BaSO4)=1 • 10-5
Ответ: [Ва2+] = [SO42-] = S =1 ּ 10 -5 моль/л.
Пример 5.
Вычислить массу ионов малорастворимого электролита в его насыщенном растворе.
KS(BaF2) при 180 С равно 1,7 • 10 -6 . Рассчитайте массу ионов Ва2 + и F- в 700мл насыщенного раствора BaF2 при этой температуре.
Решение.
BaF2 диссоциирует по уравнению: BaF2 = Ba 2+ + 2F-
Произведение растворимости соли Ks(BaF2)= [Ba2+ ]•[F-]2.
При диссоциации BaF2 ионов F-получается в 2 раза больше, чем ионов Ва2 +.
Следовательно, СF- =2CВа2+. Выразим концентрацию ионов F- через концентрацию ионов Ва 2+, тогда Ks(BaF2) = СВа2+ • (2CВа2+)2= 4(СВа2+)3 = 1,7• 10-6 .
______
Концентрация ионов Ва2 + равна: СВа2+ = 3√1,7∙10-6 /4 = 0,75 • 10-2 моль/л.
Концентрация ионов F- равна: СF-=2• 0,75•10-2= 1,50 • 10-2 моль/л
Масса ионов Ва2 + : m(Ва2 +) = С (Ва2 +)•M(Ва2 +)•Vр-ра = 0,75 • 10-2 •137•0,7 = 71,925•10-2г = 719,25мг.
Масса ионов F-: m (F-) = C (F-) •M(F-)•Vр-ра = 1,50 • 10-2 •19•0,7 = 19,95•10-2г = 199,5мг.
Пример 6.
Произведение растворимости хлорида свинца при 25 °С равно 1,6•10-5. Определите концентрацию насыщенного раствора РЬС12 при этой температуре.
Решение.
Запишем уравнение диссоциации и выражение произведения растворимости хлорида свинца:
РЬС12 = РЬ2+ + 2СГ ПР (РьCl) = [РЬ2+ ]• [Сl-]2
Обозначим искомую молярность насыщенного раствора РЬС12 через s. Тогда [РЬ2+] = sи [Сl-] = 2s. Далее: ПР(РЬС1т)= [РЬ2+]•[С1-]2 = s ( 2s)2. Получаем уравнение: 4s3 = 1,6 • 10-5. Находим s= 1,6•10-2.
Ответ. С(РЬС1т)=1,6 •10-2М.
Пример 7.
Произведение растворимости хлорида свинца при 25 °С равно 1,6 • 10-5. Определите, как изменится растворимость РЬС12 в 1 М растворе НС1 по сравнению с чистой водой. Диссоциацию НС1 считать полной.
Решение.
Как найти растворимость РЬС12 в чистой воде, показано в предыдущем примере. В растворе НС1 нарушается стехиометрия концентраций ионов РЬ2+ и Сl- , соляной кислоты. Обозначим, как и раньше, искомую молярность РЬС12 через s. Тогда концентрации ионов, перешедших в раствор в результате растворения РЬС12, будут равны С(Рь-) = sи С(СГ) = 2s. Учитывая концентрацию хлорид-ионов в растворе НС1, получаем уравнение:
ПР(РЬС1т)= [РЬ2+]•[С1-]2 1,6 •10-5 = s(1 + 2s)2
Можно решить это кубическое уравнение, но, как следует из решения примера 2, в чистой воде растворимость РЬС12 всего 1,6 •10-2, а в растворе НС1 она еще меньше, потому концентрацией хлорид-ионов, перешедших в раствор в результате растворения РЬС12 (< 3,2•10-2), можно спокойно пренебречь по сравнению с их концентрацией в растворе НС1 (1,0). Тогда 1,6 •10-5 = s(1 + 0) 2. Откуда s= 1,6•10 -5. Таким образом, растворимость РЬС12 в 1 М растворе НС1 по сравнению с чистой водой уменьшается в 1,6•10-2/1,6•10-5= 103раз.
Решите эту задачу для случая С(HCl) = 0,1 М и убедитесь, что и при такой концентрации НС1 величиной 2s можно спокойно пренебречь по сравнению с 0,1.
Ответ. В1М растворе НС1 растворимость РЬС12 уменьшается в тысячу раз.
Пример 8.
Чему равна растворимость в воде иодида свинца в моль/дм3 и г/дм3 при 25° С?
Решение.
Находим по таблице величину ПРРbI2 = 8,1 • 10-9. Обозначим растворимость РbI2 в моль/дм3 через s. Тогда
РbI2 = РЬ2+ + 2I-
s s 2s
ПРрbI2 = CРЬ2+ • C 2I- = s(2s) 2 = 4s3 = 8,1 • 10-9
s =3  = 1,27 • 10-3 моль/дм3
= 1,27 • 10-3 моль/дм3
Умножив полученную величину на молярную массу соли, получим растворимость в г/дм3.
461 • 1,27 • 10-3 = 0,585 г/дм3
Рассмотрим другой случай: зная, что степень диссоциации слабого электролита уменьшается при введении в раствор сильного электролита с одноименным ионом можно предположить, что и растворимость малорастворимых веществ также уменьшается в присутствии избытка одноименных ионов. В примере 4 мы нашли, что растворимость иодида свинца в воде равна 1,27 • 10-3 моль/дм3. Рассчитаем величину растворимости этой же соли в присутствии 0,1 моль/дм3 иодида калия,.
ПРРbI2 = CРЬ 2+ • CI- 2 = s• (0,1)2 = 8,1 • 10-9 отсюда выражая s получим:
s = 8,1 • 10-7 моль/дм3
© Таким образом, в присутствии избытка одноименных ионов растворимость малорастворимого вещества понижается и осаждение будет более полным.
При проведении реакций, в результате которых получаются малорастворимые вещества, важно уметь предсказывать, образуется ли осадок при данных концентрациях взятых веществ. Для такого предсказания пользуются следующим правилом:
© Малорастворимое вещество выпадает в осадок, если произведение реальных концентраций ионов в растворе больше величины произведения растворимости при данной температуре.
Пример 9.
Смешаны 20 см3 раствора нитрата серебра с концентрацией 2 • 10-3 моль/дм3 и 30 см3 раствора хромата калия с концентрацией 1 • 10-4 моль/дм3. Выпадет ли осадок?
Решение.
Уравнение реакции: 2AgNO3 + K2CrO4 = Ag2Cr04 + 2KNO3
Рассчитаем концентрации ионов Ag+ и CrO2-4 после сливания растворов, учитывая, что объем полученного раствора 50 см3.
C Ag+ = (2 • 10-3 • 20)/50 = 0,8 • 10-3 моль/дм3
C CrO42- = (1 • 10-4 • 30)/50 = 0,6 • 10-4 моль/дм3
C2Ag+ • C CrO42- = (0,8 • 10-3)2 • 0,6 • lO-4 = 0,384 • 10-10
Величина ПРAg2 CrO4= 1,1 • 10-12
Итак, произведение реальных концентраций больше величины ПР, следовательно, хромат серебра будет выпадать в осадок.
Пример 10.
Определить выпадет ли осадок при смешивании равных объёмов 0,01 М растворов хлорида бария и сульфата натрия.
Решение.
Напишем уравнение реакции: BaCL2 + Na2SO4 = BaSO4 + 2NaCL
После смешения равных объемов хлорида бария и сульфата натрия их концентрации уменьшились в 2 раза и составили: С(ВаС12)=0,005моль/л:
C(Na2SO4)=0,005моль/л. Соответственно, концентрации интересующих нас
ионов Ва2+ и SO42- так же оказались равными 5 • 10-3 моль/л.
Найдем произведение концентраций этих ионов: [Ba2+][SO42-] = (5 • 10-3)2 = 2,5 •10-5.
Найденное произведение концентраций ионов превышает значение Ks(BaSO4) = 1,1 • 10-10 следовательно, осадок образуется.
Пример 11.
Слиты вместе 0,5 л 0,01 М раствора СаС12 и 0,5 л 0,02 М раствора NaF. Выпадет ли при этом осадок CaF2?
Решение.
Выпадение осадка будет происходить в том случае, если значение произведения концентраций ионов Са2+ и F-, находящихся в растворе, будет больше, чем ПP(CaF2). Найдем это значение. Прежде всего обратите внимание на то, что при сливании растворов все концентрации изменились. Так как объемы сливаемых растворов равны, концентрации солей уменьшились в два раза.
В общем растворе концентрация С (CaCl2)= 5 • 10-3 М, С (NaF) = 1•10-2 М.
Концентрации ионов Са2+ и F- в общем растворе до начала осаждения равны концентрациям солей: С(Са2+) = 5•10-3 моль/л, С(F -) = 1•10-2 моль/л.
Найдем произведение концентраций ионов Са2+ и F- в растворе, полученном после сливания исходных растворов:
Пс(СaCl2)= С(Сa2+) • С 2(F - )= 5•10 -3•(1•10-2)2 = 5•10-7 .
В таблице находим ПР(CaCl2)= [Ca2+ ]•[F-]2 = 4•10-11.
Произведение концентраций ионов в растворе на 4 порядка больше, чем ПР(СаF2), и осадок фторида кальция будет из него выпадать.
Пример 12.
Определение условий выпадения осадка.
Произведение растворимости MgS (KS)при 25 °С равно 2,0• 10 -15 . Образуется ли oсадок MgS при смешении равных объемов 0,002моль/лMg(NO3)2 и 0,0003 моль/л Na2S?
Решение.
При смешении равных объемов растворов объем смеси стал в 2 раза больше каждого из взятых растворов, а концентрация каждого из растворенных веществ уменьшилась вдвое,
т. е. C(Mg(NO3)2) = 0,001моль/л.; C(Na2S) =0,00015моль/л.
Концентрации ионов Mg2+ и S2- после смешения соответственно равны:
С(Mg2+) = 1• 10 -3 моль/л; C(S2-)= 1,5• 10-4 моль/л.
Произведение концентраций ионов Mg2+ и S2-:
Пс = С(Mg2+) C(S2-)= 10-з •1,5•10-4= 1,5•10-7
Пс = 1,5•10-7 >больше KS . Следовательно, осадок MgS образуется.
Пример 13.
Определение условий одновременного выпадения осадков солей из раствора.
При каком соотношении концентраций ионов Ва2+ и РЬ2+ их карбонаты при введении ионов  будут выпадать одновременно?
будут выпадать одновременно?
По таблицам значения констант ПР ВаСО3 =  ,
, 
Решение.
Концентрацию вводимых карбонат-ионов обозначим через C  тогда
тогда
 ;
;  ;
; 
Итак, карбонаты бария и свинца будут выпадать одновременно из раствора, если сВа2+>срb2+ в
46700 раз. Если отношение CBa 2+/C Pb 2+>46700, то первым из раствора будет выпадать ВаСО3 до
тех пор, пока отношение сВа2+ /сPb2+ не будет равным 46 700. И только после этого начнется одновременное выпадение осадков. Если же отношение концентрации ионов бария и свинца меньше 46 700, то первым начнет осаждаться карбонат свинца. Осаждение карбоната свинца будет протекать до тех пор, пока отношение CBa 2+/C Pb 2+не достигнет значения, при котором ВаСО3 и РЬСО3 будут осаждаться одновременно.
Пример 14.
Раствор содержит нитраты кадмия и железа(П) в равных концентрациях. Гидроксид какого элемента будет первым выпадать в осадок при добавлении щелочи? Каким должно быть соотношение концентраций нитратов, чтобы при добавлении щелочи оба гидроксида начали выпадать в осадок одновременно?
Решение.
На первый вопрос ответить легко. Вы уже поняли, что чем меньше ПР, тем меньше концентрация электролита (не забудьте, что можно сравнивать только однотипные электролиты: двухионные с двухионными, трехионные с трехионными и т.д.).В данном случае оба гидроксида являются трехионными, значит, первым будет выпадать осадок того гидроксида, ПР которого меньше.
Смотрим в таблице: ПР(сd(он)2) = 2 • 10 -14, ПP(Fe(OH)2)= 1 • 10-15. ПР гидроксида железа на порядок меньше, чем гидроксида кадмия, следовательно, при равных концентрациях нитратов, т. е. при равных концентрациях ионов металлов, Fe(OH)2 будет выпадать первым.
Чтобы оба гидроксида начали выпадать в осадок одновременно, надо, чтобы концентрация вводимой щелочи удовлетворяла бы одновременно обоим значениям ПР. Равновесная концентрация ионов ОН -
 над осадком Cd(OH)2: [OН-]= √ПP(Cd(OH)2)/[Cd2+]
над осадком Cd(OH)2: [OН-]= √ПP(Cd(OH)2)/[Cd2+]
 Над осадком Fe(OH)2: [ОН-] = √ПP(Fe(OH)2)/[Fe2+]
Над осадком Fe(OH)2: [ОН-] = √ПP(Fe(OH)2)/[Fe2+]
Эти концентрации равны, если
ПP(Сd(OH)2)/[Cd2+] == ПP(Fe(OH)2)/[Fe2+].
или [Fe2+]/[Cd2+] = ПР(Fе(ОН)2)/ПР(Сd(ОН)2).
Осадки гидроксидов будут выпадать одновременно, если отношение концентраций ионов металлов равно отношению их ПР: [Fe2+]/[Cd2+] = 1• 10-15/2 • 10-14 = 0,05. Осадки гидроксидов будут выпадать одновременно, если концентрация ионов железа в 20 раз меньше, чем ионов кадмия.
Ответ. Fe(OH)2; cоотношение концентраций нитратов железа к кадмию должно быть равным 0,05.
РЕЗЮМЕ
Произведение растворимости - весьма информативная величина, очень удобная при обсуждении свойств растворов сильных электролитов исходя из произведения растворимости можно определить:
-концентрации ионов, образующих сильный электролит;
-концентрацию его насыщенного раствора;
-изменения этих величин при изменении состава раствора;
-возможность выпадения или растворения осадка.
Однако, для активного использования ее необходимо:
- уверенно пользоваться всеми способами выражения концентраций;
-хорошо понимать, как соотносится аналитическая концентрация соли с концентрациями ее ионов;
-легко ориентироваться в направлениях смещения равновесий;
-помнить и понимать свойства константы равновесия.
Если у Вас нет полной уверенности в понимании этих проблем, вернитесь еще раз, внимательно посмотрите примеры решений задач и решите одну-две задачи.
- Учтите, что без ясного понимания проблем химического равновесия Вам очень трудно разбираться в свойствах растворов электролитов, поскольку все растворы представляют собой сложные равновесные системы.
-
ВОПРОСЫ
1.В чем различие сильных и слабых электролитов?
2.Какие вещества относятся к категории сильных электролитов?
3.Напишите в общем виде равновесие, константа равновесия которого называется «произведение растворимости» (ПР).
4.Можно ли утверждать, что ПР есть характеристика малорастворимых солей? Можно ли использовать ПР при рассмотрении свойств кислот и оснований?
5.В каких случаях произведение растворимости может быть выражено
через концентрацию ионов, а в каких необходимо пользоваться их
активностями?
6.Напишите выражения для произведений растворимости следующих
веществ: AgCl; BaSO4, Ca(OH)2, Ag2,S, Fe4[Fe(CN)6]3.
Выразите ПР каждого вещества через молярность его насыщенного раствора.
7.Выразите ПР ортофосфата кальция через: а) молярность его насыщенного раствора, б) нормальность раствора, в) массовую долю растворенной
соли, г) растворимость соли s в г/100 г воды. Подумайте, как Вы будете
переходить от объема раствора к его массе.
8.Произведение растворимости одной соли 1,8 •10-10, другой - 1,4•10-12.
Можно ли по этим данным утверждать, что растворимость первой соли больше, чем второй?
9.Изменится ли растворимость AgCl, если к его насыщенному раствору
с донной фазой добавить: а) хлорид натрия, б) нитрат натрия, в) нитрат серебра, г) соляную кислоту?
Задания для самостоятельной работы
1.Растворимость иодида серебра при 25 °С равна 1 • 10-s моль/л. Вычислить произведение растворимости этой соли.
Ответ: KS(AgI ) =1• 10-l0.
2.Растворимость бромида свинца при 25 °С равна 1,3 • 10-2 моль/л. Вычислить произведение растворимости этой соли.
3.Для растворения 1,16 г РЫ2 потребовалось 2 л воды при 25 °С. Найти произведение растворимости этой соли.
Ответ: KS(PbI2) = 7.8 • 10-s.
4.Найти массу ионов серебра в 1 л насыщенного раствора AgCl.
Ответ: m(Ag+) = 1,44• 10-3 г.
5.Рассчитать растворимость и концентрации ионов в насыщенных растворах: a) AgCl; б)CdS;в)Ag2SO4; г) PbI2; д)Zn(OH)2
Ответ:
а) S(AgCI) = [Ag+] = [CI-]= 1,34 • 10-5 моль/л;
б) S(CdS) = [Cd2+] = [S2-] = 8,8• 10-14моль/л;
в) S(Ag2SO4) = 2,68 • 10-2 моль/л, [SO42-] = 2,67 • 10-2 моль/л
[Ag+]=5,34• 10-2 моль/л;
г) S(PbI2) = 1,65 • 10-5 моль/л, [РЬ2+] = 1,65 • 10-5 моль/л,
[I-]= 2,5 • 10-3 моль/л;
д) S(Zn(OH)2 = 3,9 • 10-6 моль/л, [Zn2+] = 3,19 • 10- 9 моль/л,
[ОН-] = 6,38 • 10-9 моль/л.
6.В каком объеме насыщенного раствора РЫ2 содержится I мг растворенной соли?
Ответ: 131,4мл.
7.Образуется ли осадок хлорида серебра, если 0,01 М раствора AgNO3
добавить равный объем 0,1 н. раствора НСl?
Ответ: образуется.
8.Смешали равные объемы 0,01 М растворов CuSO4 и ВаС12. Образуется ли осадок?
Ответ: образуется.
9.Смешали 2 л 0,1 н. раствора Pb(NO3)2 и 1 л 0,02 н. раствора ВаС1,. Образуется ли осадок РЬС12?
Ответ: образуется.
10.Смешали 2 объема 0,2 М раствора AgNO3 и 3 объема 0,1 М раствора
NaCI. Образуется ли осадок AgCl?
Ответ: образуется.
11.Вычислить приближенную растворимость следующих малорастворимых электролитов в растворах электролитов, содержащих одноименный ион:
a) AgI в 0,1 М растворе Nal; б) CaF2 в 0,001 М растворе СаС12;
в)BaSO4 в 0,005 М растворе Na2SO4;
Ответ: а) 1,5 • 10-15 моль/л; б) 9,2 • 10-5 моль/л; в) 2,2 • 10-8 моль/л.
12. Как изменится растворимость хлорида свинца и концентрация иона РЬ2*, если к 1 л насыщенного раствора PbCl, прибавить 0,1 моль NaCl?
Ответ: растворимость и концентрация ионов РЬ2+ уменьшится в 1584 раза.
13. К 2 л насыщенного раствора Ag2CrO4 прибавили 0,1 моль К2СгО4. Как изменится растворимость соли и концентрация иона серебра в растворе.
Ответ: растворимость соли и концентрации иона серебра уменьшилась в 26 раз.
14. Концентрация иодида серебра в его насыщенном растворе при 25 °С равна 1•10-8моль•л-1. Вычислите ПР (AgI) при этой температуре.
15. Вычислите ПР(СаСО3) при 20 °С, если при этой температуре в 100 мл раствора содержится 6,5 • 10-4 г соли.
16. Каково произведение растворимости оксалата бария ВаС2О4 при 291 К, если в 1 мл его раствора, насыщенного при этой температуре, содержится 2,4 • 1017 ионов Ва2+?
17. Чему равно ПР (РЫ2) при 298 К, если в литре насыщенного раствора иодида свинца при этой температуре содержится 0,3175 г иодид-ионов?