Органическая химия.
3.1.Тема: «Теория строения органических соединений. Классификация и номенклатура»
3.1.1. Основные положения теории строения органических соединений и классификация органических соединений.
1. Природные и синтетические органические вещества. Немного из истории органической химии. Общие свойства органических веществ (состав, тип химической связи, кристаллическое строение, растворимость, отношение к нагреванию в присутствии кислорода и без него).
2. Теория строения органических соединений А.М. Бутлерова. Развитие теории и ее значение.
3. Классификация органических веществ.
Свое название органические вещества получили потому, что первые из изученных веществ этой группы входили в состав живых организмов. Большинство известных сейчас органических веществ не встречаются в живых организмах, они получены (синтезированы) в лаборатории. Поэтому различают природные (натуральные) органические вещества (хотя большинство из них может быть сейчас получено в лаборатории), а органические вещества, не существующие в природе – синтетические органические веществами. Т.е. название «органические вещества» историческое и особого смысла не имеет. Все органические соединения являются соединениями углерода. К органическим веществам относятся соединения углерода, кроме изучаемых в курсе неорганической химии простых веществ, образованных Карбоном, его оксидов, угольной кислоты и ее солей. Другими словами, органическая химия – это химия соединений углерода.
Краткая история развития органической химии:
Берцелиус, 1827, первый учебник органической химии. Виталисты. Учение о «жизненной силе».
Первые органические синтезы. Велер, 1824, синтез щавелевой кислоты и мочевины. Кольбе,1845, уксусная кислота. Бертло,1845, жир. Бутлеров,1861, сахаристое вещество.
Но как наука органическая химия началась с создания теории строения органических соединений. Существенный вклад в нее внесли немецкий ученый Ф.А.Кекуле и шотландец А.С.Купер. Но решающий вклад несомненно принадлежит русскому химику А.М.Бутлерову.
Среди всех элементов углерод выделяется своей способностью образовывать устойчивые соединения, в которых его атомы связаны друг с другом в длинные цепи различной конфигурации (линейные, разветвленные, замкнутые). Причина этой способности: примерно одинаковая энергия связи С-С и С-О (для других элементов энергия второй – намного больше). Кроме того, атом углерода может находиться в одном из трех видов гибридизации, образуя соответственно одинарные, двойные или тройные связи, причем не только между собой, но и с атомами кислорода или азота. Правда, гораздо чаще (практически всегда) атомы углерода соединены с атомами водорода. Если в состав органического соединения входит только углерод и водород, то соединения называются углеводородами. Все остальные соединения можно рассматривать как производные углеводородов, в которых некоторые атомы водорода замещены на другие атомы или группы атомов. Поэтому более точное определение: Органические соединения – это углеводороды и их производные.
Органических соединений очень много - более 10 млн. (неорганических около 500 тыс.). Состав, строение и свойства всех органических веществ имеют много общего.
Органические вещества имеют ограниченный качественный состав. Обязательно С и Н, часто О или N, реже галогены, фосфор, сера. Другие элементы входят в состав очень редко. А вот число атомов в молекуле может достигать млн, и молекулярная масса может быть очень большая.
Строение органических соединений. Т.к. состав – неметаллы. => Химическая связь: ковалентная. Неполярная и полярная. Ионная очень редко. => Кристаллическая решетка чаще всего молекулярная.
Общие физические свойства: невысокая температура кипения и плавления. Среди органических веществ есть газы, жидкости и легкоплавкие твердые вещества. Часто летучи, могут иметь запах. Обычно бесцветные. Большинство органических веществ нерастворимо в воде.
Общие химические свойства:
1) при нагревании без доступа воздуха все органические вещества «обугливаются», т.е. при этом образуется уголь (точнее сажа) и некоторые другие неорганические вещества. Происходит разрыв ковалентных связей, сначала полярных, потом и неполярных.
2) При нагревании в присутствии кислорода все органические вещества легко окисляются, и при этом конечными продуктами окисления являются углекислый газ и вода.
Особенности протекания органических реакций. В органических реакциях участвуют молекулы, в процессе реакции должны разорваться одни ковалентные связи и образуются другие. Поэтому химические реакции с участием органических соединений идут обычно очень медленно, для их проведения необходимо применять повышенную температуру, давление и катализаторы.В неорганических реакциях обычно участвуют ионы, реакции протекают очень быстро, иногда мгновенно, при нормальной температуре. Органические реакции редко приводят к высокому выходу продукции (обычно менее 50%). Они часто являются обратимыми, кроме того, может протекать не одна, а несколько реакций, конкурирующих между собой, а значит продуктами реакции будет смесь различных соединений. Поэтому и форма записи органических реакций тоже несколько другая. Т.е. используют не химические уравнения, а схемы химических реакций, в которых нет коэффициентов, но зато подробно указаны условия реакции. Принято также под уравнением записывать названия орг. веществ и тип реакции.
Но в целом органические вещества и реакции подчиняются общим законам химии, а органические вещества превращаются в неорганические или могут образовываться из неорганических. Что еще раз подчеркивает единство окружающего нас мира.
Основные принципы теории химического строения, изложенные молодым А.М.Бутлеровым на международном съезде естествоиспытателей в 1861 г.
1). Атомы в молекулах соединены между собой в определенном порядке, в соответствии с их валентностью. Последовательность соединения атомов называют химическим строением .
Валентность - это способность атомов образовывать определенное количество связей (ковалентных). Валентность зависит от числа неспаренных электронов в атоме элемента, потому что ковалентные связи образуются за счет общих электронных пар при спаривании электронов. Углерод во всех органических веществах четырехвалентен. Водород - 1, Кислород -П, азот – Ш, сера – П, хлор – 1.
Способы изображения органических молекул.
Молекулярная формула – условное изображение состава вещества. Н2СО3 - угольная кислота, С12Н22О11 – сахароза. Такие формулы удобны для расчетов. Но они не дают информацию о строении и свойствах вещества. Поэтому даже молекулярные формулы в органике пишут особым образом: СН3ОН. Но гораздо чаще пользуются структурными формулами. Структурная формула отражает порядок соединения атомов в молекуле (т.е. химическое строение). И в основе любой органической молекулы лежит углеродный скелет – это цепочка связанных между собой ковалентными связями атомы углерода.
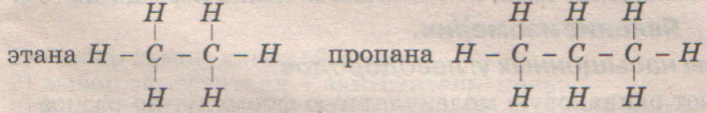 Полная структурная формула показаны все связи черточками. Химическая связь, образованная одной парой электронов, называется одинарной и в структурной формуле изображается одной черточкой. Двойная связь (=) образована двумя парами электронов. Тройная (≡) образована тремя парами электронов. И общее количество этих связей должно соответствовать валентности элемента.
Полная структурная формула показаны все связи черточками. Химическая связь, образованная одной парой электронов, называется одинарной и в структурной формуле изображается одной черточкой. Двойная связь (=) образована двумя парами электронов. Тройная (≡) образована тремя парами электронов. И общее количество этих связей должно соответствовать валентности элемента.
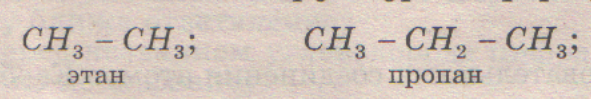 В сжатой структурной формуле опускаются черточки одинарных связей, а атомы, связанные с тем или иным атомом углерода, пишутся сразу после него (иногда в скобках).
В сжатой структурной формуле опускаются черточки одинарных связей, а атомы, связанные с тем или иным атомом углерода, пишутся сразу после него (иногда в скобках).
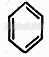 Еще более сокращенными являются скелетные формулы. Но они используются реже. Например:
Еще более сокращенными являются скелетные формулы. Но они используются реже. Например:
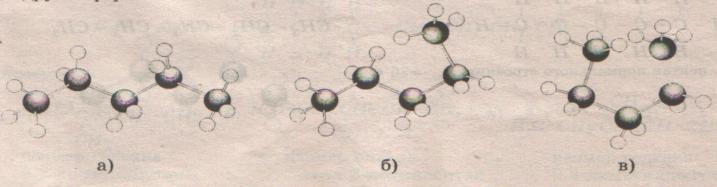 Структурные формулы отражают только порядок соединения атомов. Но молекулы органических соединений редко имеют плоское строение. Объемный образ молекулы важен для понимания многих химических реакций. Пространственное строение молекулы описывают с помощью таких понятий как длина связи и валентный угол. Наглядное представление о форме молекулы в пространстве дают молекулярные модели или специальные формулы.
Структурные формулы отражают только порядок соединения атомов. Но молекулы органических соединений редко имеют плоское строение. Объемный образ молекулы важен для понимания многих химических реакций. Пространственное строение молекулы описывают с помощью таких понятий как длина связи и валентный угол. Наглядное представление о форме молекулы в пространстве дают молекулярные модели или специальные формулы.