Часть 1
При выполнении заданий этой части в бланке ответов № 1 под номером выполняемого вами задания (А1 – А28) поставьте знак « ´ » в клеточку, номер которой соответствует номеру выбранного вами ответа.
А1 Какая электронная конфигурация внешнего энергетического уровня соответствует атому элемента IVA группы?
| 1) | 3 s 23 p 2; | 2) | 3 s 23 p 4; | 3) | 4 s 23 d 6; | 4) | 2 s 22 p 6. |
А2 В каком ряду химические элементы расположены в порядке уменьшения их атомного радиуса?
| 1) | F → Cl → Br; | 2) | Be → Mg → Ca; |
| 3) | Mg→ Al→ Si; | 4) | Sc → Ca → K. |
А3 Верны ли следующие суждения?
А. Элементы IА группы образуют водородные соединения состава RH.
Б. Химическая активность элементов в ряду Na→Mg→Al возрастает.
1) верно только А; 2) верно только Б;
3) верны оба суждения; 4) оба суждения неверны.
А4 Вещества с ковалентной полярной связью находятся в ряду:
| 1) | NH3, PCl3, HCl; | 2) | KBr, HCl, CF4; |
| 3) | CO, N2, HI; | 4) | SO3, NO, Cl2. |
А5 Степень окисления, равную +2, атом углерода имеет в соединении:
| 1) | CH2O; | 2) | HCOONa; | 3) | CH3Br; | 4) | CH3SH. |
А6 Молекулярный тип кристаллической решетки реализуется в соединении:
| 1) | NaBr | 2) | SiO2 | 3) | Cu(NO3)2 | 4) | CO2 |
А7 В перечне веществ:
А. СH3OH.
Б. H2S.
В. СH3COOH.
Г. NH3.
Д. HCOOH.
Е. CH3CHO.
кислотами являются:
| 1) | АБВ; | 2) | БBД; | 3) | БГД; | 4) | ВДЕ. |
А8 Медь реагирует с каждым из двух веществ:
| 1) | NaCl, ZnCl2; | 2) | HgSO4, HCl; | 3) | Al2O3, Na2CO3; | 4) | HNO3, Cl2. |
А9 Оксид серы (IV) взаимодействует с каждым из двух веществ:
| 1) | вода и серная кислота | 2) | оксид калия и оксид углерода (VI) |
| 3) | оксид кальция и гидроксид калия | 4) | вода и железо |
А10 Гидроксид цинка реагирует с каждым из двух веществ:
| 1) | HCl и Fe; | 2) | CO и H2O; | 3) | NaCl и NH3; | 4) | NaOH и HNO3. |
А11 Гидросульфит натрия реагирует с каждым из двух веществ:
| 1) | NaOH и HCl | 2) | Pb и KNO3 | 3) | H2SO4 и Na2SO4 | 4) | NaNO3 и NaOH |
А12 В схеме превращений

веществами «X1 » и «X2 » могут быть соответственно:
| 1) | SO3 и HNO3; | 2) | H2SO4 и Ba(NO3)2; |
| 3) | K2SO4 и HNO3; | 4) | H2SO4 и KNO3. |
А13 Изомером бутина-1 является:
| 1) | 2-метилбутадиен-1,3; | 2) | бутен-2; |
| 3) | циклобутан; | 4) | 1-метилциклопропен. |
А14 Бромной водой можно отличить следующие соединения:
| 1) | толуол и бутен-2 | 2) | бензол и гексан |
| 3) | гексен-1 и пропин | 4) | бутадиен-1,3 и пропен |
А15 Пропанол-1реагирует с каждым из двух веществ:
| 1) | СH3CH3 и CuO | 2) | Cu(OH)2 и O2 |
| 3) | O2 и СH3COH | 4) | СH2O и H2 |
А16 Верны ли следующие суждения о свойствах глюкозы:
А. Глюкоза окисляется аммиачным раствором оксида серебра.
Б. Глюкоза вступает в реакцию со свежеосажденным гидроксидом меди (II).
| 1) | верно только А | 2) | верно только Б |
| 3) | верны оба суждения | 4) | оба суждения неверны |
А17 Этилацетат образуется при взаимодействии:
| 1) | муравьиной кислоты и этанола; | 2) | уксусной кислоты и метанола; |
| 3) | этаналя и метанола; | 4) | уксусной кислоты и этанола. |
А18 В схеме превращений

веществами «X1 » и «X2 » могут быть соответственно:
| 1) | С2Н4 и С2Н5ОН; | 2) | С2Н4 и СH3CHO; |
| 3) | С2Н2 и С2Н6; | 4) | СH3CHO и С2Н4. |
А19 К реакциям замещения относится взаимодействие брома:
| 1) | с этиленом; | 2) | водородом; |
| 3) | пропаном; | 4) | бромидом железа (II). |
А20 С наибольшей скоростью с водородом реагирует:
| 1) | Cl2; | 2) | N2; | 3) | P; | 4) | S. |
А21 Химическое равновесие в системе
CO2 (г) + C (тв) 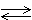 2CO(г) - Q
2CO(г) - Q
смещается в сторону образования продукта реакции при
| 1) | понижения давления | 2) | понижении температуры |
| 3) | повышения давления | 4) | понижении концентрации CO2 |
А22 Сильными электролитами являются:
| 1) | Н3РО4 и Ag3PO4; | 2) | Fe(OH)3 и H2SO4; |
| 3) | Zn(OH)2 и H2S; | 4) | НСl и AgNO3. |
А23 С выделением газа протекает реакция ионного обмена между растворами:
| 1) | нитрата бария с сульфатом натрия; |
| 2) | хлорида меди (II) с гидроксидом калия; |
| 3) | сульфита натрия с соляной кислотой; |
| 4) | соды с гидроксидом бария. |
А24 Среда раствора фосфата натрия:
| 1) | щелочная; | 2) | кислая; |
| 3) | слабокислая; | 4) | нейтральная. |
А25 Оксид серы (IV) является восстановителем в реакции, уравнение которой:
| 1) | SO2 + 2NaOH = Na2SO3 + H2O; | 2) | SO2 + 2H2S = 3S + 2H2O; |
| 3) | SO2 +H2O  H2SO3; H2SO3;
| 4) | 2SO2 + O2  2 SO3. 2 SO3.
|
А26 Раствор перманганата калия можно использовать для обнаружения:
| 1) | циклогексана; | 2) | бензола; |
| 3) | гексана; | 4) | этилена. |
А27 Сырьем для получения метанола в промышленности служат:
| 1) | СО и Н2; | 2) | НСНО и Н2; |
| 3) | СН3С1 и NaOH; | 4) | НСООН и NaOH. |
А28 Объем углекислого газа (при н.у.), полученного из 12,5 г мрамора, содержащего 80% карбоната кальция, по уравнению реакции
СaCO3 + 2HCl = CaCl2 + CO2 + H2O,
равен:
| 1) | 2,8 л | 2) | 2,24 л | 3) | 1,12 л | 4) | 4,48 л |
Часть 2
Ответом к заданиям этой части (В1 – В10) является набор цифр или число, которые следует записать в бланк ответов № 1 справа от номера соответствующего задания, начиная с первой клеточки. Каждую цифру и запятую в записи десятичной дроби пишите в отдельной клеточке в соответствии с приведенными в бланке образцами.
В заданиях В1 – В5 на установление соответствия к каждой позиции первого столбца подберите соответствующую позицию второго и запишите в таблицу выбранные цифры под соответствующими буквами. Затем получившуюся последовательность цифр перенесите в бланк ответов № 1 без пробелов и других символов. (Цифры в ответе могут повторяться.)
B1 Установите соответствие между формулой вещества и классом (группой) органических соединений, к которому(-ой) оно принадлежит.
| Формула вещества | Класс (группа) органических соединений |
| А) С6Н12О6 | 1) простые эфиры |
| Б) С6Н5С2Н5 | 2) сложные эфиры |
| В) С6Н5СН2ОН | 3) углеводороды |
| Г) C6H5COOCH3 | 4) углеводы |
| 5) альдегиды | |
| 6) спирты |
| А | Б | В | Г |
B2 Установите соответствие между формулой иона и степенью окисления центрального атома в нем.
| Формула иона | Степень окисления |
| А) РСl4+ | 1) +7 |
| Б) РСl4– | 2) +2 |
| В) S2O72– | 3) +3 |
| Г) SF22+ | 4) +4 |
| 5) +5 | |
| 6) +6 |
| А | Б | В | Г |
B3 Установите соответствие между формулой вещества и продуктами электролиза его водного раствора:
| формулы веществ | продукты элеКтролиза | ||
| А) | NaOH | 1) | Hg, NO2, |
| В) | Fe2(SO4)3 | 2) | Fe, O2, |
| В) | KNO3 | 3) | K, H2, SO3 |
| Г) | Hg(NO3)2 | 4) | Fe, H2, O2 |
| 5) | Hg, O2 | ||
| 6) | H2, O2 |
| А | Б | В | Г |
B4 Установите соответствие между формулой соли и концентрациями ионов водорода и ионов гидроксида в растворе этой соли.
| Формула соли | Концентрация [Н+] и [ОН–] |
| А) FeI2 | 1) [Н+] = [ОН–] |
| Б) Na2S | 2) [Н+] > [ОН–] |
| В) CsCl | 3) [Н+] < [ОН–] |
| Г) Be(NO3)2 |
| А | Б | В | Г |
B5 Установите соответствие между реагирующими веществами и продуктами реакции, содержащими кремний.
| Реагирующие вещества | Продукты реакции |
| А) Si + Mg → | 1) SiH4 |
| Б) Si + NaOH → | 2) H2SiO3 |
| В) Ca2Si + H2O → | 3) Na2SiO3 |
| Г) SiO2 + Mg → | 4) Mg2Si |
| 5) CaSiO3 | |
| 6) Si |
| А | Б | В | Г |
Ответом к заданиям B6–B8 является последовательность из трёх цифр, которые соответствуют номерам правильных ответов. Запишите эти цифры в порядке возрастания сначала в текст работы, а затем перенесите их в бланк ответов № 1 без пробелов, запятых и других дополнительных символов.
B6 Реакция бромирования пропана протекает:
| 1) по радикальному механизму; |
| 2) в несколько стадий; |
| 3) с разрывом связи в молекуле брома в начале реакции; |
| 4) в соответствии с правилом В.В. Марковникова; |
| 5) в присутствии катализатора; |
| 6) с преимущественным образованием 1-бромпропана. |
Ответ: ________________.
B7 Олеиновая кислота может взаимодействовать:
| 1) | с сульфатом калия; | 4) | водородом; |
| 2) | натрием; | 5) | оксидом углерода (IV); |
| 3) | сульфидом меди (II); | 6) | бромной водой. |
Ответ: ________________.
B8 Аланин может взаимодействовать:
| 1) | с водородом; | 4) | бромоводородом; |
| 2) | бензолом; | 5) | этиловым спиртом; |
| 3) | сульфатом кальция; | 6) | соляной кислотой. |
Ответ: ________________.
Ответом к заданиям В9, В10 является число. Запишите это число в текст работы, а затем перенесите его в бланк ответов № 1 без указания единиц измерения.
B9 Какую массу оксида калия необходимо взять для приготовления 280 г раствора гидроксида калия с массовой долей 2%? Ответ: ____ г. (Запишите число с точностью до десятых.)
B10 Какой объем (н.у.) кислорода образуется при разложении оксида ртути (II), если количество полученной при этом ртути 0,5 моль? Ответ: ____ л. (Запишите число с точностью до десятых.)
Не забудьте перенести все ответы в бланк ответов № 1
Часть 3
| Для записи ответов к заданиям этой части (С1 – С5) используйте бланк ответов № 2. Запишите сначала номер задания (С1 и т.д.), а затем полное решение. Ответы записывайте четко и разборчиво. |
С1 Используя метод электронного баланса, составьте уравнение реакции:
C6H5—C2H5+ KMnO4 = MnO2 + … +… + … + …
Определите окислитель и восстановитель.
С2 К раствору, полученному при растворении сульфида хрома (III) в соляной кислоте, добавили раствор карбоната натрия. Полученный осадок растворили в избытке раствора гидроксида калия, затем после добавления дополнительно раствора гидроксида калия через этот раствор пропустили газообразный хлор.
Напишите уравнения описанных реакций.
С3 Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
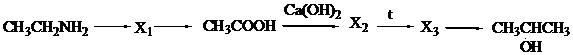
С4 К 180 г 10,6%-го раствора карбоната натрия медленно добавили 120 г 5,7%-го раствора сульфата алюминия. Выпавший осадок отфильтровали. Вычислите массовые доли соединений, содержащихся в полученном фильтрате.
С5 Установите молекулярную формулу монокарбоновой кислоты, массовая доля кислорода в котором равна 26,23%.