Кристаллизация
Движущая сила кристаллизации
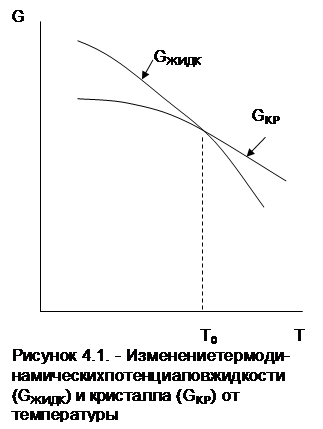
Переход металла или сплава из жидкого состояния в твёрдое с образованием кристаллической структуры называется первичной кристаллизацией. Движущейсилойкристаллизации, как и других фазовыхпревращений, являетсявыигрыштермодинамическогопотенциала (рис. 4.1), т.е. должна освобождаться энергия, так как любая система при конкретных условиях стремится к минимальной энергии.
 При этом полная энергия системы Е состоит из суммы свободной энергии F и ТS (T-температура системы, К; S – энтропия), т.е.
При этом полная энергия системы Е состоит из суммы свободной энергии F и ТS (T-температура системы, К; S – энтропия), т.е.
Е = F + TS (4.1)
Следовательно
F = Е - TS (4.2)
(термодинамический потенциал Гельмгольца)
Однако чаще пользуются термодинамическим потенциалом Гиббса G.
G = F + pV (4.3)
где p – давление, V – объём.
Для конденсированных систем D(pV) ® 0, поэтому DG»DF
Представим график зависимости G=f(T) (рис. 4.1)
При Т0Gж = Gтв, т.е.
Eж – T0*Sж = Eтв – T0*Sтв
Теплота кристаллизации Q представляет собой разницу
Eж – Eтв = T0*(Sж - Sтв) (4.4)
Следует учесть, что Q = T0*DS> 0, т.к. Sж>Sтв, т.е. тепловой эффект положителен и при кристаллизации тепло выделяется. С этим связана наблюдаемая площадка на кривых охлаждения.
Кристаллизация возможна, если есть какое-то переохлаждениеDТ относительно То. ОтDТ зависит скорость зарождения и скорость роста кристаллов, а как следствие характер структуры.
Это означает, что при переохлаждении относительно температуры кристаллизации более выгодным становится кристаллическое состояние вещества. Однако при более подробном рассмотрении ситуации все оказывается не так просто и при небольших переохлаждениях кристаллизация может не происходить даже в металлах.
Гомогенная кристаллизация
|
|
Следует учитывать, что суммарное изменение термодинамического потенциала DGS при фазовых превращениях состоит как минимум из двух слагаемых: выигрыш (снижение) потенциала за счет образования в каком-то объеме более устойчивой фазы DGV и проигрыш (возрастание) потенциала за счет образования границ раздела между старой и новой фазами.DGS
DGS=-DGV+DGS (4.5)
 Границы раздела - это всегда участки с повышенным значением термодинамического потенциала за счет возникающего между фазами поверхностного натяжения. Наименьшую энергию на поддержание системы в равновесии имеет тело равноосной формы, т.е. шара. Если поперечный размер возникающего равноосного кристалла - r, то термодинамический энергетический выигрыш (снижение DGV) пропорционален r3, а проигрыш (повышение DGS) - r2 (рис 4.2).
Границы раздела - это всегда участки с повышенным значением термодинамического потенциала за счет возникающего между фазами поверхностного натяжения. Наименьшую энергию на поддержание системы в равновесии имеет тело равноосной формы, т.е. шара. Если поперечный размер возникающего равноосного кристалла - r, то термодинамический энергетический выигрыш (снижение DGV) пропорционален r3, а проигрыш (повышение DGS) - r2 (рис 4.2).
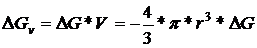 (4.6)
(4.6)
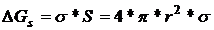 (4.7)
(4.7)
Определим критический размер частицы r, а для этого продифференцируем DGS по r и приравняем к 0.
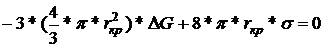 ;
;
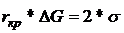 Þ
Þ 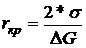
Следовательно суммарная кривая имеет максимум при r= rкр. Таким образом зарождающиеся кристаллы с r<rкр энергетически невыгодны и самопроизвольно растворяются, а существование кристаллических участков с r>rкр является термодинамически выгодным и они самопроизвольно растут. Следует учесть, что коэффициент поверхностного натяжения s слабо зависит от температуры, а DG заметно растет при повышении переохлаждения DТ. Отсюда следует, что rкр тем меньше, чем больше переохлаждение. Так, например, для железа приDТ = 10° rкр = 100нм, а при DТ = 100°, rкр = 10нм.
Зарождение кристаллов, т.е. участков по строению подобных кристаллическому (кластеров), в расплаве – процесс статистический, поэтому, чем меньше rкр, тем больше вероятность зарождения кристаллов с r>rкр, а значит в единице объема количество зародившихся кристаллов оказывается большим, а их окончательный размер – меньшим. Таким образом, меняя величину переохлаждения, т.е. скорость охлаждения при кристаллизации, можно оказывать влияние на структуру, а значит и на свойства отливок.
|
|