ПОЛУЧЕНИЕ АЛКАНОВ.
Очень много метана на тяжёлых планетах таких как Юпитер, Уран, Сатурн, Нептун, атмосферы этих планет богаты водородом, а потому образуют восстановительную атмосферу богатую аммиаком, метаном.
На нашей планете сила тяжести на много слабее, а потому водород удерживать не может. И потому Земля имеет окислительную атмосферу богатой кислородом, азотом. При этом метана образуется примерно 2×107 за счет бактерий «метаногенов».
Алканы выделяют из природных источников (природный и попутный газ, нефть, каменный уголь).
Газообразные алканы получают из природного и попутных нефтяных газов, а твердые алканы — из нефти. Природной смесью твердых высокомолекулярных алканов является горный воск — природный битум.
Метан широко распространен в природе. Он является главной составной частью многих горючих газов как природных (80-97%), так и искусственных, выделяющихся при сухой перегонке дерева, торфа, каменного угля, а также при крекинге нефти. Природные газы, особенно попутные газы нефтяных месторождений, помимо метана содержат этан, пропан, бутан и пентан.
Метан выделяется со дня болот (до 99%) и из каменноугольных пластов в рудниках, где он образуется при медленном разложении растительных остатков без доступа воздуха. Поэтому метан часто называют болотным или рудничным газом.
В ПРОМЫШЛЕННОСТИ
1. Получение алканов из природных источников (нефть, природный газ)

2. Метод Фишера – Тропша (Гидрирование СО)
Смесь (CO и H2) называют синтез газом или водяным газом
I – стадия:
C + H2O → CO + H2
CO ≈ 44%
H2 ≈ 45 %
II – стадия:
Синтезом из водяного газа (СО+Н2) получают смесь алканов:

Синтезом на основе водяного газа из оксида углерода (III) и водорода можно получить метан:
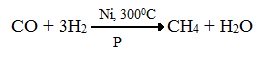
В ЛАБОРАТОРИИ
1. Каталитическая гидрогенизация
n C + (n+1) H2  → CnH2n+2
→ CnH2n+2
Метан можно получить синтезом из простых веществ при нагревании, повышенном давлении в присутствии катализатора (Ni, Fe или других d – элементов):

Перспектива реакции в получении синтетического бензина.
2. Восстановление галогеналканов.
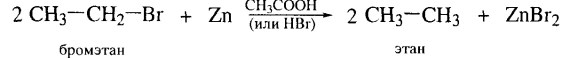
3. Разложение реагентов Гриньяра водой
Реагенты Гриньяра –соединения, отвечающие общей формуле R–MgX, где R-радикал X-атом галогена.
1. Получение реактива Гриньяра:

Связь C-Mg на 80 % ионная, 20 % ковалентная.
2. Для получения алканов достаточно подействовать на реактивы Гриньяра водой, спиртами, кислотами.

Воздействие воды на другие металлорганические соединения

4. Взаимодействие галогеналканов с щелочными металлами (реакция Вюрца)
Происходит димеризация углеродной цепи исходного галогеналкана, образуется алкан с четным числом атомов углерода в цепи:
R-Г + 2Na + Г-R1 → R-R1 + 2NaГ
(R- это радикал; Г- это галоген)

Если в реакции участвуют разные галогеналканы, то образуется смесь алканов:

5. Гидролиз карбида алюминия (получение метана)


6. Декарбоксилирование карбоновых кислот и их солей.
Декарбоксилирование — это реакция элиминирования молекулы диоксида углерода из карбоксильной группы (-COOH) или карбоксилатной (-COOMe) группы органических соединений:

Реакция элиминирования (от лат. elimino — изгоняю) — процесс отщепления от молекулы органического соединения атомов или атомных групп без замены их другими. Исходными веществами могут служить представители разных классов органических соединений.
{\displaystyle {\mathsf {RCOOH\rightarrow RH+CO_{2}}}}Сплавление солей уксусной кислоты со щелочами (реакция Дюма)
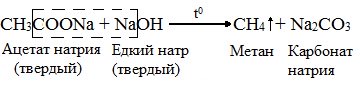
7. Каталитическое гидрирование (+Н2) непредельных углеводородов

8. Электролиз растворов солей карбоновых кислот (реакция Кольбе)

ТИПЫИ МЕХАНИЗМЫРЕАКЦИЙ В ОРГАНИЧЕСКОЙ ХИМИИ
Существуют разные системы классификации органических реакций, которые основаны на различных признаках. Среди них можно выделить классификации:
· по конечному результату реакции, то есть изменению в структуре субстрата;
· по механизму протекания реакции, то есть по типу разрыва связей и типу реагентов.
Взаимодействующие в органической реакции вещества подразделяют на реагент и субстрат. При этом считается, что реагент атакует субстрат.
Реагент и субстрат
ОПРЕДЕЛЕНИЕ
Реагент — вещество, действующее на объект — субстрат — и вызывающее в нем изменение химической связи. Реагенты делятся на радикальные, электрофильные и нуклеофильные.
ОПРЕДЕЛЕНИЕ
Субстратом, как правило, считают молекулу, которая предоставляет атом углерода для новой связи.