Дайте характеристику общих реакций идентификации алкалоидов. Какие химические процессы лежат в осадочных и цветных реакций алкалоидов. Приведите пример общих алкалоидов осаждаясь и специальных реактивах.
Алкалоиды — группа органических веществ, вырабатываемых различными растениями, которые принято называть ядовитыми (белена, красавка, чемерица и др.), содержащие в своей молекуле азот и обладающие высокой физиологической активностью (аконитин, атропин, лупинин, никотин, анабазин). Некоторые из алкалоидов обладают исключительно высокой токсичностью. Так, смертельная доза аконитина для животных при введении внутрь составляет 0,02—0,05 мг/кг (И. А. Гусынин, 1947). Отмечены случаи отравлений крупного рогатого скота и лошадей при поедании сена с примесью чемерицы, содержащей алкалоиды протовератрин и йервин. Для диагностики отравлений исследуют на алкалоиды растительные корма, с которыми связана интоксикация животных. Для определения в кормах алкалоидов в основном используют реакции осаждения и колориметрии.
Принцип. Метод основан на экстракции алкалоидов из щелочной среды хлороформом и идентификации их посредством специфических реакций с различными реагентами — Эрдмана, Ман- делина, Вагнера, Драгендорфа, растворами танина, пикриновой, серной и азотной кислот (Сметов с соавт., 1987).
Реактивы: алкалоиды аконитин, атропин, берберин, бруцин, колхицин, кураре, дигитамин, дигитоксин, морфин, никотин, фи- зостиомин, пикротоксин, соланин, стрихнин, вератрин и др.; аммония ванадат мета (ч. д. а.); висмута нитрат (ч. д. а.); йод элементный (ч. д. а.); калия гидроксид (ос. ч.); калия йодид (х. ч.); кислота азотная (х. ч.); кислота серная (ос. ч.); кислота хлористоводородная (х. ч.); кислота пикриновая (ч. д. а.);
3%-ный раствор натрия гидроксида (х. ч.); реактив I: концентрированная серная кислота; реактив II: концентрированная азотная кислота; реактив III (Эрдмана). К 20 мл концентрированной серной кислоты прибавляют азотную кислоту (10 капель кислоты на 100 мл дистиллированной воды);
реактив IV (Манделина). Свежеприготовленный раствор: 0,01 г аммония ванадата в 2 мл концентрированной серной кислоты;
реактив V (Вагнера). 5 г йода в 100 мл 10%-ного раствора калия йодида;
реактив VI: 5%-ный водный раствор танина; реактив VII: 1%-ный водный раствор пикриновой кислоты; реактив VIII (Драгендорфа). 8 г висмута нитрата растворяют в 20 мл азотной кислоты, полученный раствор вливают в концентрированный раствор калия йодида (27,2 г соли в 20 мл воды), через сутки фильтруют, объем фильтрата доводят до 100 мл дистиллированной водой;
реактив тимолфталеиновый.
Предложите возможные методы индентификации йодоформа. Где это возможно, приведите уравнения химических реакций.
Йодоформ ГФ Х
Iodoformium
CHI 3
Formylum triiodatum
Химическое название: трийодметан, формилтрийодид
Йодоформ (Iodoformium)
CHI3
Трийодметан
Добыча. Йодоформ получают электролизом раствора калия йоди-
Да в присутствии натрия карбоната и этилового спирта
или реакцией:
C2H5OH + 4I2 + 3Na2CO3 → CHI3 ↓ + 5NaI + HCOONa + 2H2O + 3CO2 ↑
Идентификация
Разложение (окисления) субстанции
При нагревании препарата в пробирке на пламени выделяются фиолетовые пары йода I 2:
2CHI 3 + 2O 2 = 3 I 2 + CO + CO 2 + H 2 O
Омыление спиртовым раствором щелочи
Субстанцию растворяют в спиртовом растворе калий гидроксида KOH, а затем полученный раствор подкисляют азотной кислотой HNO 3; образуется желтое окрашивание йода I 2:
CHI 3 + 4KOH → 3KI + НСООК + 2Н 2 О
6KI + 8HNO 3 = 2 I 2 + 6KNO 3 + 2NO + 2H 2 O
Применение. Наружное антисептическое средство
Применяют наружно как антисептическое средство в виде присыпок, паст, эмульсий, мазей для лечения инфицированных ран, язв. Принцип антисептического действия заключается в том, что в отличие от хлороформа, в молекуле йодоформа атомы Йода связанные непрочно и поэтому препарат, медленно разлагаясь к свободному йода I 2, обнаруживает длительную антисептическим действием. Попадая на пораженные ткани (раны, язвы) при столкновении с кровью или другими жидкостями организма, которые содержат окислительный фермент каталазу, йодоформ оказывает действие, аналогичное йода.
Большим недостатком йодоформа является его неприятный специфический запах.
3) Охарактеризуйте возможные методы количественного определения кальция хлорида. Приведем уравнения реакций, формулы вычисления массовой доли (%). Укажите молярные массы эквивалентов.
Calcii chloridum
Кальция хлорид
Calcium chloratum
СаС12 * 6Н20 М. в. 219,08
Описание. Бесцветные кристаллы без запаха, горько-соленого вкуса. Препарат очень гигроскопичен, на воздухе расплывается.
Растворимость. Очень легко растворим в воде, вызывая при этом сильное охлаждение раствора, легко растворим в 95% спирте.
Подлинность. Препарат дает характерные реакции на кальций и хлориды (стр. 744; 747).
Прозрачность и цветность раствора. Раствор 1 г препарата в 10 мл воды должен быть прозрачным и бесцветным.
Вещества, нерастворимые в 95% спирте. 0,5 г препарата должны полностью растворяться в 5 мл 95% спирта, образуя прозрачный бесцветней раствор.
Кислотность или щелочность. 1 г препарата растворяют в 20 мл све-жепрокипяченной и охлажденной воды, прибавляют 1 каплю раствора метилового красного. Окраска раствора должна изменяться от прибавления не более 0,05 мл 0,01 н. раствора едкого натра или соляной кислоты.
Сульфаты. 4 г препарата растворяют в 20 мл воды. 10 мл полученного раствора должны выдерживать испытание на сульфаты (не более 0,005% в препарате).
Тяжелые металлы. 5 мл того же раствора, разведенные водой до 10 мл, должны выдерживать испытание на тяжелые металлы (не более 0,0005% в препарате).
Железо. Раствор 15 г препарата в 10 мл воды должен выдерживать испытание на железо (не более 0,0002% в препарате).
Барий. 2 г препарата растворяют в 40 мл воды. К 10 мл полученного раствора прибавляют 5 мл насыщенного раствора сульфата кальция; в течение 1 часа в растворе не должна появляться муть.
Железо, алюминий, фосфаты. К 10 мл того же раствора прибавляют 1 мл раствора хлорида аммония, 1 каплю раствора фенолфталеина и раствор аммиака до появления розового окрашивания; в полученном растворе ни при комнатной температуре, ни при кипячении не должна появляться муть.
Соли магния и щелочных металлов. 20 мл того же раствора нагревают до кипения. К горячему раствору прибавляют 0,5 г хлорида аммония, раствора аммиака до щелочной реакции и 20 мл горячего раствора оксалата аммония. После охлаждения выпавший осадок отфильтровывают. К 20 мл фильтрата прибавляют 0,5 мл концентрированной серной кислоты и выпаривают до полного удаления аммонийных солей, остаток прокаливают до постоянного веса. Остаток не должен превышать 0,5%.
Цинк. Раствор 1 г препарата в 10 мл воды не должен давать реакции на цинк.
Мышьяк. 0,5 г препарата должны выдерживать испытание на мышьяк (не более 0,0001% в препарате).
Количественное определение. Около 0,8 г препарата (точная навеска), отвешенные в закрытом бюксе, растворяют в воде, переносят в мерную колбу емкостью 100 мл, доводят объем раствора водой до метки и тщательно перемешивают.
К 25 мл приготовленного раствора прибавляют 5 мл аммиачного буферного раствора, 0,1 г индикаторной смеси или 7 капель раствора кислотного хром темно-синего и титруют 0,05 мол раствором трилона Б до сине-фиолетового окрашивания.
1 мл 0,05 мол раствора трилона Б соответствует 0,01095 г СаCl2 * 6Н20, которого в препарате должно быть не менее 98,0%.
Хранение. В небольших, хорошо укупоренных стеклянных банках с пробками, залитыми парафином, в сухом месте.
Источник ионов кальция; антиаллергическое средство.
Особенности определения чистоты бария сульфата для рентгеноскопии.
Бария сульфат для рентгеноскопии Barii sulfas pro roentgeno
BaS04 М. м. 233,43
Для получения бария сульфата, предназначенного для медицинских целей, используют природный карбонат бария (витерит), который обрабатывают хлороводородной кислотой, получая растворимую соль бария - хлорид бария ВаС12. К раствору полученной соли бария добавляют сульфат натрия или магния, при этом тотчас выпадает осадок бария сульфата.
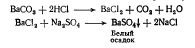
Чтобы бария сульфат получился мелкодисперсный, к растворам хлорида бария и сульфата натрия добавляют льняное семя или другой слизистый отвар, котррый,играет роль защитг
ного коллоида при образовании сульфата бария. Осадок бария сульфата тщательно промывают, чтобы удалить примеси, особенно хлорид-ионы. Если в промывных водах обнаруживается С1~, то можно предполагать наличие в препарате примеси растворимой соли хлорида бария. Препарат отмывается также и от иона SCU2-.
Бария сульфат представляет собой белый рыхлый тяжелый порошок без запаха и вкуса. Подлинность его непосредственно определить невозможно из-за нерастворимости этой соли. Поэтому бария сульфат переводят сначала в растворимые соединения, которые диссоциируют с образованием ионов Ва2+ и SO42-. Для этого препарат нагревают с карбонатом натрия.

Осадок отфильтровывают, в фильтрате определяют S042- путем добавления хлорида бария, при этом выпадает белый осадок сульфата бария.

Осадок, представляющий собой карбонат бария, обрабатывают хлороводородной кислотой, чтобы перевести его в растворимую соль (хлорида бария), в которой легко подтвердить наличие иона Ва2+осаждением его серной кислотой.

Эта реакция является фармакопейной.
Летучие соли бария (ВаС12) окрашивают пламя горелки в желто-зеленый цвет.
Бария сульфат применяется внутрь в больших дозах (50- 100 г), поэтому ГФ X предъявляет строгие требования к чистоте препарата. Он не должен содержать примесей растворимых солей бария, причем растворимых не только в воде (ВаСЬ), но в кислотах (ВаСОз, BaS).
Не допускается в препарате примесь сульфитов, мышьяка. Мышьяк может попасть в препарат в том случае, если при получении бария сульфата использовались не сульфаты натрия и магния, а сама серная кислота, которая может содержать примесь мышьяка. ГФ X допускает в препарате примеси хлоридов, сульфатов, тяжелых металлов в пределах, установленных эталонами.
Чтобы обнаружить возможные примеси, из препарата делают несколько вытяжек:
- обрабатывают препарат уксусной кислотой и делают пробы на растворимые в воде соли бария и карбонат бария (с серной: кислотой не должно появляться осадка в течение часа);
- обрабатывают препарат хлороводородной кислотой и открывают сульфид бария, железо и соли других тяжелых металлов;
- водная вытяжка должна быть нейтральна и может содержать лишь следы хлоридов и сульфатов;
- обрабатывают препарат азотной кислотой и определяют с молибдатом аммония фосфаты бария и кальция.
Особенно тщательно препарат исследуют на карбонат и сульфид бария. При наличии примесей вытяжка, полученная при обработке препарата хлороводородной кислотой, будет иметь запах сероводорода. Однако одной органолептической пробы в этом случае недостаточно, поэтому вытяжку препарата помещают в пробирку, накрывают фильтровальной бумагой, смоченной раствором ацетата свинца, и нагревают. При наличии примеси сульфида бария BaS выделяющийся сероводород, реагируя с ацетатом свинца, вызовет потемнение бумаги вследствие образования сульфида свинца PbS.

ГФ X требует определения степени дисперсности препарата.
Количественного определения препарата ГФ X не требует. Бария сульфат поступает в аптеку в фабричной упаковке - в плотно заклеенных двойных бумажных пакетах (внутренний пакет должен быть из пергаментной бумаги). В аптеках препарат не расфасовывается. На этикетке должно быть полностью написано название препарата на русском и латинском языке. Указывается серия, дата выпуска, кем и когда проведен контроль качества препарата. Хранить препарат следует в хорошо закупоренных банках или пакетах отдельно от карбонатов калия, натрия.
5) Вычислить массовую долю (%) тропацина (М. 371,91) в субстанции, если масса анализируемого вещества составляет 0,1976 г, объем 0,1 М раствора хлорной кислоты (КП = 1,0014) в рабочем опыте - 5,43 мл, в контрольном - 0,18мл, а потеря в массе при высушивании составляет 0,4%.