Применяем 2 способ.
Оборудование: весы, газовая горелка с треножником, ступка, мерный
цилиндр.
Посуда: стаканы, колбы, воронки, фильтры бумажные, стеклянные палочки для перемешивания раствора.
Реактивы: бура техническая.
Для получения однородных кристаллов десятиводной буры необходимо продажную буру подвергнуть перекристаллизации, соблюдая следующее условие: раствор должен иметь температуру не выше 60оС, так как из растворов, имеющих температуру выше 60оС, выкристаллизовывается тетраборат натрия с непостоянным содержанием кристаллизационной воды, лишь приблизительно отвечающий формуле.
36 г буры при 600С растворяем в 150 мл воды. Полученный раствор быстро фильтруем через складчатый фильтр, вставленный в воронку для горячего фильтрования. Фильтрат сначала охлаждаем медленно до 25 - 300С, а затем быстро в снегу, усиливая кристаллизацию перемешиванием палочкой.
Для ускорения кристаллизации непрерывно перемешивают содержимое стакана стеклянной палочкой. В этих условиях бура выделяется из раствора в виде чрезвычайно мелких кристаллов. При медленном охлаждении получаются большие кристаллы, которые почти всегда содержат включения маточного раствора и непригодны для установки титра.
Выпавшие кристаллы отсасываем, промываем небольшим количеством ледяной воды и высушиваем между листами фильтровальной бумаги в течение 2-х дней. Высушенные кристаллы буры легко отстают от сухой палочки.
Расчеты
36 г безводной буры растворили при 600С в 150 мл воды.
После перекристаллизации по методике 2 масса чистой буры равна 54,20 г Na2B4O7*10H2O. Принимаем потери на фильтре нулевыми.
В 54,20 г Na2B4O7*10H2O содержится 54,2*201,42/381,42 = 28,62 г тетрабората натрия (безводной буры), где 201,42 г и 381,42 г – молярные массы безводной бура и Na2B4O7*10H2O соответственно.
Рассчитываем практический выход:

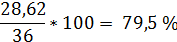
Выводы
1. Для получения однородных кристаллов десятиводной буры необходимо продажную буру подвергнуть перекристаллизации, соблюдая следующее условие: раствор должен иметь температуру не выше 60оС, так как из растворов, имеющих температуру выше 60оС, выкристаллизовывается тетраборат натрия с непостоянным содержанием кристаллизационной воды, лишь приблизительно отвечающий формуле.
2. Для ускорения кристаллизации непрерывно перемешивают содержимое стакана стеклянной палочкой. В этих условиях бура выделяется из раствора в виде чрезвычайно мелких кристаллов. При медленном охлаждении получаются большие кристаллы, которые почти всегда содержат включения маточного раствора и непригодны для установки титра.
3. Практический выход составил  .
.
Список литературы
1. Альмединген А. Н. Бура, фальсификация её // Энциклопедический словарь Брокгауза и Ефрона: в 86 т. (82 т. и 4 доп.). - СПб.: 1890 - 1907.
2. Герценштейн Г. М. Бура, в медицине // Энциклопедический словарь Брокгауза и Ефрона: в 86 т. (82 т. и 4 доп.). - СПб.: 1890 - 1907.
3. Глинка Н.Л. Общая химия. – Ленинград: 1987.
4. Левинсон-Лессинг Ф. Ю. Бура, нахождение в природе // Энциклопедический словарь Брокгауза и Ефрона: в 86 т. (82 т. и 4 доп.). - СПб.: 1890 - 1907.
5. Лидин Р.А.. Справочник по общей и неорганической химии. – М.: 1997.
6. Лидин Р.А., Молочко В.А., Андреева Л.Л. Химические свойства неорганических веществ. – М.: 1997.
7. Методичка НТУ «ХПИ». 1978 год, Харьков. Методические указания к лабораторным работам по органической химии.
8. Основы аналитической химии. В 2 кн. Кн.1. Общие вопросы. Методы разделения. Кн.2. Методы химического анализа: Учеб. для вузов/ Под ред. Ю.А. Золотова. - М.: Высш. шк., 2000.
9. Титриметрия с использованием кислотно-основной реакции (протолитометрия): Метод. указ. к лаб. раб./Сост. Б.М. Стифатов, Ю.В. Рублинецкая. – Самара: Самар. гос. тех. ун-т., 2013. - 34 с.
10. Химические свойства неорганических веществ: Учеб. пособие для вузов. Под ред. Лидина Р.А. – М.: «Химия», 1996.
11. Химическая энциклопедия/ Гл. редактор И.Л. Кнунянц. – М.: 1998.