Живые организмы представляют собой системы с очень развитыми поверхностями раздела, к которым относят кожные покровы, поверхность стенок кровеносных сосудов, слизистые оболочки, клеточные мембраны, мембраны ядер, митохондрий, лизосом.
Поверхностькожи взрослого человека составляет ~ 2,0 м2,
эритроцитов ~ 2500—3800 м2,
капилляров печени ~ около 400 м2,
альвеол ~ около 90-120 м2,
скелета ~ около 2 тыс. км2.
Ионная адсорбция
Основное влияние – радиус гидратированного иона.
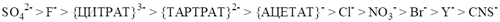
Li+>Na+>K+>Rb+>Cs+
Последние члены лиотропных рядов адсорбируются лучше!
Многозарядные ионы адсорбируются лучше!
Правило Панета-Фаянса
В первую очередь из растворов адсорбируются те ионы, которые входят в состав кристаллической решетки адсорбента(или изоморфны с ней - HS-, S2- на поверхность As2S3)
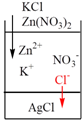
Явление избирательной адсорбции токсинов тканями и клетками наблюдаются в организме человека:
ü токсины возбудителей столбняка и ботулизма поражают ЦНС;
ü токсины возбудителей дизентерии – вегетативную нервную систему.
Введение в организм цианистых соединений (СN-) вызывает смерть через несколько секунд вследствие блокады железосодержащих дыхательных ферментов.
Ионообменная адсорбция - процесс, в котором адсорбент и раствор обмениваются между собой в эквивалентных количествах одноименно заряженными ионами.
Ионообменные смолы, или иониты, разделяют на
катиониты аниониты
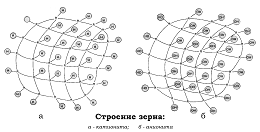
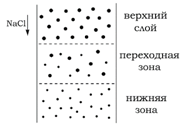 Весовая обменная емкость Гвес - число ммоль-эквивалентов ионов, поглощенных 1 г сухого ионита (ммоль-экв/г), находящимся в равновесии с раствором определенной концентрации.
Весовая обменная емкость Гвес - число ммоль-эквивалентов ионов, поглощенных 1 г сухого ионита (ммоль-экв/г), находящимся в равновесии с раствором определенной концентрации.
Динамическая обменная емкость Гполн. – число ммоль-экв ионов, поглощенных 1 г сухого ионита при полном поглощении ионов в динамических условиях.
Н+(кат)+Nа+(р-р) ↔ Н+(р-р)+Nа+(кат)
Определение динамической обменной емкости ионита(микроаналог схемы опреснения воды)
Н+(кат)+Nа+(р-р) ↔ Н+(р-р)+Nа+(кат)
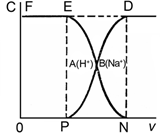
Выходные кривые обмена H+ на Na+
Иониты после использования легко регенерируются посредством обработки кислотой или щелочью
Применение ионитов
1. Разделение и очистка аминокислот и белков:(пепсин (рI=2), химотрипсин (рI=8.6) помещаются в аммиачный буфер с рН = 8.4. Пепсин заряжается отрицательно (рН>рI) и при пропускании смеси через катионит не вступает в реакцию обмена. Положительно заряженный химотрипсин (рН<рI) будет адсорбироваться на катионите
2. Консервирование крови
3. Изменение солевого состава молока
4. Лечение отеков и ацидоза
5. Очистка сточных вод
6. Удаление ионов металлов (Fe3+, Cu2+ и Ca2+), вызывающих помутнение вин
7. Опреснение воды
Хроматография
Хроматография - динамический метод анализа, основанный на многократно повторяющихся процессах адсорбции и десорбции.

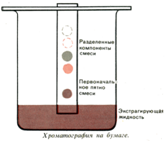 Скорость перемещения отдельных компонентов смеси вдоль неподвижной фазы связана с различным характером взаимодействия в системе: «вещество–подвижная фаза–неподвижная фаза».
Скорость перемещения отдельных компонентов смеси вдоль неподвижной фазы связана с различным характером взаимодействия в системе: «вещество–подвижная фаза–неподвижная фаза».
Адсорбент не должен вступать в химическую реакцию и проявлять свойства катализатора
Вещества распределяются по высоте колонки в зависимости от адсорбционных свойств: плохо адсорбирующиеся вещества
 выходят из колонки первыми.
выходят из колонки первыми.
Виды хроматографии
1. Адсорбционная
Основана на различии в адсорбционных свойствах разделяемых веществ.
Хорошо адсорбирующиеся компоненты перемещаются с низкой скоростью.
а) бумажная
Хроматографическое разделение чернил на компоненты
в водно-метанольной смеси
б) колоночная
в) тонкослойная
Хроматография на пластинке в тонком слое сорбента.
2. Распределительная хроматография
Основана на различной растворимости вещества в неподвижной фазе (жидкость) и в подвижной фазе
(жидкость или газ)
Первыми из колонки выходят плохо растворимые вещества!
3. Молекулярно-ситовая хроматография (гель-фильтрация, гель-хроматография)
В качестве стационарной фазы используют молекулярные сита - пористые гели агарозы, полиакриламида и декстрана (сефадексы).
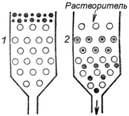 Крупные молекулы, не попадая в поры, перемещаются вдоль стационарной фазы быстрее, чем мелкие.
Крупные молекулы, не попадая в поры, перемещаются вдоль стационарной фазы быстрее, чем мелкие.
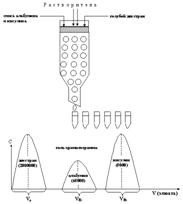 Схема гель-хроматографии:
Схема гель-хроматографии:
1 – на колонку с гелем (сферические светлые частицы)
нанесен исследуемый раствор;
2 – после промывания колонки растворителем.
Схема фракционированияполимеров.
Из гель-хроматограммы видно, что вещества
из колонки выходят в следующем порядке:
1) декстран (Мr=2000000); 2) альбумин (Мr=65000); 3) инсулин (Мr=5000).
4. Афинная хроматография (биоспецифическая)
Основана на специфичности взаимодействия ферментов.
Стационарная фаза содержит либо фермент, либо субстрат.
Иммобилизация -закрепление веществ на твердой поверхности адсорбента-носителя (силикагели, силохромы)
Иммобилизованные ферменты можно многократно применять в проточных системах, и они не теряют активности при длительном хранении (до полугода).
Из анализируемой смеси с высокой степенью специфичности будет «вылавливаться» партнер соответствующей
фермент-субстратной реакции.
Размеры каждого кармана и природа образующих его радикалов определяют тип аминокислотной цепи, которую он удерживает лучше всего.
Иммобилизация уреазы широко применяется при аналитическом определении мочевины и в аппарате «искусственная почка».
Для удаления токсических веществ из биологических жидкостей через адсорбент пропускают:
кровь – гемосорбция (гемоперфузия);
плазму – плазмосорбция (плазмоперфузия);
лимфу – лимфосорбция (лимфоперфузия).
Клиренс - объем крови, полностью очищаемый в данном аппарате за единицу времени при заданной объемной скорости крови или среды.
Принцип афинной хроматографии в сочетании с абсорбцией используется в марлевых повязках
Современные активные медицинские сорбенты можно разделить на четыре группы:
1. Дренирующие сорбенты - обеспечивают отток раневого отделяемого и микрофлоры со дна раны;
2. Биологически активные сорбенты – содержат иммобилизованные в их структуре лекарственные вещества;
3. Избирательные сорбенты - необратимо адсорбируют микрофлору в пористой структуре;
4. Комбинированные сорбенты - это перевязочные средства, содержащие различные по механизму действия сорбенты.
5. Ионообменная хроматография
Разделение вещества связано с различием термодинамических констант ионного обмена определяемых ионов.
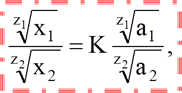 Уравнение Б.П.Никольского:
Уравнение Б.П.Никольского:
где x1 и x2 – количество поглощенных ионов
(мг-экв/г);
a1 и a2 – активности ионов;
z1 и z2 валентности ионов;
K – константа обмена.
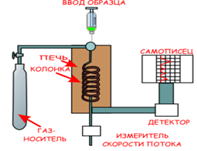 6. Газо-адсорбционная хроматография
6. Газо-адсорбционная хроматография
Степень разделения зависит от:
ü длины колонки;
ü природы адсорбента;
ü природы адсорбтива;
ü температуры.
Типичная запись показаний прибора при хроматографическом разделении газов.
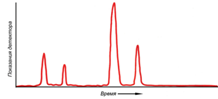
Первыми из колонки выходят газы, которые адсорбируются хуже.
tуд – время удерживания - качественная характеристика;
S - площадь пика - количественная характеристика.
7. Газо-жидкостная хроматография
 На твердый адсорбент наносится тончайший слой растворителя, что позволяет разделять жидкие смеси
На твердый адсорбент наносится тончайший слой растворителя, что позволяет разделять жидкие смеси
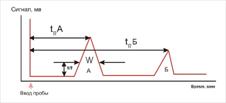
Хроматограмма смеси изомерных ксилолов.
Разделение великолепное:
Пики, соответствующие изомерам, далеко отстоят друг от друга.