АЛЛОТРОПНЫЕ МОДИФИКАЦИИ ФОСФОРА
Фосфор может существовать в виде большого числа аллотропных модификаций, в настоящее время их насчитывается 11, но всё многообразие видов можно свести к трем: белый, красный и черный фосфор.
Наиболее распространен белый, или желтый, фосфор. Белый фосфор имеет молекулярную решетку, в узлах которой находятся тетраэдрические молекулы Р4.
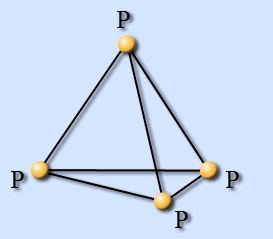
Это очень реакционноспособное, мягкое воскообразное вещество бледно-желтого цвета, с неприятным чесночным запахом, растворимое в сероуглероде и бензоле, нерастворимое в жидкой воде, с водяным паром образует газовую смесь. Очень ядовито. Воспламеняется при трении, обладает уникальной способностью светиться в темноте за счет медленного окисления. Температура плавления 44 °С. В лаборатории его хранят под слоем воды.
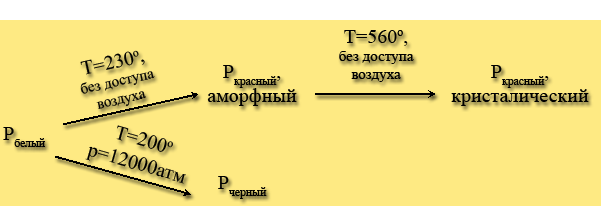
Название красный фосфор относится к нескольким модификациям, различающимся по плотности и окраске: она колеблется от оранжевой до темно-красной и даже фиолетовой. Красный фосфор, образующийся при нагревании белого до 320 °С без доступа воздуха, является рентгеноаморфным, при дальнейшем нагревании до 560 °С переходит в кристаллическое состояние за счет разрыва одной связи Р – Р в тетраэдре Р4 и дальнейшего связывания оставшихся групп в цепи, кольца и трубки. Такая полимеризация приводит к упрочнению связи Р – Р, увеличению плотности и температуры плавления до 600 °С и уменьшению реакционной способности.
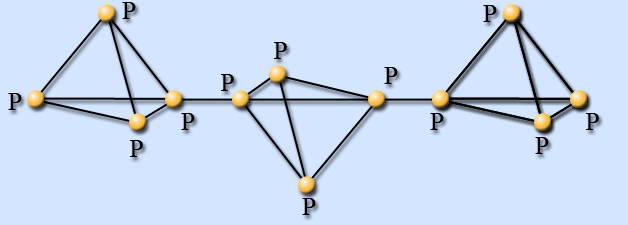
Красный фосфор менее активен, чем белый, нерастворим в воде и сероуглероде, не светится в темноте, абсолютно безвреден.
При повышенном давлении белый фосфор переходит в черный фосфор. Это самая устойчивая модификация фосфора. Кристаллический черный фосфор тоже имеет несколько модификаций. Ромбическая модификация построена из гексагональных колец Р6, упакованных в слои, причем кольца не являются плоскими.
|
|
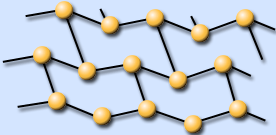
Ромбическая модификация
Существуют также кубическая и гексагональная модификация.
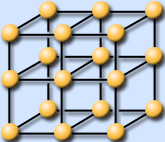
Кубическая модификация
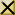
Гексагональная модификация
По внешним признакам черный фосфор напоминает металл, имеет металлический блеск, обладает электропроводностью, теплопроводностью, довольно твердый. Наименее активный из всех модификаций.
Красный и черный фосфор получают из белого фосфора.
Явление аллотропных модификаций у фосфора вызвано образованием различных кристаллических форм.
Белый фосфор (Р4) имеет молекулярную кристаллическую решетку, красный и черный – атомную. Различие в строении кристаллической решетки обуславливает и различие в их физических и химических свойствах. Белый фосфор – сильный яд, даже в малых дозах действует смертельно. В твердом состоянии получается при быстром охлаждении паров фосфора. В чистом виде совершенно бесцветен, прозрачен, по внешнему виду похож на воск: на холоде хрупок, при температуре выше 15 °C – мягкий, легко режется ножом; в воде нерастворим, но хорошо растворяется в сероуглероде – СS2 и в органических растворителях; легко плавится, летуч. Прочность связи в молекуле невелика, чем обусловлена высокая химическая активность. Белый фосфор быстро окисляется на воздухе, при этом светится в темноте – превращение химической энергии в световую; самовоспламеняется на воздухе, при слабом нагревании, незначительном трении. С кислородом реагирует без поджигания, даже под водой, образуя сначала Р2О3, затем P2O5:
|
|
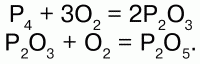
При длительном нагревании белый фосфор превращается в красный. Белый фосфор применяется для изготовления боеприпасов артиллерийских снарядов, авиабомб, предназначенных для образования дымовых завес. Широкого применения не имеет.
Красный фосфор – порошок красно-бурого цвета, неядовит, нелетуч, нерастворим в воде и во многих органических растворителях и сероуглероде; не воспламеняется на воздухе и не светится в темноте. Только при нагревании до 260 °C воспламеняется. При сильном нагревании, без доступа воздуха, не плавясь (минуя жидкое состояние) испаряется – сублимируется. При охлаждении превращается в белый фосфор. Идет на изготовление спичек: красный фосфор в смеси с сульфидом сурьмы, железным суриком, с примесью кварца и клея наносят на поверхность спичечной коробки. Головка спичек состоит в основном из бертолетовой соли, молотого стекла, серы и клея. При трении головки о намазку коробки красный фосфор воспламеняется, поджигает состав головки, а от него загорается дерево. Также красный фосфор применяется в приготовлении фармацевтических препаратов.
Черный фосфор получается при сильном нагревании и при высоком давлении белого фосфора. Черный фосфор тяжелее других модификаций. Применяется очень редко – как полупроводник в составе фосфата галлия и индия в металлургии.