Тепловой баланс процессов горения основан на определении тепла, поглощѐнного продуктами горения.
Уравнение теплового баланса имеет вид:
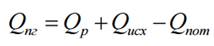
где Qпг -теплота, поглощенная продуктами горения,
Qр - теплота химической реакции,
Qисх - теплота, поступившая из внешних источников,
Qпот - тепловые потери.
Тепловой баланс процесса горения складывается из следующих составляющих:
Приход:
Основная статья приходной части теплового баланса – это теплота горения вещества Qгор.
Вторая составляющая – Qисх – теплота исходных веществ, т.е. теплосодержание горючего и окислителя. Эта величина зависит от агрегатного состояния и химической природы горючего. Например, для метана Qисх < 1 %, а для древесины » 3%.
Расход:
QПГ – теплота, уходящая с продуктами горения. Так как продукты горения создают конвективный поток над пламенем, то QПГ называют также теплотой конвекции или конвективной теплотой. QПГ колеблется в пределах 35 – 95 % от Qгор.
Анализ этого уравнения показывает, что практически единственным источником тепловой энергии любого процесса горения, а значит, и любого пожара, является тепловой эффект химических реакций окисления в пламени, т.е. теплота горения, которая относится к важнейшим характеристикам пожарной опасности веществ и материалов [2, с 26].
Одним из важных параметров термодинамического расчета является адиабатическая температура процесса. Адиабатическая температура связана с реальными параметрами течения взрыва, горения [5, с. 11].
Адиабатическая температура горения - есть средняя температура продуктов стехиометрического полного горения, получаемая из уравнения теплового баланса горючей системы при условии, что вся энергия исходных компонентов преобразована а тепловую энергию продуктов горения.
Существуют различные алгоритмы расчета адиабатической температуры горения, взрыва, но в методологическом плане проблема разработана не полностью. Это обусловлено тем, что проверить расчеты экспериментально не представляется возможным – адиабатический процесс не реализован на практике. Следует выделить основные положения методики расчетов. Основы расчетов базируются на первом законе термодинамике и следствиях из него.
Существует несколько равнозначных определений первого закона термодинамики и одно их них формулируется следующим образом – теплота процесса расходуется на увеличение внутренней энергии и совершении работы системой:
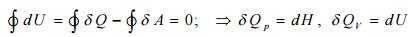
Для расчета адиабатической температуры применяют уравнения Кирхгофа для изобарного и изохорного процесса:
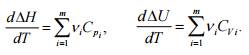
Здесь ΔН, ΔU – изменение энтальпии, внутренней энергии, Дж/моль;
Ср, Сv – соответственно изобарная и изохорная теплоемкости, Дж/моль. град;
v – стехиометрические коэффициенты формальной схемы процесса,
T – температура, К.
Процедура оценки адиабатической температуры горения, взрыва состоит из следующих этапов.
1. Составление формальной схемы процесса.
2. Расчет энтальпии химической реакции
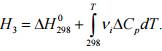
3. Составление системы уравнений с учетом константы равновесия Kp.
4. Расчет адиабатической температуры горения, взрыва:
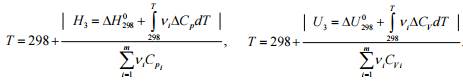
Для удобства расчетов температуры величины энтальпии и внутренней энергии внесены под знак модуля. Таким образом, необходимо правильно записать формальную схему процесса – указать все продукты реакции и исходные вещества. Более того, необходимо указать, как меняется теплоемкость, стехиометрический состав смеси в зависимости от температуры процесса, фазовые переходы. В расчетах энтальпии или внутренней энергии необходимо учитывать алгебраические суммы по теплоемкостям продуктов реакции и исходных веществ.