Водородный показатель
Методические указания к лабораторной работе
Великий Новгород
Водородный показатель: Метод указ. / Сост. Г.Н.Олисова; Н.И.Ульянова4 Е.Н.Телешова / НовГУ им. Ярослава Мудрого, - Великий Новгород, 2017. – 17с.
Рассмотрены теоретические методы расчета и экспериментальные способы определения концентрации водородных ионов в растворах электролитов (рН растворов).
Методические указания предназначены для студентов всех специальностей, изучающих курс химии.
ВВЕДЕНИЕ
Протекание различных химических процессов сильно зависит от реакции среды в растворе. Поэтому величина рН раствора является важнейшим показателем, который необходимо контролировать как при проведении реакций в научно-исследовательских лабораториях, так и в ходе разнообразных технологических процессов.
Настоящая лабораторная работа даёт возможность освоить способы измерения и методы расчёта рН в водных растворах электролитов. Перед её выполнением необходимо усвоить понятия: ионное произведение воды, характер среды, индикатор, гидролиз солей, водородный показатель.
ЦЕЛЬ РАБОТЫ
Изучить методы расчета рН растворов электролитов.
Освоить методы определения рН растворов.
ОСНОВНЫЕ ТЕОРЕТИЧЕСКИЕ ПОЛОЖЕНИЯ
Водородный показатель. Ионное произведение воды
Водородный показатель (рН) величина, характеризующая активность или концентрацию ионов водорода в растворах. Водородный показатель обозначается рН.
Водородный показатель численно равен отрицательному десятичному логарифму активности или концентрации ионов водорода, выраженной в молях на литр:

В воде концентрация ионов водорода определяется электролитической диссоциацией воды по уравнению

Константа диссоциации при 22° С составляет
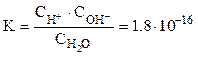
Пренебрегая незначительной долей распавшихся молекул, можно концентрацию недиссоциированной части воды принять равной обшей концентрации воды, которая составляет: СH2O =1000/18=55,55моль/л.
Тогда: 
Для воды и ее растворов произведение концентраций ионов Н+ и ОН- величина постоянная при данной температуре. Она называется ионным произведением воды  и при 25° С составляет
и при 25° С составляет  .
.
Постоянство ионного произведения воды дает возможность вычислить концентрацию ионов  если известна концентрация ионов ОН
если известна концентрация ионов ОН 
и наоборот:
 .
.
Понятия кислая, нейтральная и щелочная среда приобретают количественный смысл.
В случае, если  ,эти концентрации (каждая из них) равны
,эти концентрации (каждая из них) равны  моль/л, т.е
моль/л, т.е  моль/л и среда нейтральная, в этих растворах
моль/л и среда нейтральная, в этих растворах
 и рОН=-lg[ OH-]
и рОН=-lg[ OH-]
Если  >10
>10  моль/л, [OH-]<10
моль/л, [OH-]<10  моль/л - среда кислая; рН<7.
моль/л - среда кислая; рН<7.
Если  <10
<10  моль/л, [OH-]>10
моль/л, [OH-]>10  моль/л - среда щелочная; рН>7.
моль/л - среда щелочная; рН>7.
В любом водном растворе рН + рОН =14, где 
Величина рН имеет большое значение для биохимических процессов, для различных производственных процессов, при изучении свойств природных вод и возможности их применения и т.д.
2.2 Вычисление рН растворов кислот и оснований
Для вычисления рН растворов кислот и оснований следует предварительно вычислить молярную концентрацию свободных ионов водорода ( ) или свободных гидроксил ионов (
) или свободных гидроксил ионов ( ), а затем воспользоваться
), а затем воспользоваться
формулами:
 ; рОН-=-lg[ OH-]; рН + рОН =14
; рОН-=-lg[ OH-]; рН + рОН =14
Концентрация любого иона в моль/л в растворе электролита можно вычислить по уравнению

где См иона – молярная концентрация иона в моль/л;
См – молярная концентрация электролита в моль/л;
 -степень диссоциации электролита;
-степень диссоциации электролита;
n - количество ионов данного вида, которое получается при распаде одной молекулы электролита.
Если электролит слабый, то значение степени диссоциации может быть определено на основании закона разбавления Оствальда:
 ; тогда
; тогда  = √ СмКдис
= √ СмКдис
Пример 1. Вычислить рН 0,001H раствора гидроксида натрия.
Решение: гидроксид натрия является сильным электролитом, диссоциация в водном растворе происходит по схеме:

Степень диссоциации в разбавленном растворе можно принять равной 1. Концентрация ионов ОН  (моль/л) в растворе равна:
(моль/л) в растворе равна:
 |
Пример 2. Вычислить рН 1%-ного раствора муравьиной кислоты, считая, что плотность раствора равна 1г/мл; Кдисс = 
Решение: 1л раствора содержит 10г НСООН, что составляет 10/46= =0,22моль, где 4б г/моль - молярная масса муравьиной кислоты. Следовательно, молярная концентрация раствора равна 0,22моль/л. Муравьиная кислота – слабый электролит, поэтому
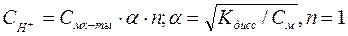 , так как
, так как
 ,
,

Пример 3. рН раствора составляет 4,3. Вычислить  и
и 
Решение:
[Н+] = 10-рН =10-4,3 = 5∙10-5моль/л
 моль/л.
моль/л.