ОК – 38
Законы (начала) термодинамики
Закон сохранения энергии: энергия в природе не возникает из ничего и не исчезает, а переходит от одного тела к другому и превращается из одного вида в другой.
| Q = ΔU + A' или ΔU = Q + A | Первый закон термодинамики:количество теплоты, переданное системе, идет на изменение ее внутренней энергии и на совершение системой работы над внешними телами. или Первый закон термодинамики:изменение внутренней энергии системы при переходе из одного состояния в другое равно сумме работы внешних сил и количества теплоты, переданного системе. |
1842 г.- Р. Майер сформулировал I закон термодинамики, то есть закон сохранения энергии примени-тельно к тепловым процессам, 1843 г. – экспериментально подтвердил Д. Джоуль.
Применение первого закона термодинамики
| изменение состояния | I закон терм-ки | физ. смысл I з. т. | р – V диаграмма |
| Изобарный процесс р = const Δр = 0 | Q = ΔU + A' | Расширение: подводимое к газу теп-ло идет на увеличение его внутрен-ней энергии и на совершение газом работы Сжатие: внутренняя энергия умень-шается за счет того, что над газом совершается работа, он отдает тепло окружающей среде | 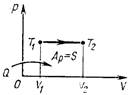
|
| Изохорный процесс V = const ΔV = 0 A' = 0 | Q = ΔU | Нагревание: внутренняя энергия газа увеличивается за счет подводимого тепла Сжатие: внутренняя энергия умень-шается за счет того, что газ передает тепло окружающей среде | 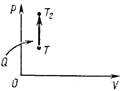
|
| Изотермический процесс Т = const ΔТ = 0 ΔU = 0 | Q = A' | Расширение: все переданное газу тепло идет на совершение работы Сжатие: при совершении работы внешними силами газ отдает тепло |  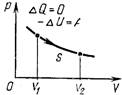
|
| Адиабатный процесс(без теплообмена с окружающей средой) Q = const | ΔU = - A' | Расширение: внутренняя энергия га-за уменьшается за счет того, что газ совершает работу без охлаждения Сжатие: работа внешних сил идет на увеличение внутренней энергии газа. Газ нагревается | 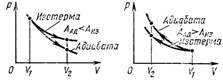
|
Адиабатный процесс:
Дизельный двигатель: воспламенение горючего при адиабатном сжатии.
Образование облаков.
Кондиционер, холодильник: расширение.
Процессы в природе:
1) необратимые: диффузия, жизнь человека, Емех→ U (процессы только в одном направлении)
2) обратимые: смена дня и ночи, движение планет, движение молекул
Второй закон термодинамики: невозможен процесс, при котором теплота переходила бы самопроиз-вольно от тел более холодных к телам более нагретым (принцип Клаузиуса).
Второй закон термодинамики: невозможен процесс, единственным результатом которого является превращение теплоты в эквивалентную ей работу (принцип Кельвина).
Принцип Кельвина эквивалентен утверждению о невозможности вечного двигателя.
Третий закон термодинамики: абсолютный нуль температуры недостижим (теорема Нернста).
Общий постулат термодинамики: каково бы не было начальное состояние тел изолированной системы, в ней в конце концов установится термодинамическое равновесие, в котором прекратятся все макроскопичес-кие процессы.
Нулевой постулат термодинамики: пусть имеются три тела А, В, С. Если при контакте тела С с телом А не происходит теплообмена и при контакте тела С с телом В тоже не происходит теплообмена, то не будет теплообмена и при контакте тел А и В.