Разнообразные механизмы процессинга РНК в клетках были уже рассмотрены выше. Как оказалось, созревание мРНК играет важную роль и в регуляции экспрессии тех генов, транскриптами которых эти РНК являются. Одними из первых доказательства такого рода регуляции экспрессии генов были получены для морских ежей. Транскрипты, обнаруживаемые в цитоплазме клеток на стадии бластулы, можно видеть с помощью специфических ДНК-зондов в ядрах клеток кишечника. В ядрах клеток бластулы и дифференцированных клеток кишечника морских ежей синтезируются похожие наборы РНК, однако наборы цитоплазматических РНК, участвующих в трансляции, у этих типов клеток сильно различаются вследствие разного процессинга предшественников мРНК в ядрах.
Убедительные данные о контроле экспрессии генов на уровне процессинга РНК получены в экспериментах с вирусами клеток животных. Вирусы полиомы и SV40 не способны размножаться в недифференцированных стволовых клетках тератокарциномы. Однако, если стволовые клетки дифференцируются в клетки соматических типов, они становятся пермиссивными (чувствительными) к этим вирусам. Одной из причин исходной непермиссивности стволовых клеток к указанным вирусам является их неспособность осуществлять процессинг (сплайсинг) вирусных РНК в ядрах. Это сопровождается накоплением в ядрах стволовых клеток гигантских предшественников вирусных РНК, которые в конце концов разрушаются. Данные такого рода в совокупности свидетельствуют о зависимости развития соматических клеток от образования в них специфических ферментов сплайсинга, которые отвечают за процессинг предшественников клеточных мРНК, необходимых для функционирования и дифференцировки соматических клеток.
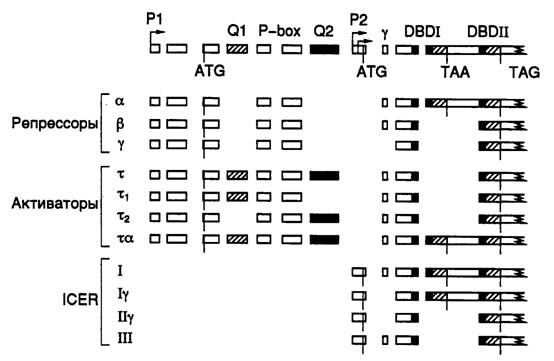
Рис. I.35. Схема формирования активаторов и репрессоров транскрипции, кодируемых геном CREM и образующихся в результате альтернативного сплайсинга
В верхней части рисунка изображена схема гена CREM, включающая альтернативные промоторы Р1 и P2, кодоны альтернативной инициации и терминации трансляции, а также экзоны, кодирующие различные домены факторов. Внизу представлены комбинации последовательностей экзонов, объединяющихся в зрелые мРНК, которые кодируют разных представителей групп репрессоров и активаторов транскрипции, а также ICER-белков
Альтернативный сплайсинг. Одним из примеров посттранскрипционных модификаций РНК, имеющих большое значение в регуляции экспрессии генов эукариот, является альтернативный сплайсинг. Сущность его заключается в том, что в результате посттранскрипционного процессинга предшественника мРНК, из которого в результате сплайсинга вырезаются некодирующие последовательности нуклеотидов, соответствующие интронам транскрибированного гена, образуются зрелые мРНК, различающиеся по своей первичной структуре. В результате в разных клетках и тканях из одного и того же предшественника получаются молекулы зрелых мРНК, которые объединяют в различных комбинациях последовательности экзонов транскрибированного гена.
На рис. I.35 представлена схема экзонной структуры гена модулятора cAMP-респонсивного элемента человека (CREM), кодирующего целое семейство позитивно и негативно действующих изоформ фактора транскрипции, связывающихся с cAMP-респонсивными регуляторными элементами ДНК – CRE. Данное семейство факторов вовлечено в регуляцию экспрессии генов, участвующих в обеспечении эндокринных функций организма и сперматогенезе. Ген построен из функциональных модулей, заключающих в себе информацию двух промоторов, двух альтернативных ДНК-связывающих доменов, а также нескольких транс- действующих доменов этих факторов. Пре-мРНК транскрибируется с неиндуцируемого промотора P1 и подвергается альтернативному сплайсингу, специфичность которого определяется типом ткани, в которой он происходит. Например, во время сперматогенеза происходит переключение с синтеза репрессоров транскрипции CREMa, CREMb и CREMg на образование CREMt, который содержит в своей полипептидной цепи две дополнительные последовательности, обогащенные Gln (Q1 и Q2), необходимые для транс -активации транскрипции. Более короткий транскрипт, синтез которого инициируется на промоторе P2, процессируется с образованием зрелых мРНК, которые кодируют группу небольших молекул репрессоров (ICER). Инициация синтеза РНК на промоторе P2 активируется под действием ритмических гормональных сигналов эпифиза мозга.
Рассмотренный пример показывает важную роль альтернативного сплайсинга в расширении кодирующего потенциала генов эукариот, поскольку в результате использования такого механизма одна и та же последовательность нуклеотидов гена может кодировать несколько разных белков.
Комбинаторика объединения последовательностей нуклеотидов пре-мРНК в процессе альтернативного сплайсинга может быть очень сложной, поскольку в него вовлекаются интроны и экзоны, а их объединение происходит с использованием различных точек сплайсинга, локализованных в этих последовательностях. Распознавание участков ДНК, в которых находятся точки сплайсинга, участвующие в конкретном акте посттранскрипционного процессинга пре-мРНК, происходит с участием специфических белков в результате белково-нуклеинового взаимодействия.
Альтернативный сплайсинг у дрозофилы. Механизм регуляции альтернативного сплайсинга хорошо изучен у дрозофилы, использующей этот процесс, в частности при генетическом определении пола (рис. I.36). Каскад реакций альтернативного сплайсинга в данном случае начинается с альтернативного выбора в пре-мРНК гена sxl последовательности экзона 3, содержащей кодон терминации трансляции. Если в результате альтернативного сплайсинга последовательность нуклеотидов, кодируемая экзоном 3, включается в зрелую мРНК самок, то при ее трансляции рибосомами образуется укороченная полипептидная цепь белка SXL, у которой отсутствует биологическая активность. Напротив, удаление такой последовательности в результате альтернативного сплайсинга приводит к образованию функционально активного белка, который, в свою очередь, участвует в регуляции альтернативного сплайсинга пре-мРНК гена tra, предотвращая взаимодействие мяРНК U2AF65 с одним из 3’-концевых сайтов сплайсинга. Это обеспечивает соединение белка с другим менее эффективным сайтом сплайсинга, расположенным ниже первого, участвующего в определении пола.
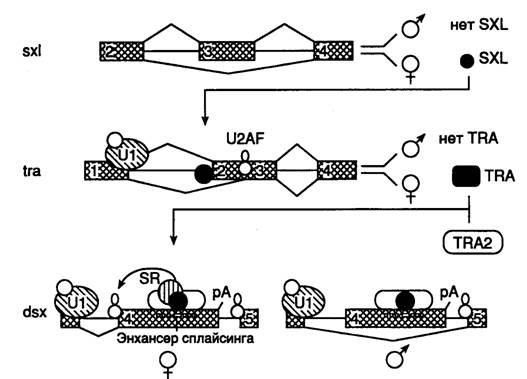
Рис. I.36. Схема каскада реакций альтернативного сплайсинга, приводящих к определению пола у дрозофилы
Белок TRA стабилизирует связывание белка TRA2 с энхансером сплайсинга в tra-пре-мРНК. 1–5 – экзоны
Образующийся в результате белок TRA, содержащий аминокислотную последовательность, кодируемую экзоном 3 гена tra, в комплексе с другими белками TRA2 и SR-белком участвует в образовании мультипротеинового комплекса на специфической последовательности альтернативного экзона в мРНК гена dsx. Подобные регуляторные последовательности обнаружены также в мРНК позвоночных и вирусов животных и получили название энхансеров сплайсинга (они не имеют отношения к энхансерам, регулирующим транскрипцию эукариотических генов). В случае dsx -пре-мРНК образование такого энхансерного комплекса, включающего и белковые факторы, узнающие 3’-концевые сайты сплайсинга, способствует взаимодействию факторов сплайсинга с его низкоэффективным 3’-концевым сайтом, расположенным перед энхансером (и последовательностью экзона 4), а также вырезанию этого интрона. Образующийся в результате трансляции такой мРНК белок DSX блокирует экспрессию генов, обеспечивающих формирование у мух мужского фенотипа. В отсутствие TRA-белка в результате объединения экзонов 3 и 5 получается альтернативный белок DSX, который не препятствует экспрессии этих генов и подавляет дифференцировку самок.
Позитивная и негативная регуляция альтернативного сплайсинга в клетках животных. У животных описано много генов, пре-мРНК которых подвергаются альтернативному сплайсингу. Однако механизмы регуляции этого процесса не так ясны, как в только что рассмотренном примере с генами дрозофилы. Основную роль в выборе альтернативных сайтов сплайсинга у животных, по-видимому, играют общие факторы сплайсинга. В частности, установлено, что простое повышение концентрации SR-белков способствует предпочтительному выбору для сплайсинга проксимально расположенных, т.е. сближенных друг с другом, сайтов сплайсинга во многих пре-мРНК.
Механизм этого явления представлен на рис. I.37 на примере гипотетической пре-мРНК, содержащей два альтернативных одинаково эффективных 5’-концевых сайта сплайсинга. Для простоты показано связывание с РНК только U1-мяРНП и SR-белка. В условиях недостатка U1-мяРНП (см. рис. I.37,а) не все 5’-концевые сайты сплайсинга заполнены мультибелковыми комплексами. Поскольку наиболее эффективно в альтернативном сплайсинге используется внутренний сайт, максимально сближенный со своим 3’-концевым партнером, альтернативный 5’-концевой сайт вовлекается только в том случае, если ниже расположенный сайт не занят. Повышение концентрации U1-мяРНП приводит к тому, что оба 5’-концевых сайта сплайсинга взаимодействуют с белковыми комплексами и сплайсинг происходит преимущественно с участием его максимально сближенных сайтов (см. рис. I.37,б). В этом случае SR-белки усиливают взаимодействие между расположенными по соседству U1-мяРНП-комплексами.
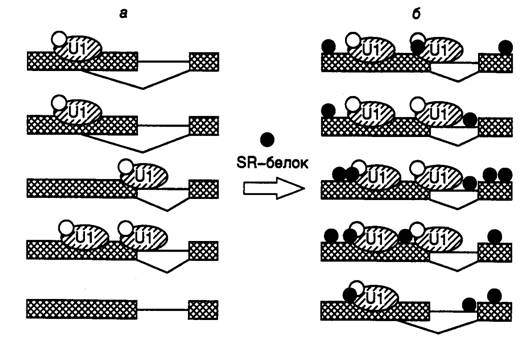
Рис. I.37. Механизм действия белков SR при обеспечении выбора сплайсомой альтернативных сайтов сплайсинга
U1 - U1-мяРНП. Эффективность вырезания интронов: а – 40% проксимальных, 40% дистальных; б – 80% проксимальных, 20% дистальных
У многих генов животных и их вирусов обнаружены последовательности нуклеотидов, блокирующие сплайсинг. Некоторые из этих последовательностей способствуют формированию в пре-мРНК характерной вторичной структуры, которая маскирует сайты сплайсинга. Поскольку многие белковые факторы сплайсинга обладают ДНК-расплетающей активностью и вызывают локальное плавление спирализованных участков РНК, то дифференциальная экспрессия таких факторов оказывает влияние на выбор белками сплайсинга определенных сайтов. Другие негативные регуляторные элементы альтернативного сплайсинга требуют для своего функционирования наличия транс- действующих факторов. Например, белок вируса иммунодефицита человека взаимодействует с последовательностью RRE пре-мРНК и, блокируя ее сплайсинг, обеспечивает экспорт непроцессированной пре-мРНК. Описаны экзоны, также оказывающие негативное влияние на сплайсинг. Кроме того, показано, что белки гетерогенных ядерных РНП A1, A1b, A2 и B1 выступают антагонистами SR-белков при взаимодействии последних с дистальными 5’-концевыми сайтами сплайсинга. Для индивидуальных белков этой группы (A и B) характерна субстратная специфичность, и они оказывают существенное влияние на выбор конкретных сайтов сплайсинга во время процессинга пре-мРНК, что в ряде случаев обеспечивается наличием высокоаффинных сайтов связывания для таких белков между конкурирующими 5’-концевыми сайтами сплайсинга. Например, наличие участка сильного связывания для белка А1, входящего в состав гяРНП, между двумя 5’-концевыми сайтами сплайсинга приводит к преимущественному участию в процессинге дистального сайта сплайсинга (более удаленного от 3’-концевого сайта). Такое взаимодействие не оказывает влияния на связывание обоими 5’-концевыми сайтами сплайсинга U1-мяРНП.
Рассмотренные механизмы позитивной и негативной регуляции альтернативного сплайсинга во многом гипотетичны. Однако существование внутриклеточных механизмов, с высокой точностью регулирующих этот процесс, в настоящее время доказано. Такая специфичность может достигаться за счет контролируемых изменений внутриядерной концентрации индивидуальных SR-белков и белков гетерогенных ядерных РНП-частиц, функционирующих в сочетании с регуляторными последовательностями нуклеотидов (энхансерами сплайсинга) и с сайтами сплайсинга определенной эффективности, локализованными в самих пре-мРНК. В некоторых случаях подобная регуляция требует участия дополнительных специфических факторов.
Переключение классов иммуноглобулинов. В процессе дифференцировки B-лимфоцитов происходит смена классов иммуноглобулинов, синтезируемых этими клетками. В начале дифференцировки образуются иммуноглобулины, обладающие способностью как секретироваться в окружающую среду, так и интегрироваться в плазматическую мембрану B-лимфоцитов. Поверхностные иммуноглобулины выполняют здесь роль рецепторов антигенов и принадлежат к одному из двух классов белков: IgM или IgD. Белки этих двух классов обладают одинаковыми аминокислотными последовательностями в N-концевых частях, взаимодействующих с антигенными детерминантами, и различаются по С-концам. В начале процесса дифференцировки поверхностные иммуноглобулины представлены белками только класса IgM, а после первой стимуляции антигеном появляются белки обоих классов; далее, после завершения дифференцировки B-лимфоцитов, на поверхности клеток остаются иммуноглобулины только класса IgD. Именно они продолжают синтезироваться зрелыми B-лимфоцитами.
В основе феномена переключения классов иммуноглобулинов у B-лимфоцитов лежит механизм альтернативного сплайсинга. На любой стадии дифференцировки B-лимфоцитов синтезируются транскрипты генов иммуноглобулинов, в состав которых входят экзоны вариабельных частей иммуноглобулинов, а также их константных частей, как m, так и d, определяющих класс иммуноглобулинов (IgM или IgD соответственно). В результате альтернативного сплайсинга с последовательностями экзонов вариабельных частей в зрелой мРНК соединяются последовательности экзонов m или d, что и определяет, в конечном счете, класс иммуноглобулинов, образующихся в результате трансляции этих мРНК рибосомами. С помощью альтернативного сплайсинга B-лимфоциты решают вопрос и о том, какая из форм IgM – секретируемая или интегрирующаяся в мембраны – образуется в клетках. Так же как и в случае обсуждавшихся выше классов иммуноглобулинов, секретируемая и ассоциированная с мембранами формы IgM различаются по С-концевым аминокислотным последовательностям. Последовательности, кодирующие эти С-концевые домены иммуноглобулинов, добавляются в зрелые мРНК или удаляются из их предшественников в результате альтернативного сплайсинга.
Исследования последних лет показали, что регуляция экспрессии генов с помощью альтернативного сплайсинга широко распространена в клетках высших организмов. Использование такого изящного механизма позволяет одному и тому же гену кодировать несколько полипептидов, различающихся по своим биологическим функциям, и контролировать их биосинтез во времени (на разных этапах дифференцировки клеток) и в пространстве (в различных органах и тканях). Все это повышает информационную емкость генома высших организмов без существенного увеличения его размеров.
Транс -сплайсинг. Из рассмотренных выше примеров следует, что во время постоянного или альтернативного сплайсинга интроны удаляются из предшественников мРНК в результате нескольких сложных реакций при участии крупного РНП-комплекса, называемого сплайсомой. Обычно 5’- и 3’-концевые сайты сплайсинга, участвующие в таком процессе, расположены на одной молекуле пре-мРНК, т.е. в цис -положении по отношению друг к другу. В отличие от этого в процессе транс -сплайсинга сплайсома выбирает для объединения 5’-сайт и 3’-сайт сплайсинга, которые располагаются на разных молекулах РНК. В настоящее время транс -сплайсинг обнаружен у простейших (трипаносом), евглен, круглых нематод и плоских червей, а также в митохондриях, хлоропластах и безрибосомных пластидах высших растений. Наиболее хорошо изучен механизм транс -сплайсинга у нематоды Caenorhabditis elegans, который подробнее будет рассмотрен ниже. Только у этих групп организмов (за исключением трипаносом, гены которых не содержат интронов) механизмы цис - и транс -сплайсинга функционируют в клетках на одних и тех же молекулах РНК.
Интересной особенностью транскрипции у нематод, сближающих их с трипаносомами, является то, что их РНК синтезируются в виде полицистронных предшественников, которые далее расщепляются до моноцистронных единиц, полиаденилируются и подвергаются транс -сплайсингу. Однако в отличие от трипаносом, у которых транс -сплайсинг ограничивается присоединением к акцепторному 3’-концевому сайту сплайсинга одной и той же лидерной РНК SL1 (spliced leader 1), нематоды обладают еще одним донорным сайтом сплайсинга, ассоциированным с SL2-РНК, молекулы которой присоединяются к внутренним сайтам полицистронных транскриптов. Таким образом, в клетках C. elegans сплайсинг осуществляется по трем механизмам (рис. I.38). Это обычный цис - и транс -сплайсинг, в результате которых SL1-РНК присоединяется вблизи 5’-концов первичных транскриптов-предшественников зрелых мРНК, и, наконец, транс -сплайсинг с участием молекул SL2-РНК, которые объединяются с внутренними последовательностями нуклеотидов полицистронных транскриптов. Все три типа сплайсинга проходят в основном с участием одних и тех же компонентов РНП-комплекса, представляющего собой сплайсому, которая использует одни и те же 3’- и 5’-концевые канонические последовательности сайтов сплайсинга. Подобно высшим организмам в состав сплайсомы нематод входят U1-U6-мяРНК, из которых U2-U6 участвуют в транс- сплайсинге. Молекулы SL-РНК, содержащие донорные сайты сплайсинга, также входят в состав РНП-комплекса.
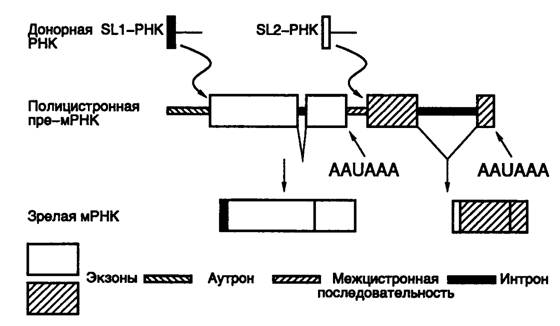
Рис. I.38. Цис- и транс- сплайсинг ядерной полицистронной пре-мРНК у нематоды C. elegans
AAUAAA – сайты полиаденилирования
Последовательности нуклеотидов сайтов транс - и цис -сплайсинга идентичны и взаимозаменяемы в генно-инженерных экспериментах. Интроноподобные последовательности, расположенные на 5’-концах транскриптов, названные аутронами, подвергаются транс- сплайсингу, тогда как внутренние интроны вырезаются по механизму цис -сплайсинга. Единственным отличием гена, транскрипт которого подвергается транс- сплайсингу, является наличие на его 5’-конце последовательности аутрона, а не экзона. При перемещении интрона одного гена из внутреннего положения на 5’-конец другого или того же самого гена он начинает функционировать в качестве аутрона, т.е. подвергается транс- сплайсингу. Если размер такого аутрона превышает 50 п.о., то он нормально функционирует в транс- сплайсинге. При искусственном введении 5’-концевого сайта сплайсинга в аутрон на расстояние более 50 п.о. от его сайта транс- сплайсинга заключенная между этими сайтами последовательность нуклеотидов в РНК подвергается обычному цис- сплайсингу. Таким образом, единственным сигналом, разрешающим транс- сплайсинг, является положение последовательности нуклеотидов вблизи 5’-конца пре-мРНК.
Зрелые, полностью процессированные РНК C. elegans содержат SL1- и SL2-РНК на 5’-концах, причем соблюдаются пропорции в содержании маркированных таким способом РНК внутри клеток. Следовательно, процесс транс- сплайсинга, в результате которого происходит выбор лидерной SL-РНК, каким-то образом регулируется. Предполагается, что белки, взаимодействующие с сайтами полиаденилирования соответствующих РНК, специфически взаимодействуют с белками мяРНП, в состав которых входят SL-РНК, и тем самым осуществляют их выбор.
Функциональная роль транс- сплайсинга в жизненном цикле нематод неизвестна. Экспериментами in vivo продемонстрирована взаимозаменяемость генов, продукты которых подвергаются цис- или транс- сплайсингу. Известно, что сайты транс- сплайсинга часто располагаются непосредственно перед инициирующими AUG-кодонами мРНК. Это позволяет предположить, что SL-последовательности играют определенную роль в инициации трансляции. В частности, с помощью транс- сплайсинга могут удаляться лишние AUG-кодоны, находящиеся не в одной рамке считывания с основной кодирующей последовательностью нуклеотидов мРНК, или создаваться контексты нуклеотидов, которые обеспечивают эффективную инициацию синтеза белка рибосомами. Это, в свою очередь, может допускать определенную эволюционную гибкость в расположении соответствующих промоторов и создавать условия для возникновения новых сайтов инициации транскрипции на ДНК нематод.