Методы исследования лекарственных веществ подразделяются на физические, химические, физико-химические, биологические. Физические методы анализа предусматривают изучение физических свойств вещества, не прибегая к химическим реакциям. К ним относятся: определение растворимости, прозрачности или степени мутности, цветности; определение плотности (для жидких веществ), влажности, температуры плавления, затвердевания, кипения. Химические методы исследования основаны на химических реакциях. К ним относятся: определение зольности, реакции среды (рН), характерных числовых показателей масел и жиров (кислотное число, йодное число, число омыления и т. д.). Для целей идентификации лекарственных веществ используют только такие реакции, которые сопровождаются наглядным внешним эффектом, например изменением окраски раствора, выделением газов, выпадением или растворением осадков и т. п. К химическим методам исследования относятся также весовые и объемные методы количественного анализа, принятые в аналитической химии (метод нейтрализации, осаждения, редокс-методы и др.). В последние годы в фармацевтический анализ вошли такие химические методы исследования, как титрование в неводных средах, комплексометрия. Качественный и количественный анализ органических лекарственных веществ, как правило, проводят по характеру функциональных групп в их молекулах. С помощью физико-химических методов изучают физические явления, которые происходят в результате химических реакций. Например, в
колориметрическом методе измеряют интенсивность окраски в зависимости от концентрации вещества, в кондуктометрическом анализе — измерение электропроводности растворов и т. д. К физико-химическим методам относятся: оптические (рефрактометрия, поляриметрия, эмиссионный и флюоресцентный методы анализа, фотометрия, включающая фотоколориметрию и спектрофотометрию, нефелометрия, турбодиметрия), электро - химические (потенциометрический и полярографический методы), хроматографические методы.
Препараты
Rp: Sol. Natrii chloridi 0,9% - 100ml
D.S. для инъекций
Rp: Sol. Natrii chloridi 10% - 100ml
D.S. наружно
Протокол результатов анализа лекарственного препарата натрия хлорида Natrii chloride. Мм 58,44. Структурная формула Na Cl
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| 0,9 % р-р NaCl | Прозрачная жидкость | бесцветная | отсутствует | солоноватый |
2. Подлинность
| ЛП | реагент |  химизм химизм
| Данные исследования |
| 0,9 % р-р NaCl | На Cl- c AgNO3 |  HCl + AgNO3 AgCl + HNO3 HCl + AgNO3 AgCl + HNO3
 AgCl + NH4OH [Ag(NH3)2]Cl AgCl + NH4OH [Ag(NH3)2]Cl
| Белый творожистый осадок растворим в NH4OH |
| На N+ пламя | Пламя желтого цвета | ||
 С пикриновой кислотой С пикриновой кислотой
| 
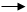 +NaCl + HCl +NaCl + HCl
| Образование пикратов желтого цвета |
3. Количественное определение
| методика | Химизм | ||||
| 01 ml NaCl 3 кап K2CrO4 Тит. 0,1 AgNO3 | 
  AgNO3 + NaCl AgCl + NaNO3 AgNO3 + NaCl AgCl + NaNO3
|
Rp: Ac. hydrochloriсi 1% - 100ml
Pepsini 2,0
D.S. для инъекций
Протокол результатов анализа лекарственного препарата кислоты хлористоводородной Ac. hydrochloriсi Мм 36,46. Структурная формула НCl
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| Микстура с НCl | Прозрачная жидкость | прозрачный | своеобразный | кислый |
2. Подлинность
| ЛП | реагент |  химизм химизм
| Данные исследования |
| Микстура с НCl | AgNO3 |  HCl + AgNO3 AgCl + HNO3 HCl + AgNO3 AgCl + HNO3
 AgCl + 2NH4OH [Ag(NH3)2 Сl]+2Н2О AgCl + 2NH4OH [Ag(NH3)2 Сl]+2Н2О
| Белый творожистый осадок |
3. Чистота
| испытание | реагент | химизм | Данные исследования |
| прозрачность | Раствор прозрачный, красного окрашивания нет | ||
| примеси | КСNS |  Fe3+ + 3 КСNS Fe(СNS)3 + 3K+ Fe3+ + 3 КСNS Fe(СNS)3 + 3K+
|
4. Количественное определение
| Что делали | Химизм |
| 1 ml НCl Inf м/ор NaOH |  HCl + NaOH NaCl + Н2О
оранжево-розовый HCl + NaOH NaCl + Н2О
оранжево-розовый
|
Протокол результатов анализа лекарственного препарата раствор натрия бромида Natrii bromide. Мм 102,90. Структурная формула NaBr
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| р-р NaBr | Прозрачная жидкость | прозрачный | отсутствует | соленый |
2. Подлинность
| ЛП | реагент | химизм | Данные исследования |
| р-р NaBr на Na+ | 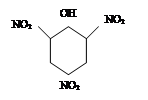 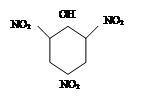 пикриновая кислота
пикриновая кислота
|

 + Na+ + Н+ + Na+ + Н+

| Пикраты желтого цвета |
| на Br- | AgNO3 |  Br- + AgNO3 Ag Br + NO3 Br- + AgNO3 Ag Br + NO3
| Слегка желтоватый осадок |
3. Чистота
| испытание | реагент | химизм | Данные исследования |
| на Ва2+ на Са2+ | Н2SO4 |  2 NaBr + H2SO4 Na2SO4 + 2HBr 2 NaBr + H2SO4 Na2SO4 + 2HBr
   Ba2+ + H2SO4 BaSO4 =
Нет белого осадка Ba2+ + H2SO4 BaSO4 =
Нет белого осадка
| Помутнения раствора нет |
Протокол результатов анализа лекарственного препарата перекиси водорода, Hydrogeniumperoxidi 3% - 100,0 Мм 364,01. Структурная формула Н2O2
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| Н2O2 | Прозрачная жидкость | прозрачный | Своеобразный или без запаха | Жгучий, вяжущий |
2. Подлинность
| ЛП | реагент | химизм | Данные исследования |
| Окислительно-восстановительные свойства H2O2 | KI H2SO4 крахмал |  H2O2 + 2KI + H2SO4 I2 +2H2O + K2SO4 H2O2 + 2KI + H2SO4 I2 +2H2O + K2SO4
| Взвесь фиолетового цвета |
| Восстановительные свойства H2O2 | KMnO4
 H2SO4 H2SO4
|   5 H2O2 + 2KMnO4 + 3H2SO4
2MnSO4 + 5O2 + K2SO4 + 8H2O 5 H2O2 + 2KMnO4 + 3H2SO4
2MnSO4 + 5O2 + K2SO4 + 8H2O
| Раствор обесцвечивается |
4. Количественное определение
| Методика | Химизм |
| Метод рефрактометрии | Смотрим по нижней шкале |
| Метод перманганатаметрии | 0,01Н
 5 H2O2 + 2KMnO4 + H2O
Розовое окрашивание 5 H2O2 + 2KMnO4 + H2O
Розовое окрашивание
|
Протокол результатов анализа лекарственного препарата Natrii hydrocarbonatis Мм 84,01. Структурная формула NaHCO3
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| 5% NaHCO3 | прозрачная жидкость | прозрачный | отсутствует | Солено-щелочной |
2. Подлинность
| ЛП | реагент | химизм | Данные исследования |
| Na+ | пламя | Пламя окрашивается в желтый цвет | |
| HCO3 | НCl |   NaHCO3+НCl NaCl+CO2 +H2O NaHCO3+НCl NaCl+CO2 +H2O
|  выделяется CO2 выделяется CO2
|
| MgSO4 |    2NaHCO3 +MgSO4 Na2SO4 +
+ Mg(OH)2 + CO2 2NaHCO3 +MgSO4 Na2SO4 +
+ Mg(OH)2 + CO2
|  Белый Белый
|
3. Чистота
| испытание | реагент | химизм | Данные исследования |
| Соли аммония | р-в Несслера |      Hg Hg
   2К2HgI4 + 3KOH NH4OH O NH4 I 2К2HgI4 + 3KOH NH4OH O NH4 I
 Hg
+ 3H2O + IKI Hg
+ 3H2O + IKI
| Желтого окрашивания нет |
4. Количественное определение
| Что делали | Химизм |
| 0,5 ml р-ра Inf м/ор 0,1 н НСl |    NaНСO3 + HCl м/ор NaCl + Н2SО3
H2O CO2 NaНСO3 + HCl м/ор NaCl + Н2SО3
H2O CO2
|
Протокол результатов анализа лекарственного препарата Zinci sulgas 0,25% - 10 ml.
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| 0,25% ZnSO4 | прозрачная жидкость | бесцветный | отсутствует | отсутствует |
2. Подлинность
| ЛП | реагент | химизм |  Данные исследования Данные исследования
|
| На SO42- | BaCl2 |  SO42+ + BaCl2 BaSO4
белый SO42+ + BaCl2 BaSO4
белый
| Белый |
| Zn2+ | K4 [Fe(CN)6] |    Zn2++K4 [Fe(CN)6] K2Zn [Fe(CN)6] Zn2++K4 [Fe(CN)6] K2Zn [Fe(CN)6]  + K2SO4 + K2SO4
|  Желтый крист. Желтый крист.
|
| Ca(NO3)2 |  Zn2+ + Ca(NO3)2 CaZnO2 + NO2 Zn2+ + Ca(NO3)2 CaZnO2 + NO2
| Зелень Ринмана |
3. Чистота
| испытание | реагент | химизм | Данные исследования | ||||||||
| Тяж. Ме | Na2S |    Pb2+ + Na2S PbS + 2Na+ Pb2+ + Na2S PbS + 2Na+
|  Черного нет Черного нет
| ||||||||
| Соли Fe3+ |     OH O OH O
 Fe3+ + Fe3+ +
SO3H SO3 3
  O- O-
2 SO3
| Кирп. Красный
 не выпал не выпал
|
4. Количественное определение
| Методика | Химизм |
| Метод комплексонометрии 1 ml р-ра ZnSO4 9ml амм. Будера эриохр. Черный Тр Б до синего окрашивания | Zn2+ + Нтр Б Zn ТрБ + Н+
 Zn ТрБ + Н2Inf Zn Inf + HТрБ Zn ТрБ + Н2Inf Zn Inf + HТрБ
|

Протокол результатов анализа лекарственного препарата Sol. Calcii chloridi. 20%-100 ml.
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| 20 % р-р CaCl | Прозрачная жидкость | бесцветный | отсутствует | Горько - соленый |
2. Подлинность
| ЛП | реагент | химизм | Данные исследования |
| На Cl- | AgNO3 |  Cl- + AgNO3 AgCl Cl- + AgNO3 AgCl
  AgCl + NH4OH [Ag(NH3)2]Cl + Н2О AgCl + NH4OH [Ag(NH3)2]Cl + Н2О
| Белый творожистый осадок растворим в аммиаке |
| пламя | t° | Кирпично-красный цвет | |
| На Са2+ | (NH4)2 C2O4 |  Са2+ +(NH4)2 C2O4 CaC2O4 +2NH4 Са2+ +(NH4)2 C2O4 CaC2O4 +2NH4
| Белый осадок |
Протокол результатов анализа лекарственного препарата борной кислоты. Acidi borici. Мм 61,83. Структурная формула Н3 BO3
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| Н3 BO3 | Белый кристаллический порошок | белый | отсутствует | Солено-горький |
2. Подлинность
| ЛП | реагент | химизм | Данные исследования |
| Н3 BO3 | KI H2SO4 крахмал |   ОН Н2SO4 ОС2Н5 ОН Н2SO4 ОС2Н5
 В ОН + 3С2Н5ОН В ОС2Н5+ 3Н2О
ОН ОС2Н5
борноэтил. эфир В ОН + 3С2Н5ОН В ОС2Н5+ 3Н2О
ОН ОС2Н5
борноэтил. эфир
| Горит зеленой каймой |
| С куркум. Бум. | Курк. бум. НСl NH4OH |  О О
   С ОН С ОН
 НО СН = СН-СН-СН-СН- +
Н3СО ОСН3 НО СН = СН-СН-СН-СН- +
Н3СО ОСН3
 О-В-О OH О-В-О OH
    С С
 Н3ВО3 НСl НО СН = СН-СН=С-СН-
Н3СО OCH3 Н3ВО3 НСl НО СН = СН-СН=С-СН-
Н3СО OCH3
| Бурое пятно, при добавление аммиака - черное |
3. Чистота
| испытание | реагент | химизм | Данные исследования | ||
| На Cl- | Ag CO3 |  
| Осадка нет | ||
| SO42- | BaCl2 |  SO42- + BaCl2 Ba SO4
белый SO42- + BaCl2 Ba SO4
белый
| Осадка нет | ||
| Cоли Ca2+ | (NH4)2C2O4 |   Ca2+ +(NH4)2C2O4 CaC2O
белый Ca2+ +(NH4)2C2O4 CaC2O
белый
| Осадка нет | ||
| Fe3+ | KCNS |   Fe3+ + KCNS Fe (CNS)3 Fe3+ + KCNS Fe (CNS)3
| Осадка нет |
Протокол результатов анализа лекарственного препарата раствор димедрола 1% - 10 ml. Sol. Dimedroli.
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| 1% р-р димедрола | прозрачная жидкость | бесцветный | отсутствует | горький |
| ЛП | описание | растворимость |
| 1% р-р димедрола | Белый кристаллический порошок без запаха, горького вкуса гигроскопичен | В воде легко, в спирте, хлороформе, трудно в эфире и бензоле |
2. Подлинность
| ЛП | реагент | химизм | Данные исследования |
| димедрол | Конц. H2SO4 0,2 гр. димед 1-2 кап. H2O |   СН3 СН3
 СН-О-СН2- СН2-N + Н2SО4
СН3 СН-О-СН2- СН2-N + Н2SО4
СН3
    СН3 СН3
 СН-О-(СН2)2- N Н2SО4-
Н СН3 СН-О-(СН2)2- N Н2SО4-
Н СН3
| Ярко-желтое окрашивание, переходящее в кирпично-красное + Н2О оно исчезает |
| 0,01 гр. Препарата 1мл смеси (1мл НNO3 + 9 млH2SO4) по кап. 5 мл Н2О взболтать + 3 мл хлороформа | Красное окрашивание при добавлении Н2О коричневое, хлоформ слой фиолетового цвета | ||
| Сl- | 0,1 мл. препарата 5 мл Н2О кипятить 3 мин, отфильтровать и добавить Ag NO3 |   СН3 t СН3 t
  СН-О-(СН2)2- N + НCl
СН3 СН-О-(СН2)2- N + НCl
СН3
    СН3 СН3
 СН-О-(СН2)2- N Cl-
СН3 СН-О-(СН2)2- N Cl-
СН3
 HCl + AgNO3 AgCl + HNO3 HCl + AgNO3 AgCl + HNO3
|
 Белый осадок
Белый творожный осадок
Белый осадок
Белый творожный осадок
|
3. Чистота
| испытание | реагент | химизм | Данные исследования |
| кислотность | 0,5 препарата 10 мл H2O 1 кап. м/кр 0,1 мл 0,05Н NaOH |   BaCl2 + Na2SO4 BaCl2 + Na2SO4
| Красное окрашивание. Желтое при добавлении NaOH |
| сульфаты | BaCl2 Р-р димедрола 10 мл. (1:10) | Раствор остался прозрачным |
Протокол результатов анализа лекарственного препарата раствор Сalcii gluconats 5% - 100 ml.
Письменный контроль
Кальция глюконата 5,0
Вода для инъекций до 100 мл
Vобщ. 100мл
ОТК ± 5%
[4,75 – 5 – 5,25]
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| Са глюконат | жидкость | бесцветный | отсутствует |
2. Подлинность
| ЛП | реагент | химизм | Данные исследования | |||||
| Са глюконат – 5% | (NH4)2 C2O4 |   Ca2+ + C2O4 Ca C2O4 Ca2+ + C2O4 Ca C2O4
 Ca C2O4 + 2HCl H2C2O4 + CaCl2
растворим Ca C2O4 + 2HCl H2C2O4 + CaCl2
растворим
| <tksq jcfljr | |||||
| пламя | Кирпично-красного цвета | |||||||
| Глюконат СlOH | Fe Cl3 |  
H2O + 2 FeCl3 Са
+ 3CaCl2
Fe2
|
3. Чистота
| испытание | реагент | химизм | Данные исследования |
| кислотность | H2O t° | pH нейтральный | |
| Cl- | AgNO3 | Cl- + AgNO3 | Осадка нет |
| SO42+ | BaCl2 | BaCl2 + SO42+ | Осадка нет |
| прозрачность | Раствор прозрачен |
4. Количественное определение
| Методика | Химизм |
| Метод комплексонометрии до синего окрашивания | Са2+ + Тр Б Са ТрБ
 Са ТрБ + Н2Inf Са Inf + HрТрБ Са ТрБ + Н2Inf Са Inf + HрТрБ
|
Протокол результатов анализа лекарственного препарата Sol. Sulfaciti natrii 30% - 10 ml.
1. Органолептический контроль
| ЛП | описание | цвет | запах | вкус |
| Сульфацил Na | прозрачная жидкость | бесцветный | отсутствует | специфический |
2. Подлинность
| ЛП | реагент |  химизм химизм
| Данные исследования |
| Сульфацил Na (альбуцид) | NaCO3 HCl β - нафтол |  H2N SO2-N-COCH3+HCl+HNO3
Na H2N SO2-N-COCH3+HCl+HNO3
Na
 H2N SO2-N-N H2N SO2-N-N
 Cl Cl
| Вишнево-красное окрашивание |
| СuSO4 |     H2N SO2-N-COCH3+CuSO4
Na H2N SO2-N-COCH3+CuSO4
Na
 H2N SO2-N-CO- Cu
Na H2N SO2-N-CO- Cu
Na
| Осадок голубо-зеленого цвета не изменяется при стоянии | |
| пламя | Окрашивание в желтый цвет |
4. Количественное определение
| Методика | Химизм |
| Метод нейтрализации |   H2N SO2-N-COCH3+HCl м/ор
Na H2N SO2-N-COCH3+HCl м/ор
Na
 H2N SO2-N-COCH+NaCl
H
До розового окрашивания H2N SO2-N-COCH+NaCl
H
До розового окрашивания
|


