а) Реакции замещения. Реакционная активность уменьшается в следующем направлении – пиррол > фуран > тиофен ≈ бензол. Реакции электрофильного замещения (галогенирование, нитрование, сульфирование, алкилирование и ацилирование - см. «Арены») осуществляются в положении 2 (α), протекают в отсутствии ионов водорода Н+ и действия очень слабых электрофилов.
б) Каталитическое гидрирование. Водород присоединяется в присутствии катализаторов (Ni,Pt,Pd) при нагревании, при этом образуются тетрагидропроизводные (тетрафуран, тетрапиррол, тетратиофен):
Тиофен. При восстановлении тиофена образуется тетрогидротиофен: Производным тетрогидротиофена является биотин или витамин Н, или коэнзим R. Молекула биотина состоит из конденсированных тетрогидротиофена, мочевины и валериановой кислоты. 2 Он входит в состав биотиновых ферментов, которые катализируют реакции карбоксилирования и транскарбоксилирования при синтезах высших жирных кислот, белков, пуриновых нуклеотидов. Содержится во всех продуктах животного и растительного происхождения, а также синтезируется микрофлорой кишечника. Недостаточность проявляется в случае употребления большого количества сырого яичного белка или приема сульфаниламидных препаратов и антибиотиков, подавляющих рост бактерий в кишечнике. У человека при недостаточности биотина возникают дерматиты, анемии, депрессии. Производные тиофена содержатся в медицинском препарате ихтиоле, который обладает противовоспалительным, антисептическим и местным обезболивающим действием.
Фуран (фурфуран). Важнейшее производное фурана – фурфурол или а-фуран- 2-альдегид: Получают из пентоз при нагревании их с кислотами. В малых концентрациях он обладает приятным запахом, напоминающих запах свежего ржаного хлеба; в больших концентрациях пахнет неприятно, раздражая слизистые оболочки. По химическим свойствам сходен с ароматическими альдегидами. Из фурфурола получают 5-нитропроизводные, обладающие сильным бактерицидным действием: фурацилин, фуразолидон:
Пиррол. Ароматические свойства пиррола выражены слабее, чем у тиофена. Продуктом полного восстановления пиррола является пирролидин. Ядро пирролидина входит в состав никотина, пролина и гидроксипролина: Пролин (а-пирролидин карбоновая кислота) – аминокислота, образующаяся при гидролизе белков. Остаток пролина участвует в построении молекулы антибиотика – грамицидина С. Ядра пиррола и его продуктов восстановления содержатся в гемоглобине, хлорофилле, витамине В 12, желчных пигментах, образующихся в организме при разрушении гемоглобина. В ряде важных соединений ядро пиррола встречается в виде конденсированной системы, состоящей из пиррола и бензола. Такая система называется индол, или бензопиррол. Свое название индол получил в связи с тем, что впервые был получен из синего красителя индиго.
Природные соединения гетероциклов. Пиррол образует порфирины (содержат 4 молекулы пиррола), которые входят в состав природных соединений, например гема - небелковой части гемоглобина, хлорофилла, витамина В12. Группировка пиррола с бензолом (индол) содержится в триптофане, серотонине, некоторых алкалоидах (резерпин, лизергиновая кислота и т.д.).
Наиболее важные пятичленные гетероциклы с двумя атомами азота:
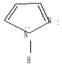
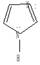 пиразол имидазол
пиразол имидазол
Соединения проявляют амфотерные свойства.
Имидазол (1,3-диазол) входит в состав пуриновых оснований, из него получают лекарственные препараты - антипирин, амидопирин, анальгин и т.д.
-Красное вещество крови гемоглобин. Переносящий кислород из легких в каждую клетку тела, является хромопротеидом, состоящим из белка глобина и окрашенной в красный цвет небелковой части — гема. Гем является порфирином, содержащим Fe (III). Строение гемв выяснил и осуществил синтез Г.Фишер в 1927 году.
-Хлорофиллы в процессе фотсинтеза трансформируют световую энергию в химическую. Его структуру установили в 1913-1938 годах; полный синтез осуществлен Р.Вудвордом в 1956 году.
-Строение витамина В12 — темно-красного кристаллического вещества, установлено Д.Кроуфтом в 1950 году, полный синтез витамина осуществлен Р.Вудвордом в 60-десятых годах 20 века. Это одно из выдающихся достижений органического синтеза.
Шестичленные гетероциклы с одним гетероатомом.
Пиридин – наиболее типичный представитель ароматических гетероциклов. Производные пиридина широко представлены среди веществ, имеющих важное биологическое значение. 3-Метилпиридин – важный синтетический предшественник пиридин-3-карбоновой (никотиновой) кислоты – представителя витаминов В. Амид никотиновой кислоты (никотинамид) – структурный компонент коферментов никотинамидадениндинуклеотида (НАД+) и никотинамидадениндинуклеотидфосфата (НАДФ+). Последний кофермент (один из комплекса витаминов В2, входит в состав эритроцитов и принимает участие в важных биохимических процессах. Молекула пиридина отвечает критериям ароматичности, сформулированным для ароматических углеводородов.
Шестичленные азотсодержащие гетероциклы с одним и двумя гетероатомами:
Пиридин (азин) – 6-членный ароматический гетероцикл с одним атомом азота.
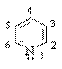
Ароматическая система пиридина включает 6 π-электронов и подобна ароматической системе бензола: каждый атом цикла подает в ароматический секстет один р-электрон. Неподеленная пара электронов азота в силу своей пространственной ориентации в сопряжении не участвует:

Атом азота действует как акцептор и понижает электронную плотность на атомах углерода цикла в положениях 2, 4, 6:
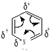 Химические свойства пиридина определяются наличием ароматической системы (электрофильное замещение в 3 и 5 положениях кольца, по активности в этих реакциях уступает бензолу) и основного атома азота (образует соли). Нуклеофильное замещение протекает в положениях 2,4 или 6. Пиридин и метилпиридины (пиколины) — бесцветные жидкости с неприятным запахом, получают из каменноугольной смолы и широко используют в органическом синтезе. При окислении алколоида — никотина впервые была получена никотиновая кислота (3-карбоксипиридин), являющаяся провиамином, а её амид — витамином РР. Недостаток этого витамина вызывает заболевание кожи, называемое пеллагрой.
Химические свойства пиридина определяются наличием ароматической системы (электрофильное замещение в 3 и 5 положениях кольца, по активности в этих реакциях уступает бензолу) и основного атома азота (образует соли). Нуклеофильное замещение протекает в положениях 2,4 или 6. Пиридин и метилпиридины (пиколины) — бесцветные жидкости с неприятным запахом, получают из каменноугольной смолы и широко используют в органическом синтезе. При окислении алколоида — никотина впервые была получена никотиновая кислота (3-карбоксипиридин), являющаяся провиамином, а её амид — витамином РР. Недостаток этого витамина вызывает заболевание кожи, называемое пеллагрой.
Пиримидин (1,3-диазин) – 6-членный ароматический гетероцикл с двумя атомами азота:
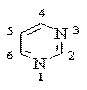
Ароматическая система пиримидина подобна ароматической системе пиридина.
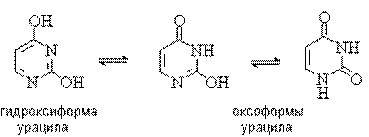
Важную биологическую роль играют гидрокси- и аминопроизводные пиримидина: урацил, тимин и цитозин – нуклеиновые основания; входят в состав нуклеозидов, нуклеотидов, нуклеиновых кислот. Существуют в таутомерных оксо- и гидроксиформах:
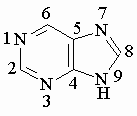
Пурин – ароматическое гетероциклическое соединение, содержащее конденсированные пиримидиновый и имидазольный циклы:
Пурин, подобно имидазолу, существует в виде двух таутомерных форм. Более стабильной является форма с атомом водорода в положении 7:
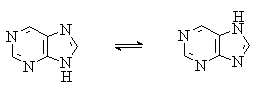
Гидрокси- и аминопроизводные пурина: аденин и гуанин - нуклеиновые основания; входят в состав нуклеозидов, нуклеотидов, в том числе нуклеотидных коферментов, нуклеиновых кислот.
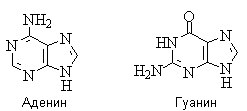
Для аденина известны две таутомерные формы, являющиеся результатом миграции протона между атомами азота имидазольного цикла. У гуанина существуют таутомерные гидрокси- и оксоформы:
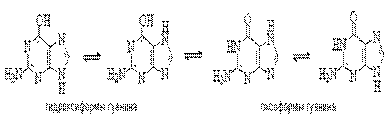
Стабильными таутомерными формами гуанина являются оксо-формы.
Нуклеиновые кислоты
Нуклеиновые кислоты (ДНК и РНК) – биополимеры, которые содержатся в клетках любого живого организма и выполняют важнейшие функции по хранению и передаче генетической информации, участвуют в механизмах ее реализации в процессе синтеза клеточных белков.
В результате последовательного гидролитического расщепления ДНК и РНК можно выделить следующие структурные компоненты: полинуклеотиды → нуклеотиды (рибоза или 2-дезоксирибоза + азотистое основание + фосфорная кислота) → нуклеозиды (азотистое основание + углевод).
Азотистые основания: пиримидиновые, пуриновые.
Пиримидиновые основания- производные пиримидина. Это- урацил, тимин, цитозин.
Пуриновые основания- производные пурина. Это – аденин, гуанин.
https://youtu.be/V6YC97Dj5E0
https://youtu.be/Td15aK0w9uM
Учебник «Репетитор по химии под ред. А.С.Егорова» § 11.4 стр. 714-723.
Таблицы стр.719, 720.