Вариант № 8
Гетерогенная реакция между веществами А и В (табл. 1) протекает при постоянной температуре Т;
1) определите стандартное сродство  веществ А и В при 298 К;
веществ А и В при 298 К;
2) вычислите константы равновесия  и
и 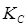 при температуре Т;
при температуре Т;
3) определите количество прореагировавшего твёрдого вещества А, если объём системы V м3, а исходное давление газа В равно Р1, объёмом твердой фазы можно пренебречь;
4) определите изменение энергии Гиббса, для начала реакции, если исходное давление газообразных веществ В и С соответственно равны Р2 и Р3, реакция протекает при температуре Т, К идеально обратимо.
Таблица 1
| Реакция | Т, К | 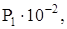 Па Па
|  Па Па
|  Па Па
|  м3 м3
|

|
Решение:


| 
| 
|

| 
| 
|
1) Вычисление стандартного сродства  веществ А и В при 298 К;
веществ А и В при 298 К;




2)Вычисление констант равновесия  и
и 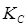 при температуре 773 К.
при температуре 773 К.

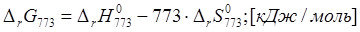


| Вещество | 

|  , Дж/моль∙К , Дж/моль∙К
| Температурный интервал | ||

| 
| 
| |||

| 16,86 | 4,77 | – 8,54 | 298…2500 | |

| 31,46 | 3,39 | – 3,77 | 298…3000 | |

| -110,53 | 28,41 | 4,10 | – 0,46 | 298…2500 |

| - | 28,41 | 4,10 | – 0,46 | 298…2500 |

| - | 48,32 | 8,16 | 12,31 | 298…2500 |

| -9,47 | – 19,91 | –4,06 | –12,77 | 298…2500 |







Константу равновесия 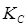 можно найти из соотношения:
можно найти из соотношения:

3)Определение количества прореагировавшего твёрдого углерода, если объём системы  м3, а исходное давление газа
м3, а исходное давление газа  равно
равно  Па
Па
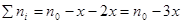 , что говорит о том, что смесь неравновесная
, что говорит о том, что смесь неравновесная


| 
| 
|

| 
| 2 
|
 ,
,

Равновесные парциальные давления определим по закону Дальтона:
 ;
;
 ;
;
где  - общее давление. Закон действующих масс для данной реакции запишется так:
- общее давление. Закон действующих масс для данной реакции запишется так:


С учетом того, что углерода расходуется в 2 раза больше, чем кислорода, то количество прореагировавшего углерода составит 0,005 молей.
4) Определение изменения энергии Гиббса для начала реакции

Самостоятельная работа № 5
Вариант 8
Зависимость константы равновесия реакции от температуры (табл. 9) выражается уравнением  коэффициенты a, b, c и d приведены в табл. 1, давление выражено в Паскалях:
коэффициенты a, b, c и d приведены в табл. 1, давление выражено в Паскалях:
1. определите константу равновесия реакции при Т, К;
2. постройте график зависимости  в интервале температур от (Т – 100) до (Т + 100) К;
в интервале температур от (Т – 100) до (Т + 100) К;
3. укажите, как изменяется константа равновесия при повышении температуры;
4. определите тепловой эффект реакции  при Т, К;
при Т, К;
5. сопоставьте тепловой эффект, вычисленный в п. 4, с тепловым эффектом, вычисленным по закону Кирхгофа при температуре Т, К;
6. определите стандартное сродство реагирующих веществ при температуре Т, К.
| Реакция (А) | К | Т, К |

| 
|
Таблица 1
| a | b | c | d |
| – 4600 | 0,623 | – 0,001 02 | 17,776 |
Решение:
1)Определение константы равновесия при 500 К.
Заменяем десятичный логарифм натуральным, для чего умножаем обе части уравнения на  .
.

Подставляем значение Т в полученное уравнение:

2)Построение графика зависимости  в интервале температур от 400 до 600 К;
в интервале температур от 400 до 600 К;

| 
| 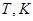
| 
| 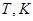
| 
|
| 7,489 | 9,724 | 10,558 | |||
| 8,156 | 9,747 | 10,908 | |||
| 8,747 | 10,173 | 11,228 |
3) Константа равновесия при повышении температуры увеличивается. Принимаем Т=1000К и повторяем расчет. Функция экспоненты в степени х является возрастающей, значит чем больше значение логарифма функции, тем больше сама функция.

4)Определение стандартного теплового эффекта при Т=500К



5)Сопоставление теплового эффекта, вычисленного в п. 4, с тепловым эффектом, вычисленным по закону Кирхгофа при температуре 500 К;
Сначала вычисляем стандартный тепловой эффект при 298 К.


Вычисление теплоёмкостей конечных и исходных продуктов реакции. Значения  и
и  взяты из приложения 1 методического пособия.
взяты из приложения 1 методического пособия.
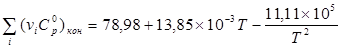





Небольшая разница возникает из-за погрешности вычисления.
6) Вычисление стандартного сродства  веществ А и В при 500 К;
веществ А и В при 500 К;
