Оксидирование
Оксидирование – процесс искусственного образования на поверхности металлов оксидов с целью защиты от коррозии, декоративной отделки, повышения сопротивления износу и др. Наибольшее распространение получило оксидирование алюминия и его сплавов, применяемых в качестве конструкционных материалов в самолетостроении, авиационном моторостроении и автомобилестроении, для изготовления различных изделий бытовой техники и др.
Как известно, алюминий и его сплавы всегда покрыты тонкой (0,02 – 0,04 мкм) естественной оксидной пленкой Al 2 O 3 или Al 2 O 3· nH 2 O, которая, однако, не может служить надежной защитой от коррозии в атмосфере, особенно загрязненной хлоридами. Поэтому для создания более толстого сплошного оксидного слоя изделия из алюминия и его сплавов после очистки от различных загрязнений подвергаются анодному и химическому оксидированию.
Анодное оксидирование производится в серной, хромовой или щавелевой кислотах и их смесях, химическое – преимущественно в щелочных растворах двухромовокислого калия или в хромовокислых растворах с добавками фторидов. Анодная обработка позволяет получать более толстый, плотный окисный слой, чем химическая обработка.
Пленки оксидов на алюминии и его сплавах обладают высокой адсорбционной способностью, что используется при последующей обработке поверхности антикоррозионными жидкостями и различными красителями для повышения защитных и декоративных свойств пленки. Очень толстые (100 мкм и более) оксидные пленки способствуют повышению поверхностной твердости и износостойкости, а также тепло- и электроизоляции поверхности.
Анодно-окисная пленка состоит из двух слоев: тонкого (0,01 – 0,1 мкм) барьерного-беспористого слоя и более толстого пористого. Механизм возникновения и роста такой пленки представляет собой сложную картину физико-химических явлений, протекающих на поверхности алюминия при анодной его поляризации. Предполагается, что тонкий барьерный слой образуется и растет в результате взаимодействия ионов алюминия и кислорода при встречной миграции их в барьерном слое. Ионы алюминия, возникающие по реакции Al → Al 3+ + 3 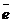 , мигрируют вследствие большой напряженности электрического поля в ионной решетке окисла к внешней поверхности барьерного слоя, а ионы кислорода, образующиеся на поверхности барьерного слоя по реакции Н 2 О → 2 Н + + О 2-, мигрируют в направлении к металлу навстречу ионам Al 3+ (рис. 13.1).
, мигрируют вследствие большой напряженности электрического поля в ионной решетке окисла к внешней поверхности барьерного слоя, а ионы кислорода, образующиеся на поверхности барьерного слоя по реакции Н 2 О → 2 Н + + О 2-, мигрируют в направлении к металлу навстречу ионам Al 3+ (рис. 13.1).
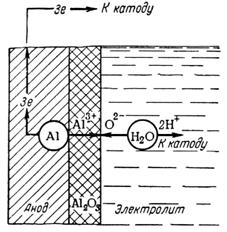
Рис.1. Схема анодного процесса ионизации алюминия, электродной реакции передачи кислорода из молекулы воды на оксидируемый металл и образования Al2O3.
В порах (d = 0,05 – 0,1 мкм), заполненных электролитом, происходит дальнейшее формирование нового барьерного слоя. Таким образом, окисная пленка растет за счет образования пористого слоя, продвигаясь в глубь металла (рис. 13.2).
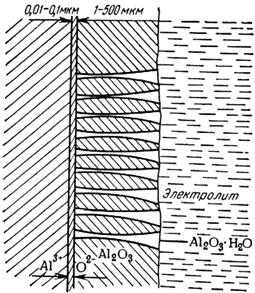
Рис.2. Схема образования оксидной пленки на алюминии.
В общем виде процесс анодного окисления алюминия можно выразить уравнением:
2 Al + 3 H 2 O → Al 2 O 3 + 6 H + + 6 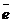 (13.а)
(13.а)
Так как под действием электролита окисная пленка растворяется, то рост ее будет зависеть от относительных скоростей образования и растворения барьерного слоя. При равенстве этих скоростей толщина барьерного слоя сохраняется практически постоянной. При этом с внешней стороны барьерный слой под действием электролита разрыхляется и в нем образуются поры.
Одним из главных условий нормального роста пленки является подбор состава электролита и условий электролиза, при которых образующийся окисный слой в течение электролиза поддерживается как бы в разрыхленном, проницаемом для ионов состоянии. Максимальная толщина анодных пленок для каждого условия проведения процесса имеет предел, до которого возможен их рост.
В качестве электролита при анодном оксидировании чаще всего применяется 20%-ный раствор серной кислоты при температуре около 20°С. При увеличении концентрации H 2 SO 4 и повышении температуры при прочих равных условиях возрастают скорость растворения и пористость пленки и уменьшается толщина пленки. Поэтому при наращивании толстых пленок процесс ведут, как правило, при более низкой температуре. Скорость формирования окисной пленки возрастает при повышении плотности тока. Однако при увеличении плотности тока выше допустимого предела для данных условий скорость формирования может уменьшиться вследствие увеличения температуры в зоне роста пленки.
Пленки толщиной до 10 – 15 мкм получают при комнатной температуре и плотности тока 1 – 2 А/дм2, напряжении 12 – 28 В за 20 – 40 мин, а пленки толщиной 50 – 100 мкм – при температуре не выше 0°С, плотности тока 2 – 10 А/дм2, напряжении 80 – 120 В за 90 мин. В электролите, содержащем серную и щавелевую (или другую органическую) кислоты, толстые пленки можно получать при 20°С. Пленки толщиной 150 мкм и более получают с применением двустороннего охлаждения: электролита и металла (внутреннее охлаждение).
Оксидирование алюминия возможно переменным током в серной и щавелевой кислотах при пониженной концентрации (до 12 – 13%).
Для повышения защитных и антикоррозионных свойств окисной пленки изделия после оксидирования и промывки обрабатывают паром или горячей водой, погружают в горячие растворы хроматов и бихроматов. При этом происходит гидратация оксида и поры смыкаются, а при обработке хроматами, кроме того, образуются соединения типа (AlO)2 CrO 4.
Для окрашивания оксидированной поверхности алюминия применяют органические и неорганические красители. Последние представляют собою нерастворимые соединения, которые образуются в порах пленки в результате химических реакций, протекающих при последовательном погружении изделий в соответствующие растворы. Так, при погружении в растворы железистосинеродистого калия и хлорного железа поверхность окрашивается в синий цвет.
Существует процесс защитно-декоративной обработки алюминия под названием эматалирование. Он отличается от способа оксидирования главным образом тем, что обработку ведут в менее агрессивных электролитах, содержащих щавелевую, борную, лимонную кислоты низкой концентрации и щавелевокислые соли титана, при 40 – 60°С. Получаемые пленки имеют молочный оттенок и хорошо окрашиваются.
Для получения оксидных пленок с высокими электроизоляционными свойствами применяют щавелевокислые электролиты. Такие электролиты могут работать на постоянном и переменном токе. Пробивное напряжение при соответствующей толщине пленки достигает 500 В и выше. Электролит, работающий на постоянном токе, содержат 50 – 70 г/л щавелевой кислоты. Температура электролита 25 – 30°С, анодная плотность тока 1,5 А/дм2, напряжение на ванне 40 – 60 в. Время обработки 0,5 – 2,5 ч.
Для защиты магния и его сплавов от коррозии может быть также применено анодное окисление. В зависимости от методов оксидирования можно получить пленки толщиной до 60 – 80 мкм (защитные пленки, получаемые химическим путем, имеют толщину порядка 3 – 5 мкм).
Используется также оксидирование сталей, для чего применяются концентрированные растворы щелочей или смеси хромовой и борфтористой кислот.
Оксидирование производят переменным током при начальной плотности тока 5 А/дм2 и напряжении 75 В. Температура электролита 70 – 80°С. В состав пленки входят сложные нерастворимые соединения фосфата магния, фторида магния и соединения хрома.
Для анодирования титана применяют серную кислоту, щавелевую или смесь серной и фосфорной кислот.
Толщина оксидных пленок не превышает 1,5 мкм. Эти пленки весьма пористы и хорошо удерживают смазку, обеспечивая улучшение антифрикционных свойств.
Оксидные пленки, получаемые на титане технической чистоты, не проявляют диэлектрических свойств подобно оксидным пленкам на алюминии, т.е. не являются препятствием для прохождения электрического тока. Исключением являются пленки, получаеиз серно-фосфорного электролита.
мые
Электрохимическое и химическое полирование
Электрохимическое полирование производится на аноде преимущественно в кислородсодержащих кислотах (H 3 PO 4, H 2 SO 4, H 2 Cr 2 O 7, HClO 4 и др.) достаточно высокой концентрации при относительно больших плотностях тока. В некоторых случаях применяют смеси минеральных и органических кислот, растворы щелочей (для цинка), цианидов (для серебра), HBF 4 (для алюминия), добавляют к электролитам спирты, эфиры, ингибиторы травления и др. Составы предложенных растворов и режим электролиза весьма разнообразны и выбираются главным образом в зависимости от природы и состава полируемого материала.
Выравнивание и сглаживание микрорельефа поверхности при электрохимическом полировании происходит за счет неодинаковой скорости растворения выступов и углублений. Она будет наблюдаться в том случае, когда основное сопротивление прохождению тока лежит в области диффузионного слоя на поверхности металла. Поэтому, как правило, анодное полирование наблюдается в области анодных предельных токов, обусловленных образованием концентрации насыщения продуктов растворения, то есть при достаточно высоких плотностях тока, зависящих также от скорости перемешивания раствора.
Электрохимическое полирование применяется главным образом для отделки поверхности несложных по форме изделий из алюминия, серебра, нержавеющей стали, а также изделий после покрытий их другими металлами (никелем, медью).
Благоприятное влияние, которое оказывает электрохимическое полирование на фрикционные свойства металла, позволило использовать этот процесс для чистовой обработки деталей, работающих в условиях трения (детали текстильных машин). В последние годы электрополирование применяют для чистовой обработки режущего инструмента (сверла, метчики), для заточки и правки инструмента, а также оно может выполнять роль доводочной операции при изготовлении мерительного инструмента.
Сравнительно новой областью применения электрополирования является электрохимическое изготовление металлографических шлифов.
Химическое полирование применяется реже, чем электрохимическое, так как оно не обеспечивает зеркального блеска поверхности. Однако в отношении экономичности и простоты выполнения химическое полирование имеет несомненные преимущества перед электрохимическим и механическим, особенно при обработке изделий сложной формы. Электролиты отличаются сильным окислительным действием, почти все они содержат азотную кислоту. Механизм процесса точно не установлен. Предполагается, что он подобен механизму электрохимического полирования