Американский трипаносомоз (болезнь Шагаса) – протозойное трансмиссивное заболевание, протекающее с поражением сердца и органов пищеварительного тракта. У детей и неиммунных лиц возможна острая фаза с развитием первичного аффекта, лихорадки и увеличением лимфатических узлов, печени, селезенки, миокардита, иногда с возникновением менингоэнцефалита.
Этиология. Возбудитель – Trypanosoma cruzi – имеет длину 15–20 мкм. В организме позвоночных хозяев трипаносомы проникают в клетки различных органов и тканей, где утрачивают жгутик и приобретают округлую или овальную форму Размножение паразита происходит внутриклеточно с образованием амастигот размером около 2–6 мкм. В течение 1,5–2 мес. амастиготы интенсивно размножаются продольным делением и, заполняя всю клетку, образуют псевдоцисты. В них формируются трипомастиготы, которые после разрушения псевдоцист попадают в кровяное русло и затем внедряются в новые клетки. Вне клеток трипаносомы не размножаются.
Эпидемиология. Резервуаром и источником инвазии являются человек и некоторые дикие и домашние животные: броненосцы, опоссумы, грызуны, обезьяны, собаки, кошки, кролики, свиньи и др. В отличие от человека, у опоссумов трипаносомы постоянно обнаруживаются в крови, что в значительной степени повышает их роль как источника инвазии.
Основной путь передачи американского трипаносомоза трансмиссивный. Переносчиками трипаносом являются крупные летающие клопы рода Triatoma, размерами 15–34 мм. Клопы нападают на спящих людей и кусают в открытые участки тела с нежной кожей, чаще около глаз и губ, из‑за чего получили образное название «поцелуйных» клопов. Во время кровососания происходит заражение клопа, трипаносомы развиваются в кишечнике насекомого и сохраняются в течение всей его жизни – до 2 лет. Одновременно с этим по мере заполнения кишечника насекомого происходит акт дефекации. В его испражнениях содержатся I cruzi (до 3500 в 1 мкл), которые во время расчесывания проникают в организм человека через поврежденную кожу (ранка от укуса, расчесы) или слизистые (наиболее часто конъюнктива глаз) (рис. 13). Возможна передача инвазии при гемотрансфузиях, не исключается трансплацентарный путь.
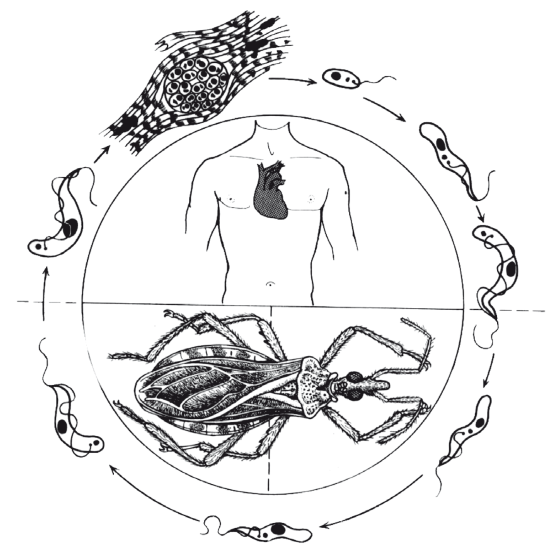
Рис. 13. Схема жизненного цикла Trypanosoma cruzi и ее переносчик – Triatoma megista (no J. Donges, 1980)
Географическое распространение. Американский трипаносомоз встречается в природных и синатропных очагах. Заболевание распространено в Центральной и Южной Америке (рис. 14).
Патогенез. В патогенезе острой стадии ведущее значение имеют токсико‑аллергические реакции, сопровождающиеся аутоиммунными процессами. При поражении интрамуральных ганглиев гладкой мускулатуры кишечника могут возникать «мегасиндромы»: мегаэзофагус, мегадуоденум, мегаколон, мегасигма. В миокарде, скелетных мышцах развиваются воспалительно‑дистрофические изменения, иногда некробиотического характера. В отдельных случаях наблюдаются эндокардиты, перикардиты. Вокруг пораженных трипаносомами клеток отмечаются инфильтраты из лимфоцитов, моноцитов, плазматических клеток, очаги скопления полиморфно‑ядерных лейкоцитов. В случае поражения ЦНС в головном и спинном мозге на вскрытии обнаруживаются кровоизлияния, в субарахноидальном пространстве – желатиноподобный экссудат; твердая и мягкая мозговые оболочки утолщены, гиперемированы, со множественными сращениями. В надпочечниках наблюдаются воспалительные изменения, в печени – жировая дегенерация гепатоцитов.
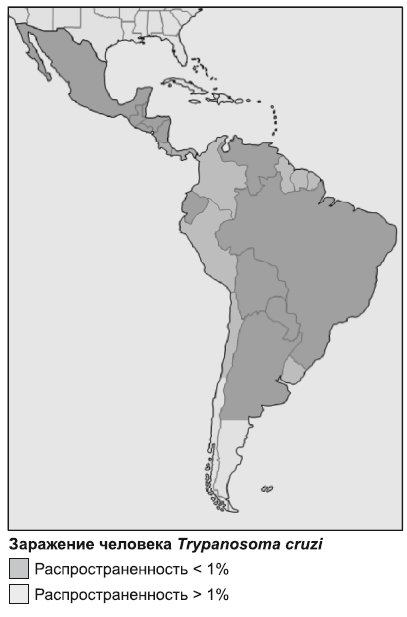
Рис. 14. Распространение американского трипаносомоза в мире (Tropical Infectious Diseases, 2011)
Длительное течение заболевания обусловлено сменой поколений трипаносом: амастигот и трипомастигот. При формировании иммунного ответа на поверхностные белки трипомастигот некоторые из них проникают в клетки и там превращаются в амастиготы, делящиеся и формирующие новую популяцию. При выходе амастигот из псевдоцисты они вновь превращаются в трипомастиготы, у которых есть новый набор поверхностных белков, что позволяет им уходить от иммунного пресса организма хозяина.
Клиническая картина. В развитии болезни выделяют три фазы: острую, латентную и хроническую.
Острая фаза наблюдается главным образом у детей в возрасте до 5–7 лет. Инкубационный период длится от 7 до 14 сут.
Заболевание начинается остро, с недомогания, озноба, головных болей, повышения температуры тела. В месте внедрения паразита часто наблюдается первичный аффект – шагома, представляющая собой воспалительный инфильтрат с лимфангитом и регионарным лимфаденитом. По внешнему виду шагома напоминает фурункул с зоной отека до 4–6 см в диаметре, однако никогда не нагнаивается. При внедрении паразитов через слизистую оболочку глаза развиваются односторонний конъюнктивит, отек век и лица на стороне поражения, которые в совокупности с реакцией околоушных, подчелюстных лимфатических узлов называются синдромом Романьи (рис. 15). Иногда в начале заболевания появляется мелкоточечная сыпь на груди и туловище, сохраняющаяся 8‑10 сут. Увеличиваются шейные, подмышечные и паховые лимфоузлы. С самого начала болезни появляется лихорадка постоянного или ремиттирующего типа, с подъемами температуры тела до 39–40 °C. У большинства больных заболевание сопровождается образованием отеков на лице и конечностях через 10–15 дней от начала лихорадки.
Смертность пациентов в острой фазе достигает 5‑10 % и наблюдается, как правило, у детей в первые 5 лет жизни. Она обусловлена развитием тяжелого острого миокардита, менингоэнцефалита и пневмонии.

Рис. 15. Симптом Романьи у мальчика из Аргентины (Harrison’s Infectious Diseases, 2010)
У взрослых прогноз для жизни более благоприятный, для выздоровления – сомнительный. Болезнь сокращает продолжительность жизни и социальную активность пациентов. Смерть в хронической стадии болезни чаще всего является результатом острой или хронической сердечной недостаточности.
Латентная фаза. После первичного инвазирования, как в случаях с развитием острой фазы болезни, так и при ее отсутствии, наступает длительный период (от 10 до 30 лет), когда клинических проявлений нет. О наличии инвазии свидетельствуют только положительные результаты серологических исследований.
В хронической фазе американского трипаносомоза различают две клинические формы: сердечно‑сосудистую и нервную.
При сердечно‑сосудистой форме развивается хроническое поражение сердечной мышцы (специфическая кардиомиопатия) с недостаточностью кровообращения. Пациенты, страдающие хронической кардиомиопатией, погибают через 1–3 года с момента выявления декомпенсации сердца. Их беспокоит одышка, сердцебиение. Границы сердца расширены, тоны приглушены, иногда выслушивается ритм галопа. Часто поражается и проводящая система сердца: полная блокада правой ножки пучка Гиса, реже – левой ножки, нарушения внутрижелудочковой проводимости. В ряде случаев атриовентрикулярная блокада переходит в полную. Клиническая картина и ЭКГ‑данные в таких случаях соответствуют синдрому Морганьи – Адамса – Стокса. В тяжелых случаях развивается острая сердечная недостаточность со смертельным исходом.
Нервная форма болезни характеризуется судорожным синдромом, развитием параличей (встречаются редко). Чаще нервная форма проявляется значительным расширением полых органов: пищевода, желудка, кишечника, мочеточников, мочевого пузыря, бронхов и др. Нарушения обусловлены поражением интрамуральных нервных узлов, особенно ауэрбаховского сплетения.
Из других поражений описаны орхиты, эпидидимиты, паразитарный зоб, паротиты. В редких случаях у больных развивается менингоэнцефалит, протекающий тяжело, с летальным исходом. Случаев спонтанного выздоровления не отмечается.
Диагностика. Лабораторная диагностика включает следующие методы:
• прямой микроскопический – обнаружение трипаносом в нативных и окрашенных по Романовскому – Гимзе мазках и толстых каплях крови, спинномозговой жидкости, биоптатах шанкра, лимфатических узлах, костном мозге;
• ксенодиагностику – выращивание трипаносом в кишечнике клопов‑переносчиков. Для этого выращенных в лабораторных условиях триатомовых клопов, свободных от трипаносом, помещают в небольших садках на кожу больных людей. В положительных случаях при содержании клопов при 30 °C через 2 недели после кормления в их кишечнике накапливается большое количество трипаносом;
• биологический – заражение белых мышей или морских свинок с последующим исследованием через 7 дней их крови и паренхиматозных органов на наличие трипаносом;
• культуральный – выращивание трипаносом на кровяном агаре (среда NNN);
• серологические – ИФА (ELISA), РИФ, реакция гемагглютинации (РГА), РЛА;
• метод ПЦР. – для выявления ДНК ядра и кинетопласта трипаносом.
Лечение. Эффективного специфического лечения американского трипаносомоза в настоящее время не существует. Наиболее перспективными считаются производные нитрофурана (нифуртимокс) и имидазола (бензонидазол ). Они подавляют паразитемию и более эффективны в острой стадии.
Нифуртимокс (lampit, Ъауег 2505) назначается внутрь по 8‑12 мг/кг в сутки в 3 приема, курс лечения – 3–4 мес. Бензонидазол принимают по 5‑10 мг/кг в сут. Длительность лечения в острой фазе до 30 дней, в хронической – 30–60 дней. Оба этих препарата эффективны в острой стадии болезни в 80 % случаев, однако токсичны: вызывают побочные эффекты у половины пациентов. В хронической фазе болезни их эффективность крайне низка.
В хронической фазе заболевания эффективность использования вышеуказанных препаратов, а также триазолова и алло‑пуринола не доказана. Кортикостероидные препараты противопоказаны. Для лечения вторичных осложнений используют антибиотики. При мегасиндромах проводится хирургическое лечение.
Профилактика: санитарное благоустройство жилых построек в сельских поселках и в пригородах эндемически районов; уничтожение переносчиков современными инсектицидами; санитарно‑просветительная работа среди населения.