Соля́ная кислота́ (хлороводоро́дная, хлористоводоро́дная, хлористый водород) — HCl, раствор хлороводорода в воде; сильная одноосновная кислота. Бесцветная (техническая соляная кислота желтоватая из-за примесей Fe, Cl2 и др.), «дымящая» на воздухе, едкая жидкость. Соли соляной кислоты называются хлоридами. Максимальная концентрация соляной кислоты - около 36%.
Химические свойства
· Взаимодействие с металлами, стоящими в электрохимическом ряду металлов до водорода с образованием соли и выделением газообразного водорода:
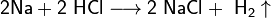
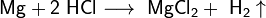
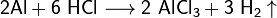
· Взаимодействие с оксидами металлов с образованием растворимой соли и воды:
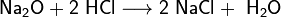
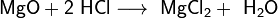

С сильными окислителями кислота соляная ведёт себя как восстановитель, например: MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O.
· Взаимодействие с гидроксидами металлов с образованием растворимой соли и воды (реакция нейтрализации):
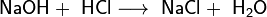
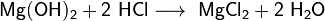
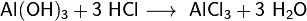
· Взаимодействие с солями металлов, образованных более слабыми кислотами, например угольной:
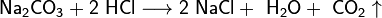
· Взаимодействие с сильными окислителями (перманганат калия, диоксид марганца) с выделением газообразного хлора:
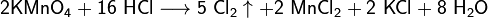
· Взаимодействие с аммиаком с образованием густого белого дыма, состоящего из мельчайших кристалликов хлорида аммония[2]:
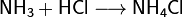
· Качественной реакцией на соляную кислоту и её соли является её взаимодействие с нитратом серебра, при котором образуется творожистый осадок хлорида серебра, нерастворимый в азотной кислоте[3]:
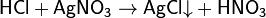
Применение:
Рассмотрим основные направления использования кислоты, чтобы иметь представление относительно того, как и где проявляет свои качества данное вещество:
· Металлургия. Соляная кислота техническая применяется для зачистки металлов при лужении и паянии. Также кислота соляная используется при получении марганца, железа и других веществ.
· Гальванопластика. В этом направлении соляная кислота техническая выступает в роли активной среды при травлении и декапировании.
· Пищевая промышленность. Всевозможные регуляторы кислотности, например, E507, имеют в своем составе кислоту. Да и содовую (сельтерскую) воду трудно представить без такого вещества, как кислота соляная.
· Медицина. В данной сфере, конечно же, используется не соляная кислота техническая, а очищенные аналоги, однако, подобное явление все же имеет место. В частности, речь идет о добавлении вещества в желудочный сок в случае недостаточной кислотности.
· Химическая. Она идёт на получение хлоридов различных металлов и синтез хлор-содержащих органических продуктов. Соляная кислота применяют для травления металлов, для очистки различных сосудов, обсадных труб буровых скважин от карбонатов, окислов и др. осадков и загрязнений.
· Соляная кислота содержится в желудочном соке (около 0,3%); способствует пищеварению и убивает болезнетворные бактерии.
Соляная кислота выпускается следующих сортов: техническая (27,5% НС1); синтетическая (31% НС1), ингибиторная (20% НС1) и реактивная (35—38% НС1, плотность при 20°С равняется 1,17— 1,19 г/см3).
Техническая синтетическая соляная кислота - едкая жидкость, стабильная в химическом отношении. На воздухе "дымит" в результате выделения хлористого водорода и притяжения им влаги воздуха с образованием кислотного тумана. Туман соляной кислоты раздражает верхние дыхательные пути и слизистые оболочки глаз. При попадании па кожу - вызывает ожоги. Класс опасности – 2.
Все работы с соляной кислотой должны проводиться в спецодежде и в защитных очках. Все работающие должны быть обеспечены промышленными фильтрующими противогазами. В случае разлива соляную кислоту смывают с поверхностей пола и оборудования большим количеством воды или щелочного раствора.
Кислоту перевозят и хранят в гуммированных (покрытых слоем резины) стальных цистернах и контейнерах, в фаолитовых баках и контейнерах и в емкостях, изготовленных из керамики и стекла При введении в кислоту 1—3% ингибитора активность НС1 к стали снижается в 150—200 раз, поэтому ингибиторную кислоту перевозят в стальных нефутерованных цистернах.