Одним из факторов, влияющих на всасывание, является молекулярная масса ЛВ, в зависимости от которой реализуется тот или иной механизм всасывания. Большинство ЛВ имеет относительно низкую молекулярную массу, поэтому их основным механизмом всасывания является диффузия (пассивная и облегченная).
Значительное влияние на всасывание в кровь оказывают физико-химические свойства ЛВ. Важным свойством, влияющим на скорость всасывания ЛВ, является их растворимость в воде и липидах (жирах). Согласно данным о фосфолипидной структуре клеточных мембран, вещества с большей липофильностью интенсивнее проникают через мембраны.
На всасывание влияет полярность ЛВ. Неполярные болеелипофильны, а полярные имеют большую степень растворимости в воде. Вещества, растворимые в липидах, легко проникают в клетки тканей.
Важным условием для быстрого всасывания ЛВ является их нахождение в месте введения в неионизированном состоянии. Всасывание веществ основного характера вкислой среде снижается. Многие лекарства липофильного характера могут полностью всасываться в кровь через слизистую оболочку полости рта и оказывать резорбтивное действие. В желудке полного всасывания лекарств обычно не происходит. Вводимые внутрь, они всасываются главным образом в тонком кишечнике, т.е. в том отделе пищеварительного тракта, где всасываются и продукты гидролиза пищевых веществ, что обусловлено анатомо-физиологическими особенностями тонкого кишечника.
К другим факторам, влияющим на процессы всасывания ЛВ, относят лекарственную форму, путь введения, площадь всасывающей поверхности и интенсивность кровоснабжения на участке всасывания. На всасывание ЛВ могут оказывать влияние возраст и пол пациента, беременность и заболевания.
3. ТРАНСПОРТ, РАСПРЕДЕЛЕНИЕ И ДЕПОНИРОВАНИЕ ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ В ОРГАНИЗМЕ
После попадания в кровь ЛВ транспортируются и распределяются в организме в соответствии с их физико-химическими свойствами и уровнем кровоснабжения органа, некоторые избирательно накапливаются (депонируются) в определенном органе. ЛВ в крови находятся в свободной форме (фармакологически активные молекулы) или в связанной форме с белками (альбуминами). В связанной форме препарат циркулирует в сосудистом русле и поступает в ткани лишь после разрыва связи с альбуминами.
Процессы распределения и накопления ЛВ в определенных органах и тканях зависят от растворимости ЛВ в воде и липидах. Липофильные молекулы распределяются в тканях с большим содержанием жировой клетчатки, мозге, клеточных мембранах, а водорастворимые - в крови и лимфе. Многие ЛВ обладают выраженным физико-химическим сродством к белкам плазмы крови (прежде всего к альбуминам). Связывание ЛВ с белками плазмы приводит к снижению их концентрации в тканях и месте действия, что следует учитывать при дозировании таких ЛС, как пропранолол, хлорпромазин, фуросемид, диклофенак, дигитоксин, лозартан, связывающихся с белками плазмы крови на 90% и более.
На процессы транспорта и распределения ЛВ влияют величина концентрации его в крови, скорость кровотока в тканях, а также способность ЛВ проникать через различные биологические барьеры, например гематоэнцефалический, плацентарный, гематоофтальмический. Скорость прохождения ЛВ через барьер зависит от его растворимости в липидах. Лиофильные веществалегко проникают в мозг, а плохо растворимые в жирах вещества почти не проникаютв ткань мозга. Поступление ЛВ из крови матери в кровь плодазависит от проницаемости плацентарного барьера и, как правило,липофильности вещества. Именно поэтому при назначении ЛС в период беременности всегда необходимо тщательно анализировать их способность и характер возможного влияния на плод.
Биодоступность (F, %) отражает количество ЛВ, которое достигло системного кровотока относительно исходной дозы препарата в процентах.
При внутривенном введении биодоступность равна 100%. При других путях введения (даже при внутримышечном и подкожном) биодоступность никогда не достигает 100%.
Лекарственные средства, содержащие одни и те же ЛВ, новыпускаемые различными фармацевтическими фирмами, существенно различаются по терапевтической эффективности и по частоте возникновения и выраженности побочных эффектов, что зависит от различий в их биодоступности. В связи с этим возникло новое понятие - биоэквивалентность. ЛС называют биоэквивалентными в тех случаях, когда они обеспечивают одинаковую концентрацию действующего вещества в крови и тканях организма. В настоящее время существует много примеров биологически неэквивалентных ЛС, например кислота ацетилсалициловая (Россия); Аспирин· (Bayer, Германия), Аспирин Упса• (Франция) или препараты ранитидина: Ранитидин-Акри•, Зантак•, Зантин.
 4. МЕТАБОЛИЗМ (БИОТРАНСФОРМАЦИЯ) ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
4. МЕТАБОЛИЗМ (БИОТРАНСФОРМАЦИЯ) ЛЕКАРСТВЕННЫХ ВЕЩЕСТВ
В организме, преимущественно в печени, лекарственные вещества подвергаются химическим изменениям. Некоторые лекарства могут подвергаться различным изменениям в ЖКТ, в крови, почках, легких и других органах
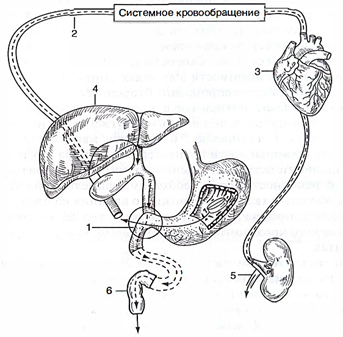
Рис. 4. Фармакокинетические процессы, характерные для сердечных гликозидов: 1 - всасывание - абсорбция и реабсорбция; 2 - транспорт с током крови; 3 - распределение - накопление в сердечной мышце; 4 - метаболизм - отщепление гликона и образование конъюгатов; 5 - выведение - экскреция через почки; 6 - выведение - экскреция через кишечник
Под метаболизмом понимают совокупность химических и биохимических превращений ЛС с образованием их метаболитов. В результате метаболизма вещества становятся высокополярными, гидрофильными (водорастворимыми). Подобное изменениехимической структуры ведет к изменению фармакологических свойств (как правило, уменьшение активности) и увеличению скорости выделения из организма с мочой. Частичнотрансформация лекарственных веществ снижает или сводит к нулю их фармакологическую активность. Однако в некоторых случаях химическиереакции превращают инертное вещество (пролекарство) в высокоактивное соединение.Метаболические реакции, протекающие в микросомах печени, катализируютсямикросомальными ферментами (система цитохромов Р-450).
Немикросомальные ферменты локализованы в цитозоле или митохондриях других органов. Их также можно разделить неспецифические и специфические. К неспецифическим относят оксидазы, редуктазы, транферазы, гидролазы. К специфическим относят моноаминооксидазу (МАО), катехол-O-метилтрансферазу, инсулиназу, алкогольдегидрогеназу и др.
Различают два типа реакций метаболизма лекарственных препаратов в организме: метаболическую трансформацию (несинтетические реакции) и конъюгацию (синтетические реакции).
К несинтетическим реакциям метаболизма относятся: окисление, восстановление и гидролиз. Эти реакции обеспечивают первую фазу метаболизма большинства гидрофобных ЛС.
В основе синтетических реакций лежит процесс соединения (конъюгация) лекарственных веществ с эндогенными субстратами: аминокислотами (глицином, глютатионом, глютамином, глюкуроновой кислотой и др.) и остатками функциональных групп (метильным, ацетильным, карбоксильным, аминным, сульфатным) и др. К синтетическим реакциям относят реакции конъюгации: ацетилирования, метилирования, глюкуронизации, глютанизации и др.
В организме может одновременно происходить несколько описанных выше реакций. Например, соединения фенола могут связываться либо с сульфатом, либо с глюкуроновой кислотой. Хлоралгидрат в организме и окисляется, и восстанавливается, а затем соединяется с глюкуроновой кислотой. ЛС, имеющие в своей структуре реакционно способные группы -ОН, -СООН, -NH2, -SH и другие, могут вступать сразу во вторую фазу - реакции конъюгации.
Способность организма метаболизировать ЛВ может изменяться при патологии печени, под влиянием других ЛВ, курения, алкоголя и др. Для обозначения повышения активности ферментов используют термин «индукция ферментов ». Ускоряется метаболизм вводимых ЛВ, ускоряется их выведение и, как правило, понижается фармакологический эффект. Понижение активности ферментов развивается при «ингибировании ферментов », что характеризуется замедлением метаболизма ЛВ, экскреции и удлинением (иногда усилением) фармакологического эффекта, а в некоторых случаях появлением отрицательных (токсических) реакций.
«Индукторами»микросомальных ферментов печени являютсяпроизводные барбитуровой кислоты (фенобарбитал), рифампицин, карбамазепин; «ингибиторами» - циметидин, хлорамфеникол (левомицетин•), кетоконазол, эритромицин.
Метаболизм ЛВ контролируется и регулируется генетическимимеханизмами через ферментные системы. Наследственные изменения ферментных систем могут существенно изменить биотрансформацию лекарств, приведя к извращению реакции организма навведение препаратов. Фармакогенетика - наука, изучающая генетически обусловленные реакции организма в ответ на введениеЛС. В результате наследственных изменений ферментных систем (дефицит или избыток фермента) происходит снижение или усиление фармакологического эффекта, а в некоторых случаях развивается патологический процесс. Врожденную индивидуальную непереносимость лекарственных средств, обусловленную отсутствием или снижением активности ферментов либо отсутствием систем обезвреживания определенных химических групп введенных лекарственных веществ или образующихся метаболитов, называют идиосинкразией.
ВЫДЕЛЕНИЕ ЛВ И ИХ МЕТАБОЛИТОВ ИЗ ОРГАНИЗМА
Под экскрецией (от лат. excretum - выделение) понимают различные пути выделения ЛВ и их метаболитов из организма (с калом, мочой, с выдыхаемым воздухом, потом, слюной, слезной жидкостью). Основным путем выведения ЛВ и метаболитов являются почки. Для оценки скорости выведения ЛВ с мочой используют показатель почечного клиренса, который отражает скорость очищения плазмы крови от ЛВ в единицу времени (мл/мин). Кровь, попадая в почки, фильтруется в клубочках от находящегося в ней в свободном состоянии ЛВ. В процессе прохождения через канальцы липофильные ЛВ реабсорбируются (обратно всасываются), а полярные, гидрофильные метаболиты выводятся с мочой. В клинической практике для определения режима дозирования используют показатель периода полуэлиминации (Т1/2), который показывает время (часы или минуты) снижения концентрации ЛВ в крови в 2 раза (50%). Например: Т1/2дигоксина 165 ч, сульфалена 65 ч, ампициллина 1 ч, ацетилхолина, эпинефрина 2-3 мин.
На выделение ЛВ оказывают влияние многие факторы, среди них молекулярная масса, концентрация вещества в крови и моче, кислотность мочи и плазмы, растворимость в воде и липидах, почечный и печеночный кровоток и др. В тех случаях, когда лекарственное вещество связано с белком, оно не может фильтроваться в почечных клубочках. В почечных клубочках фильтруются только те вещества, м.м. которых ниже 10000. При повышении рН мочи (моча приобретает большую щелочность) вещества кислого характера ионизируются и лучше выводятся из организма, а препараты со свойствами оснований подвергаются меньшей ионизации, легче становятся липофильными и их реабсорбция усиливается. Растворимые в воде (гидрофильные) вещества и их метаболиты выделяются (элиминируются) (от лат. eliminare - изгонять) в основном почками. При отравлениях для ускорения удаления токсического вещества изорганизма необходимо усилить диурез введением мочегонных преаратов.
Через легкие выделяются газообразные и летучие вещеетва (эфир, хлороформ, этанол). Молочные железы выделяют смолоком различные водорастворимые и жирорастворимые вещесева (снотворные, этанол, морфин, сульфаниламиды, многие антибактериальные препараты), что следует учитывать при назначенииЛС женщинам в период лактации. Многие ЛС (антибактериальные группы пенициллинов, тетрациклинов, сердечные гликозиды из наперстянки) выделяются через желчь, что необходимо учитывать при назначении ЛС, обладающих токсическим действием на печень, и больным с ее заболеванием. ЛВ, плохо всасывающиеся из желудочнокишечного тракта (фталилсульфатиазол, сульфагуанидин, натрия сульфат), выделяются с каловыми массами. Через потовые и сальные железы выделяются в небольших количествах жирорастворимые вещества (йод, бром, салицилаты).