Содержание
Введение
1. Общее понятие о химической реакции
2. Классификация химических реакций
Заключение
Список используемой литературы
Введение
Самое интересное в окружающем мире состоит в том, что он постоянно изменяется.
Понятие «химическая реакция» - второе главное понятие химии. Каждую секунду в мире происходит неисчислимое множество реакций, в результате которых одни вещества превращаются в другие. Некоторые реакции мы можем наблюдать непосредственно, например ржавление железных предметов, свертывание крови, сгорание автомобильного топлива.
В то же время, подавляющее большинство реакций остаются невидимыми, но именно они определяют свойства окружающего нас мира.
Для того, чтобы осознать свое место в мире и научиться им управлять, человек должен глубоко понять природу этих реакций и те законы, которым они подчиняются. Задача современной химии состоит в изучении функций веществ в сложных химических и биологических системах, анализе связи структуры вещества с его функциями и синтезе веществ с заданными функциями.
Итак, химических реакций протекающих вокруг человека очень много, они протекают постоянно. Что же необходимо сделать, чтобы не запутаться во всём многообразии химических реакций? Научиться их классифицировать и выявлять существенные признаки классов.
Цель данной работы: рассмотреть понятие «химическая реакция» и систематизировать и обобщить знания о классификации химических реакций.
Работа состоит из введения, двух глав, заключения и списка литературы. Общий объем работы 14 страниц.
Общее понятие о химической реакции
Химическая реакция - это превращение одних веществ в другие. Однако, такое определение нуждается в существенном дополнении.
Так, например, в ядерном реакторе или в ускорителе тоже одни вещества превращаются в другие, но такие превращения химическими не называют. В чем же здесь дело? В ядерном реакторе происходят ядерные реакции. Они заключаются в том, что ядра элементов при столкновении с частицами высокой энергии (ими могут быть нейтроны, протоны и ядра иных элементов) - разбиваются на осколки, представляющие собой ядра других элементов. Возможно и слияние ядер между собой. Эти новые ядра затем получают электроны из окружающей среды и, таким образом, завершается образование двух или нескольких новых веществ. Все эти вещества являются какими-либо элементами Периодической системы. В отличие от ядерных реакций, в химических реакциях не затрагиваются ядра атомов. Все изменения происходят только во внешних электронных оболочках. Разрываются одни химические связи и образуются другие.
Таким образом, химическими реакциями называются явления, при которых одни вещества, обладающие определенным составом и свойствами, превращаются в другие вещества - с другим составом и другими свойствами. При этом в составе атомных ядер изменений не происходит.
Выделим признаки и условия химических реакций (рис.1, 2).

Рисунок 1 – Признаки химических реакций
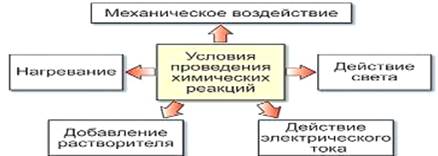
Рисунок 2 – Условия проведения химических реакций
Рассмотрим типичную химическую реакцию: сгорание природного газа (метана) в кислороде воздуха (данную реакцию можно наблюдать дома, у кого есть газовая плита) на рисунке 3.

Рисунок 3 - Сгорание природного газа (метана) в кислороде воздуха
Метан СН4 и кислород О2 реагируют между собой с образованием диоксида углерода СО2 и воды Н2О. При этом разрываются связи между атомами С и Н в молекуле метана и между атомами кислорода в молекуле О2. На их месте возникают новые связи между атомами С и О, Н и О.
На рисунке 3 хорошо видно, что для успешного осуществления реакции на одну молекулу метана надо взять две молекулы кислорода. Однако записывать химическую реакцию с помощью рисунков молекул не слишком удобно, поэтому для записи химических реакций используют сокращенные формулы веществ - такая запись называется уравнением химической реакции.

Рисунок 4 – Уравнение реакции
Уравнение химической реакции показанной на рисунке 3 выглядит следующим образом
CH4 +2O2 = CO2 + 2H2O
Количество атомов разных элементов в левой и правой частях уравнения одинаково. В левой части один атом углерода в составе молекулы метана (СН4), и в правой - тот же атом углерода мы находим в составе молекулы СО2. все четыре водородных атома из левой части уравнения мы обязательно найдем и в правой - в составе молекул воды.
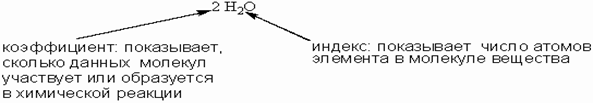
В уравнении химической реакции для выравнивания количества одинаковых атомов в разных частях уравнения используются коэффициенты, которые записываются перед формулами веществ.
Рассмотрим другую реакцию - превращение оксида кальция СаО (негашеной извести) в гидроксид кальция Са(ОН)2 (гашеную известь) под действием воды (рис.5).

Рисунок 5 - Оксид кальция СаО присоединяет молекулу воды Н2О
с образованием гидроксида кальция Са(ОН)2
В отличие от математических уравнений, в уравнениях химических реакций нельзя переставлять левую и правую части. Вещества в левой части уравнения химической реакции называются реагентами, а в правой - продуктами реакции.
Если сделать перестановку левой и правой части в уравнении из рисунка 5, то получим уравнение совсем другой химической реакции
Ca(OH)2 = CaO + H2O
Если реакция между СаО и Н2О (рис. 4) начинается самопроизвольно и идет с выделением большого количества теплоты, то для проведения последней реакции, где реагентом служит Са(ОН)2, требуется сильное нагревание. Добавим также, что реагентами и продуктами могут быть не обязательно молекулы, но и атомы - если в реакции участвует какой-нибудь элемент или элементы в чистом виде, например
H2 + CuO = Cu + H2O
Таким образом, мы подошли к классификации химических реакций, которую рассмотрим в следующей главе.