Массовая доля химического элемента в соединении
Массовая для элемента в данном веществе (w) – отношение относительной атомной массы данного элемента, умноженной на число его атомов в молекуле к относительной молекулярной массе вещества.
где w – массовая доля элемента в веществе, n– индекс в химической формуле, Ar– относительная атомная масса, Mr– относительная молекулярная масса вещества. Массовые доли выражают в процентах или в долях: w(элемента) = 20% или 0,2. АЛГОРИТМ РЕШЕНИЯ Вычислите массовые доли элементов в фосфорной кислоте, имеющей простейшую химическую формулу H3PO4, с точностью до сотых.
|
РАСЧЕТ МОЛЯРНОЙ МАССЫЭКВИВАЛЕНТА СОЕДИНЕНИЯ
Для любого соединения общей является формула (1), но эквивалентное число z для каждого класса находится по-разному. Рассмотрим основные классы неорганических соединений в реакциях нейтрализации и обмена:
|
|
1.Кислоты имеют в своем составе активный водород, способный замещаться в реакциях нейтрализации, следовательно, эквивалентное число z для кислоты равно числу катионов водорода в ее составе, или ее основности.
z кислоты= n(Н+) = основности. (4)
2.Основания имеют в своем составе гидроксогруппу ОН–, способную соединяться с одним ионом водорода:
ОН– + Н+ = Н2О.
Следовательно, эквивалентное число z для основания равно числу гидорксогрупп в его составе, или его кислотности.
z основания= n(ОН–) = кислотности. (5)
3.Соли имеют в своем составе металл и кислотный остаток. Каждая соль может быть получена реакцией нейтрализации, в которой ион металла замещает ионы водорода. Следовательно, эквивалентное число z для соли равно произведению числа атомов металла в ее составе и степени окисления металла.
z соли= n(Ме) · | С.О. (Ме) | (6)
4.Оксиды состоят из элемента и кислорода. Если предположить, что в реакциях обмена элемент замещается на водород, то эквивалентное число z для оксида равно произведению числа атомов элемента и валентности элемента, образующего оксид.
z оксида= n(элемента) * |C.O.(элемента)| (7)
Пример 2: Рассчитайте молярные массы эквивалента для соединений: Cu(OH)2, H2CO3, Al2(SO4)3, Fe2O3.
Решение: Молярная масса соединения равна:
М(Cu(OH)2) = 63.5 + (16 +1)2 = 97.5 г/моль.
Cu(OH)2относится к классу оснований, в своем составе содержит две группы ОН–, эквивалентное число z (Cu(OH)2) = 2. Таким образом, химический эквивалент данного соединения – это условная частица, составляющая 1/2 часть реально существующей молекулы Cu(OH)2, или 1/2 Cu(OH)2.
|
|
Молярная масса эквивалента 1/2Cu(OH)2:
M(1/2 Cu(OH)2 ) = 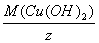 =
= 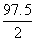 = 48.8 г/моль.
= 48.8 г/моль.
H2CO3 относится к классу кислот, в своем составе содержит два водорода, следовательно, эквивалентное число z (H2CO3) = 2.
Молярная масса соединения равна:
М(H2CO3) = 1×2 + 12 +16×3 = 62 г/моль.
Таким образом, молярная масса эквивалента H2CO3 составляет:
M(1/2 H2CO3) = 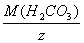 =
= 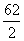 = 31 г/моль.
= 31 г/моль.
Al2(SO4)3 относится к классу солей, в своем составе содержит два атома металла со степенью окисления +3. Эквивалентное число для соли находим по формуле (6):
z (Al2(SO4)3) = n(Al) · | С.О. (Al) |= 2×3 = 6
Молярная масса соединения равна:
М(Al2(SO4)3) = 27×2 + (32 +16×4)×3 = 342 г/моль.
Теперь можно рассчитать молярную массу эквивалента данной соли:
M(1/6Al2(SO4)3)=  =
= 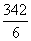 = 57 г/моль.
= 57 г/моль.
Fe2O3 относится к классу оксидов, в своем составе содержит два атома железа со степенью окисления +3. Эквивалентное число для оксида находим по формуле (7):
z (Fe2O3) = n(Fe) * |C.O.(Fe)| = 2×3 = 6
Молярная масса соединения равна:
М(Fe2O3) = 56×2 +16×3 = 160 г/моль.
Далее рассчитаем молярную массу эквивалента данного оксида:
M(1/6 Fe2O3)= 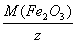 =
= 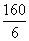 = 26.7 г/моль.
= 26.7 г/моль.
Ответ: 48.8 г/моль; 31 г/моль; 57 г/моль; 26.7 г/моль.