Лекция 1.
Способы фиксации азота.
В обычных условиях азот (N2) – двухатомный газ. Температура кипения при атмосферном давлении – минус 195,8°С, температура плавления – минус 209,9°С. Молекулярная масса азота – 28,016 г, молекулярный объем – 22,404 л/моль (при 0°С и 1 атм).
Процесс перевода атмосферного азота в какие-либо соединения называется фиксацией.
Существует два принципиальных метода фиксации атмосферного азота:
- биологический;
- технический.
Биологическая фиксация атмосферного азота связана с жизнедеятельностью организмов – бактерий, находящихся в почве. К азотофиксирующим бактериям относятся клубеньковые и азотобактеры. Биологический способ фиксации не может обеспечить потребности сельского хозяйства, помимо этого биологическая фиксация азота протекает с низкой скоростью.
Так как соединения азота применяются не только в сельском хозяйстве, но и во многих областях промышленности, необходимо фиксировать атмосферный азот другими способами, способными обеспечить потребности в соединениях азота. Такими способами являются технические методы фиксации.
Технические способы можно условно разделить на три основных группы:
- высокотемпературный метод;
- цианамидный;
- аммиачный.
Высокотемпературная фиксация атмосферного азота.
Метод связывания азота и кислорода, содержащихся в атмосфере, при помощи пламени электрической дуги (дуговой метод) был разработан в начале XX века. Окисление азота воздуха при высокой температуре (около 3300К) происходит по реакции:

Других оксидов азота при данных условиях не образуется.
Зависимость константы равновесия данной реакции от температуры можно описать при помощи уравнения Нернста:

где  – константа равновесия реакции;
– константа равновесия реакции;  – температура, К.
– температура, К.
Равновесную концентрацию NO можно определить по уравнению:

где  – концентрация оксида азота (II), в об.%; 79,2 и 20,8 – концентрации азота и кислорода в воздухе, в об.%.
– концентрация оксида азота (II), в об.%; 79,2 и 20,8 – концентрации азота и кислорода в воздухе, в об.%.
Равновесную концентрацию оксида азота в зависимости от температуры можно рассчитать по эмпирическому уравнению:

Я.Б. Зельдович, П.Я. Садовников и Д.А. Франк-Каменецкий предложили цепной механизм образования оксида азота (II):

На основе цепного механизма Я.Б. Зельдович предложил следующие уравнения для определения скоростей образования и разложения NO:
Скорость образования NO (в моль/(см3·с)):

Скорость разложения NO (в моль/(см3·с)):

где  – текущие концентрации кислорода и оксида азота,
– текущие концентрации кислорода и оксида азота,  – равновесная концентрация оксида азота, моль/см3.
– равновесная концентрация оксида азота, моль/см3.
Цианамидный способ фиксации азота.
Химически чистый цианамид кальция ( ) содержит 34,98% азота, технический продукт – 55-65 мас.% CaCN2, что соответствует 18,6-22,8% азота.
) содержит 34,98% азота, технический продукт – 55-65 мас.% CaCN2, что соответствует 18,6-22,8% азота.
В промышленности цианамид кальция используется для получения цианплава, дициадиамида, тиомочевины. Цианплав используется в сельском хозяйстве для борьбы с грызунами; в металлургии – для закалки специальных сталей.
Химически чистый цианамид кальция представляет собой бесцветные кристаллы; температура возгонки 1363 К. До 1370 К цианамид кальция устойчив, при более высоких температурах происходит частичное разложение.
Цианамид кальция получают взаимодействием тонко измельченного карбида кальция с газообразным азотом при 1320-1370 К. Реакция является обратимой.

Теоретически из 64 кг СаС2 может быть получено 80 кг CaCN2. Фактический выход колеблется в пределах 82-85% от теоретического и зависит от качества сырья, температуры и наличия в шихте добавок.
Влияние температуры и продолжительности азотирования технического карбида кальция на степень связывания азота представлена в таблице:
| Температура, К | Продолжительность азотирования, ч | |||
| Содержание связанного азота, масс. % | ||||
| 0,8 | 1,2 | 1,3 | 1,5 | |
| 2,0 | 5,2 | 8,1 | 9,2 | |
| 7,0 | 14,2 | 19,5 | 21,2 | |
| 22,1 | 23,8 | 24,0 | - |
Хорошие результаты азотирования достигаются при добавлении 2 % (масс.) CaF2. Азотирование карбида кальция при использовании добавки позволяет снизить оптимальную температуру проведения процесса на 100 К.
Карбид кальция должен содержать не более 2% (масс.) оксидов алюминия, железа, кремния, магния.
Азотирование карбида кальция производится газообразным азотом, который получают разделением воздуха. При этом содержание кислорода в азоте не должно превышать 0,2 % (об.), влаги – не более 0,05 г/м3.
На рисунке представлена принципиальная схема получения цианамида кальция.


Рис. 1. Схема производства цианамида кальция: 1- дробилка карбида кальция; 2, 10, 19, 24 – элеваторы; 3, 7, 9, 12, 22, 23, 26, 27 – винтовые конвейеры; 4, 6, 11, 13, 20, 28 – бункеры; 5, 25 – питатели; 8, 21 – трубчатые мельницы; 14, 16 – электрические тали; 15 – охладительные стаканы; 17 – цианамидная печь; 18 – дробилка цианамида кальция; 29 – вагонетка.
Карбид кальция, измельченный в дробилке 1, элеватором 2 подается в бункер 4, откуда поступает в карбидную мельницу 8, которая имеет четыре камеры. В питатель мельницы дополнительно подается плавиковый шпат. Далее измельченная шихта винтовым конвейером 9, элеватором 10 через бункер 11 передается в разгрузочные бункера 13. При помощи мостового крана 14 загрузочный бункер с шихтой устанавливается на съемную воронку цианамидной печи 17, затвор бункера открывается и шихта ссыпается в печь.
Процесс азотирования карбида кальция проводят следующим образом. Шихту загружают в печь в течение 10-12 минут, затем закрывают печь, продувают в течение 8-10 минут азотом для удаления воздуха и включают ток для нагревания электродов. Нагревание до необходимой температуры продолжается в течение 3-х часов при непрерывной подаче азота под избыточным давлением 5-10 мм вод. ст. Спустя еще 4 часа начинается удаление из печи выделяющихся газов (ацетилен, азота) через отверстие в крышке. Подачу азота в печь продолжают до тех пор пока температура не снизится до 870-970 К, после чего подачу азота прекращают и оставляют цианамид кальция в печи на 2 часа для остывания. Цианамидные блоки вынимают из печи и отправляют в отделение окончательного охлаждения.
Охлажденные блоки цианамида кальция поступают в дробилку 18. Дробленный цианамид кальция элеватором 19 разгружается в бункер 20, установленный над трубчатой мельницей 21, в которой производится доизмельчение продукта.
На рисунке 2 представлена схема канальной цианамидной печи.
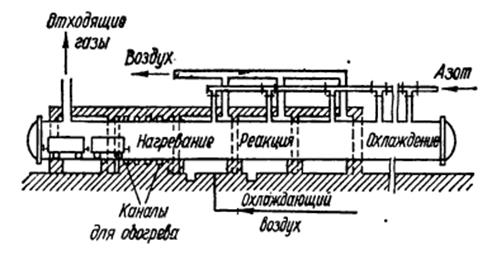
Рис. 2. Схема канальной цианамидной печи.
Внутреннее пространство канала разделено на три зоны: зону нагревания, реакционную зону и зону охлаждения продукта.
Размолотую шихту загружают в ящики, помещенные на тележках, которые по рельсам вкатываются в печь. Тележки поступают в первую зону, где подогреваются горячим газом, движущимся противотоком. После тележки переходят в зону нагрева, где шихта разогревается до температуры, необходимой для начала реакции азотирования.
В реакционной зоне происходит азотирование карбида кальция. В последней зоне происходит охлаждение полученного цианамида кальция. Азот поступает в печь с торца, противоположного места загрузки тележек. Процесс нагрева и азотирования в канальной печи составляет в среднем 28 часов.
Цианамидное производство является взрывоопасным. Сам цианамид кальция является вредным веществом для человека. Поэтому цианамидный способ фиксации азота, так же как и высокотемпературный не нашел широкого применения.
Наибольшее распространение в промышленности получил аммиачный способ фиксации атмосферного азота.