Ноября 2020 г. (пятница)
Дисциплина: Химия
Группа: № 74
Урок №10
Литература: Рудзитис Г. Е. Химия. 11 класс: учеб. для общеобразоват. организаций с прил. на электрон. носителе базовый уровень / Г. Е. Рудзитис, Ф. Г. Фельдман. – М.: Просвещение, 2014. – 224 с.
Материалы урока:
Повторить теоретический материал стр. 37-39
Тема: Природные соединения металлов.
М.В. Ломоносов в своем трактате "Слове о пользе химии" так писал о роли металлов в жизни человека: " Металлы подают укрепление и красоту важнейшим вещам в обществе потребным... И кратко сказать ни едино ремесло, ни едино художество простое употребление металлов миновать не может…". Но применять металлы человечество научилось задолго до наших дней.
Уже в глубокой древности человеку были известны семь металлов: золото, серебро, медь, олово, свинец, железо и ртуть. Из этих металлов человек вначале познакомился с теми, которые в природе встречаются в самородном виде. Это золото, серебро и медь. Остальные четыре металла вошли в жизнь человека после того, как он научился добывать их из руд с помощью огня.
Часы истории человечества стали отсчитывать время быстрее, когда в его жизнь вошли металлы и их сплавы. Век каменный сменился веком медным,
Нахождение металлов в природе.
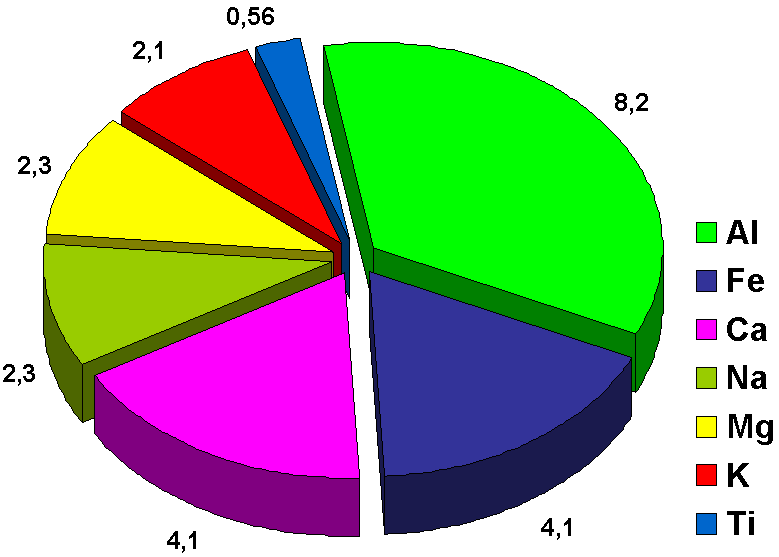 Многие металлы широко распространены в природе.
Многие металлы широко распространены в природе.
Содержание некоторых металлов в земной коре (%) отображено на диаграмме.
Большое количество натрия и магния содержится в морской воде - 1,05% и 0,12% соответственно.
В природе металлы встречаются в различном виде:
В самородном состоянии: медь, золото, серебро, платина, иногда ртуть
В виде оксидов: магнетит Fe3O4, гематит Fe2О3 и др.
Смешанные оксиды: каолин Аl2O3•2SiO2•2Н2О, алунит (Na,K)2O•Аl2О3•2SiO2, др
Сульфиды: галенит PbS, киноварь НgS, серный колчедан FeS2
Хлориды: сильвин (KCl), галит (NaCl) и сильвинит (КСl•NаСl), карналлит КСl•МgСl2•6Н2О
Сульфаты: глауберова соль Nа2SO4•2Н2О, гипсCaSO4•2H2O, баритВaSO4
Карбонаты: мел, мрамор, известняк СаСО3, магнезит МgСО3
Фосфаты: апатит Са3(РО4)2
Многие металлы часто сопутствуют основным природным минералам: скандий входит в состав оловянных, вольфрамовых руд, кадмий — в качестве примеси в цинковые руды, ниобий и тантал — в оловянные.
Железным рудам всегда сопутствуют марганец, никель, кобальт, молибден, титан, германий, ванадий.
Почему большинство металлов встречается в виде соединений?
 Большинство металлов в природе встречается преимущественно в виде соединений. Эти природные соединения называются минералами .
Большинство металлов в природе встречается преимущественно в виде соединений. Эти природные соединения называются минералами .
Природные минеральные соединения, из которых технологически возможно и экономически целесообразно добывать металлы, называют рудами.
В состав руды, кроме полезных минералов, входит еще пустая порода.
В зависимости от того, какие соединения
металлов содержатся в руде, различают:
а) оксидные руды - Fe3O4, Аl2О3;
б) сульфидные руды - FeS2, MoS2;
в) хлоридные руды - NaCl, MgCl2;
г) карбонатные - СаСО3, FeCO3.
Домашнее задание:
Контрольные вопросы (выполните тест):
1. Химические свойства металлов определяются:
А-положением в периодической таблице, строением атомов,
Б-строением атомов, особенностями химической связи,
В-особенностями химической связи, физическими свойствами.
Г-физическими свойствами, положением в периодической таблице
2.Сумма коэффициентов в уравнении реакции горения магния
А) 5; Б) 6.
3. Сумма коэффициентов в уравнении реакции взаимодействия алюминия с хлором
А) 7; Б) 8.
4. В химических реакциях металлы являются:
А-окислителями,
Б-восстановителями.
5. В результате взаимодействия металлов с серой образуются:
А-сульфаты
Б-сульфиты
В-сульфиды
6. Взаимодействие натрия с водой выражено схемой:
А-Na + H2O NaOH + H2
Б-Na + H2O Na2O + H2
В- Na + H2O NaOH
7. Одним из продуктов реакции взаимодействия железа с водой является:
А- FeO
Б-Fe2O3
В-Fe3O4
8. При взаимодействии меди с концентрированной серной кислотой образуется:
А-CuSO4 + H2
Б-CuSO4 + H2O
В- CuSO4 + SO2 + H2O
Г- реакция не идет.
Выполненное домашнее задание сфотографировать и прислать!!!