МОЛЕКУЛЯРНАЯ ФИЗИКА И
ТЕРМОДИНАМИКА
СБОРНИК
ИНДИВИДУАЛЬНЫХ ЗАДАНИЙ ПО ФИЗИКЕ
Новосибирск 2016
УДК: 53(075)
Составители: доц. И.М. Дзю, д.т.н., проф. С.В. Викулов, ст. преп. А.П. Минаев
Рецензент: к.т.н., доц., Е.П. Матус, НГАСУ (Сибстрин)
Молекулярная физика и термодинамика. Сборник индивидуальных заданий по физике / Новосиб.гос.аграр.ун-т. Инженерный ин-т; сост.:И.М. Дзю, С.В. Викулов, А.П. Минаев – Новосибирск: НГАУ, 2016. – 84 с.
Сборник индивидуальных заданий по физике (Молекулярная физика и термодинамика): составлен в соответствии с действующей программой курса физики. Каждое индивидуальное задание содержит 11 задач, охватывающие основные понятия молекулярной физики и термодинамики.
Предназначенно для студентов обучающихся по всем направлениям и формам обучения, реализуемым в НГАУ.
Утверждено и рекомендовано к изданию методическим советом Инженерного института протокол №7 от 1 марта 2016 г.
@ Новосибирский ГАУ,2016
ВВЕДЕНИЕ
В учебном пособии рассмотрены три темы: «Молекулярная физика», «Основы термодинамики» и «Реальные газы и жидкости».Материал тем изложен следующим образом. Кратко изложена суть рассматриваемых тем, по каждой из них в систематизированной форме приведены основные законы и формулы. Приведены примеры решения типовых задач и двенадцать вариантов индивидуальных заданий.
Пособие может быть использовано на практических и контрольных занятиях, при выполнении домашних заданий, а также при самостоятельном изучении курса физики.
МОЛЕКУЛЯРНАЯ ФИЗИКА
Молекулярная физика – раздел физики, изучающий строение и свойства вещества исходя из молекулярно – кинетических представлений, основывающихся на том, что все тела состоят из атомов и молекул, находящихся в непрерывном хаотическом движении. Атомы и молекулы взаимодействуют между собой с силами притяжения и отталкивания.
Законы поведения огромного числа молекул, являясь статистическими закономерностями, изучаются с помощью статистического метода.
Агрегатные состояния вещества: 1) твёрдое тело; 2) жидкость; 3) газ; 4) плазма.
Модель идеального газа: 1) собственный объём молекул газа пренебрежимо мал по сравнению с объёмом сосуда; 2) между молекулами газа отсутствуют силы взаимодействия; 3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Основные законы и формулы
Количество вещества однородного газа (моль)
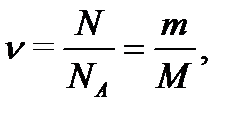 (1.1)
(1.1)
где N - число молекул газа;  число Авогадро;
число Авогадро;  масса газа, кг;
масса газа, кг;  молярная масса, кг/моль; M - молярная масса.
молярная масса, кг/моль; M - молярная масса.
Количество вещества смеси газов
 (1.2)
(1.2)
где  соответственно количество вещества, число молекул, масса, молярная масса i - й компоненты смеси.
соответственно количество вещества, число молекул, масса, молярная масса i - й компоненты смеси.
Уравнение Клапейрона – Менделеева
 (1.3)
(1.3)
 (1.4)
(1.4)
где  универсальная газовая постоянная;
универсальная газовая постоянная;  термодинамическая температура, К;
термодинамическая температура, К; 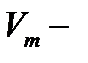 молярный объём, м3/моль;
молярный объём, м3/моль;  постоянная Больцмана;
постоянная Больцмана;  концентрация молекул (число молекул в единице объема).
концентрация молекул (число молекул в единице объема).
Число Лошмидта – число молекул, содержащихся в 1 м3 газа при нормальных условиях ( давление;
давление;  термодинамическая температура)
термодинамическая температура)
 (1.5)
(1.5)
Основное уравнение молекулярно - кинетической теории газов
 (1.6)
(1.6)
где  средняя квадратичная скорость, м/с;
средняя квадратичная скорость, м/с;  средняя кинетическая энергия молекулы газа.
средняя кинетическая энергия молекулы газа.
Распределение молекул идеального газа по скоростям (закон Максвелла)

где  функция распределения, которая определяет относительное число молекул
функция распределения, которая определяет относительное число молекул  , скорости которых лежат в диапазоне от
, скорости которых лежат в диапазоне от  до
до  .
.
Функция  удовлетворяет условию нормировки
удовлетворяет условию нормировки

Характерные скорости функции распределения 
1) наиболее вероятная
 , (1.7)
, (1.7)
2) средняя арифметическая
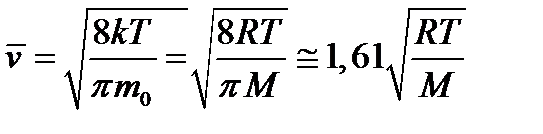 , (1.8)
, (1.8)
3) средняя квадратичная
 . (1.9)
. (1.9)
Распределение молекул идеального газа по энергиям теплового движения
 . (1.10)
. (1.10)
Средняя кинетическая энергия  молекулы идеального газа
молекулы идеального газа
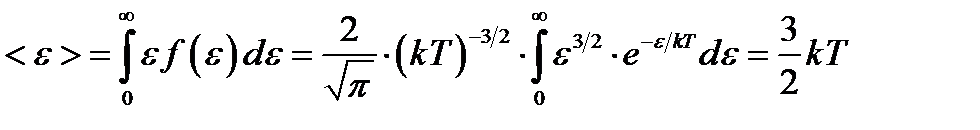 . (1.11)
. (1.11)
Барометрическая формула
 (1.12)
(1.12)
Распределение Больцмана
 (1.13)
(1.13)
где  - концентрация молекул в том месте, для которого
- концентрация молекул в том месте, для которого  принята равной нулю,
принята равной нулю,  - концентрация молекул в том месте, где потенциальная энергия молекулы равна
- концентрация молекул в том месте, где потенциальная энергия молекулы равна  .
.
Средняя длина свободного пробега молекул
 (1.14)
(1.14)
Среднее число столкновений молекулы за 1 с
 (1.15)
(1.15)
Закон диффузии Фика
 (1.16)
(1.16)
 (1.17)
(1.17)
где  плотность потока массы – величина, определяемая массой вещества, диффундирующего в единицу времени через единичную площадку, перпендикулярную оси х;
плотность потока массы – величина, определяемая массой вещества, диффундирующего в единицу времени через единичную площадку, перпендикулярную оси х;  градиент плотности;
градиент плотности;  коэффициент диффузии.
коэффициент диффузии.
Закон теплопроводности Фурье
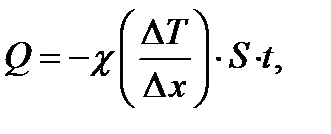 (1.18)
(1.18)
 (1.19)
(1.19)
где  плотность теплового потока – величина, определяемая энергией, переносимой в форме теплоты в единицу времени через единичную площадку, перпендикулярную оси х;
плотность теплового потока – величина, определяемая энергией, переносимой в форме теплоты в единицу времени через единичную площадку, перпендикулярную оси х;  градиент температуры;
градиент температуры;  коэффициент диффузии, где
коэффициент диффузии, где  удельная теплоёмкость газа при постоянном объёме.
удельная теплоёмкость газа при постоянном объёме.
Закон внутреннего трения (вязкости) Ньютона
 (1.20)
(1.20)
 (1.21)
(1.21)
где  плотность потока импульса – величина, определяемая полным импульсом, переносимым в единицу времени в положительном направлении оси х через единичную площадку, перпендикулярную оси х;
плотность потока импульса – величина, определяемая полным импульсом, переносимым в единицу времени в положительном направлении оси х через единичную площадку, перпендикулярную оси х;  градиент скорости;
градиент скорости;  коэффициент внутреннего трения (динамическая вязкость).
коэффициент внутреннего трения (динамическая вязкость).
ОСНОВЫТЕРМОДИНАМИКИ
Термодинамика – раздел физики, изучающий общие свойства макроскопических систем, находящихся в состоянии термодинамического равновесия, и процессы перехода между этими состояниями. Термодинамика не рассматривает микропроцессы, которые лежат в основе этих превращений. Этим термодинамический метод отличается от статистического метода. Термодинамика базируется на двух началах – фундаментальных законах, установленных в результате обобщения опытных данных.
Молекулярно-кинетическая теория и термодинамика взаимно дополняют друг друга, образуя единое целое, но отличаясь различными методами исследования. Термодинамика имеет дело с термодинамической системой – совокупностью макроскопических тел, которые взаимодействуют и обмениваются энергией, как между собой, так и с другими телами (внешней средой).