Состояние каждой термодинамической системы может полностью определяться с помощью термодинамических потенциалов. Каждому из них приписывается определенный набор независимых параметров состояния. Кроме упомянутой выше внутренней энергии U, к термодинамическим потенциалам относят: энтальпию Н, свободную энергию Гельмгольца F, свободную энергию Гиббса G. Они могут быть определены с помощью формул, где P - давление, V - объем, S - энтропия и T - температура.
 (4)
(4)
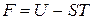 (5)
(5)
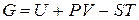 (6)
(6)
Свободная энергия Гиббса соответствует состоянию системы, при котором давление и температура являются постоянными. Поэтому этот термодинамический потенциал употребляют для описания биологических систем. Полезная работа в таких системах выполняется за счет уменьшения потенциала Гиббса.
Величина свободной энергии Гиббса, приходящейся на один ион вещества, называется электрохимическим потенциалом, который включает химическую, осмотическую и электрическую составляющие энергии:  (7)
(7)
здесь 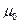 - стандартный электрохимический потенциал, зависящий от химической природы вещества; C - концентрация вещества, R - универсальная газовая постоянная, T - термодинамическая температура, z - электрический заряд частицы, F - константа Фарадея,
- стандартный электрохимический потенциал, зависящий от химической природы вещества; C - концентрация вещества, R - универсальная газовая постоянная, T - термодинамическая температура, z - электрический заряд частицы, F - константа Фарадея, 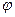 - электрический потенциал.
- электрический потенциал.
Электрохимический потенциал натрия, калия и некоторых других веществ играет решающую роль в таком важном процессе как перенос веществ в мембранах клеток.
Термодинамика неравновесных процессов
Термодинамика равновесных систем основана на принципах, которые в известной мере идеализируются. Биологические объекты не находятся в состоянии равновесия. Процессы, проходящие в таких системах, являются необратимыми. Термодинамика неравновесных процессов основана на таких принципах и понятиях как линейные соотношения, производство энтропии, стационарное состояние, теорема Пригожина.
Линейные соотношения
Закон линейных соотношений определяет зависимость между термодинамическими силами и изменениями (потоками) в термодинамических системах. Термодинамические силы представляют собой различные градиенты (концентрации, электрические, температурные и т.п.) Закон линейных соотношений указывает, что изменение физической величины J является линейной функцией соответствующей термодинамической силы X, где L является коэффициентом прямой пропорциональности: 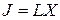 (8)
(8)
Линейный закон обобщает многие эмпирические принципы, например, закон Фика (зависимость переноса веществ от концентрационного градиента), закон Ома (зависимость переноса электрического заряда от градиента электрического потенциала) и т.п.
Каждое отдельное изменение в системе может вызвать только уменьшение её свободной энергии и повышение энтропии. Но другие изменения в этой же системе могут происходить так, что повышение энтропии при одном изменении компенсировалось её уменьшением из-за другого изменения.
Например, некоторые частицы могут перемещаться через мембрану клетки в направлении их более высокой концентрации. При этом происходит уменьшение энтропии системы, которое компенсируется гидролизом АТФ, в результате которого энтропия системы увеличивается.