Необходимость постоянного пополнения запасов воды возникает оттого, что она разными путями постоянно выводится из нашего организма. Некоторую часть уносит выдыхаемый воздух, и ее можно увидеть как пар, образующийся при дыхании в холодный день. Другая часть выводится с экскрементами (очень мало, в основном при диарее (расстройстве кишечника), и именно потеря воды делает ее столь опасной для новорожденных, у которых запасы воды еще малы). Вода также испаряется с потом даже в прохладные дни. И наконец, часть выводится в виде мочи.
При необходимости организм может «экономить» воду. Если потребление воды не соответствует потребностям организма, моча становится более концентрированной, и из организма выводится меньше воды. Обычно в день выделяется около 1300 миллилитров мочи. При необходимости ее может выделяться всего 500 миллилитров. Но это предел. Даже если вы умираете от жажды, организм все равно будет терять воду, которая ему так нужна. Именно по этой причине наступает смерть от нехватки воды.
Почки помимо прочего являются тем предохранительным клапаном, который защищает нас от того, чтобы мы не захлебнулись в собственной жидкости в тех редких случаях, когда пьем больше воды, чем нужно. Если, например, любовь к пиву выражена у человека до такой степени, что в организм поступает избыточное количество жидкости, то организм может легко и быстро избавиться от излишка при помощи почек. Поэтому у любителей пива после обильного возлияния напитка всегда бывает не менее обильное выделение разбавленной мочи.
У некоторых животных, особенно обитающих в пустыне, выработались механизмы сохранения воды, которые по совершенству намного превосходят наши. Вода из пищи и полученная в результате обмена веществ полностью заменяет им воду, которую они теряют. О таких животных пишут в разделах «Хотите верьте, хотите нет» или называют их животными, которые «никогда не пьют».
Углекислый газ представляет бóльшую проблему, чем метаболическая вода. Часть углекислого газа используется организмом. От излишка он должен избавиться, иначе погибнет. Клетки сразу же справляются с этой проблемой самостоятельно, выделяя углекислый газ в кровь. Таким образом, кровь служит как средством транспорта, так и местом выброса отходов одновременно, что может показаться нерациональным, но действует очень эффективно.
Когда кровь достигает легких, она избавляется от избытка углекислого газа, который, как свидетельствует название, представляет собой газ. Проходя через альвеолы, молекулы углекислого газа выходят в воздух, их наполняющий, в то самое время, как молекулы кислорода из воздуха переходят в кровь. В каждом случае происходит переход молекул из области большей концентрации в область меньшей. В результате, хотя вдыхаемый воздух на 20 % состоит из кислорода и на 0,03 % из углекислого газа, в выдыхаемом воздухе содержится 15 % кислорода и 5 % углекислого газа. (Оставшаяся часть представлена азотом.)
Возникает вопрос, как перемещается в крови двуокись углерода. С одной стороны, эта проблема не столь серьезна, как перенос кислорода. Кислород плохо растворяется в воде, поэтому его транспорт во многом определяется содержанием гемоглобина. В 100 миллилитрах воды при температуре тела растворяется всего 2,5 миллилитра кислорода, но зато целых 53 миллилитра углекислого газа. Это решает проблему его транспортировки, если вопрос заключается только в том, чтобы просто избавиться от углекислого газа.
Хотя химические свойства углекислого газа являются причиной многих осложнений, организм, справляясь с ними, сохраняет значительное количество этого продукта распада, чтобы он служил для выполнения жизненно важных функций. Чтобы это понять, понадобится дополнительное разъяснение.
Молекулы углекислого газа не просто растворяются в воде, а вступают в реакцию с молекулами воды, образуя угольную кислоту (ее часто называют просто углекислотой). Это можно изобразить химическим уравнением, где C обозначает углерод, O – кислород, а H – водород:
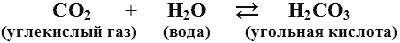
Обычно такая реакция проходит очень медленно, но в кровеносной системе она протекает быстрее. Углекислый газ, попадающий в плазму из клеток, может легко проходить сквозь мембрану красных клеток, так что часть молекул углекислого газа неизбежно окажется внутри эритроцита. В нем есть фермент, способный ускорять образование двуокиси углерода и воды. Обычно ферменты отвечают за ускорение реакций, которые протекают и без них, но со значительно более медленной скоростью. Этот фермент называется карбоангидразой, и в его молекулах содержится по крайней мере один атом металла – цинка. В организме есть и другие цинксодержащие ферменты, и одного этого достаточно, чтобы понять, почему цинк так важен для человека. Конечно, он нужен только в мизерных количествах, и в любой пище его вполне достаточно. В присутствии карбоангидразы быстро образуется угольная кислота, которая через мембрану красной клетки выходит обратно в плазму.
Угольная кислота также может расщепляться с образованием углекислого газа и воды. Поэтому у написанного выше уравнения две стрелочки, указывающие два направления. Карбоангидраза ускоряет процессы как расщепления, так и образования угольной кислоты. В результате такого двунаправленного процесса достигается равновесие, при котором происходит одновременное образование и расщепление угольной кислоты. Поэтому в крови есть как угольная кислота, так и углекислый газ.
В легких сквозь мембраны альвеол может просочиться только углекислый газ. Угольная кислота на это не способна, потому что она не газ. Однако, когда углекислый газ покидает кровь, хрупкое равновесие между содержанием его и угольной кислоты в крови нарушается. Тогда часть угольной кислоты превращается в воду и углекислый газ, чтобы сохранить равновесие, а углекислый газ, в свою очередь, опять выходит в легкие. Поэтому угольная кислота никогда не препятствует механизму выведения углекислого газа из организма.
Угольная кислота может расщепляться и другим способом. Кислота – это вещество, молекулы которого могут терять часть своих атомов водорода. Атом водорода, лишившийся одного электрона, называется ионом водорода. В оставшейся части находится дополнительный электрон (тот, который принадлежал атому водорода), и такой атом называется бикарбонатным ионом. Эта реакция происходит в обоих направлениях, между которыми также существует равновесие. Химическое уравнение реакции можно изобразить следующим образом:

Образующиеся в результате этой реакции ионы имеют электрические заряды. Бикарбонатный ион несет отрицательный заряд, а ион водорода положительный заряд, и это представлено маленькими значками «минус» и «плюс» в верхней правой части формулы ионов.
Получается, что когда углекислый газ попадает в кровь, то в ней появляются три разных вещества: собственно углекислый газ, угольная кислота и бикарбонатный ион. Все эти три вещества находятся в состоянии равновесия. Добавьте к ним немного любого из трех веществ, и часть его быстро превратится в оставшиеся два. Удалите какое‑то количество одного из трех веществ, и два других частично заменят утерянное. Таким образом, когда углекислый газ выходит в легкие, угольная кислота расщепляется и образует двуокись углерода, а бикарбонатные ионы связываются с ионами водорода, чтобы пополнить запас углекислоты. Это происходит само собой: организм просто следует бесстрастным и объективным законам химического равновесия. В результате любое локальное изменение «разбавляется» в большом объеме и сводится к минимуму. Это самое полезное свойство живой ткани – тонкой и хрупкой конструкции, не способной выносить резкие изменения.
Только не поймите последнее утверждение неправильно. Наш организм в состоянии выносить резкие изменения. Мы можем выйти из жарко натопленного дома на морозный зимний воздух, потому что внутренняя температура нашего тела даже при резком перепаде наружной остается неизменной. Большая часть химической активности организма направлена на предотвращение влияния изменения внешних условий на стабильное состояние внутренних тканей.
В качестве примера возьмем равновесие между углекислотой и бикарбонатным ионом, о которых мы только что говорили. Это один из самых важных химических механизмов, при помощи которых организм защищает нежные клетки от изменений, и по этой причине организм никогда не избавляется от углекислого газа полностью, сохраняя часть этого продукта распада для поддержания жизни.
Теперь о воде. Молекула воды состоит из двух атомов водорода и одного атома кислорода. Сама по себе вода очень слабо распадается, теряя ион водорода (как это было в случае с угольной кислотой. Оставшаяся называется гидроксильным ионом (атом водорода + атом кислорода + электрон, оставшийся после отрыва иона водорода)[1].
Ионизация воды представляет собой еще одну реакцию, происходящую в двух направлениях для достижения равновесия. В чистой воде большинство молекул остаются целыми. Всего одна из шестидесяти миллиардов молекул воды ионизирована. То есть на шестьдесят миллиардов молекул приходятся всего один ион водорода и один гидроксильный ион. То, что в воде находится одинаковое количество ионов обоих видов, делает ее нейтральным веществом.
Эти два типа ионов поддерживают обратный баланс (по образцу качелей). Если концентрация ионов водорода увеличивается, соответственно падает концентрация гидроксильных ионов. Тогда этот раствор становится кислотой – чем больше в нем ионов водорода, тем сильнее выражена кислая реакция. С другой стороны, если концентрация ионов водорода уменьшается, концентрация гидроксильных ионов растет. Тогда раствор превращается в щелочь – чем больше гидроксильных ионов, тем сильнее выражена щелочная реакция. (При наличии воды концентрация обоих видов ионов никогда не достигает нулевой отметки.)
Ион водорода – одно из самых активных химических веществ. Почти любая химическая реакция проходит быстрее или медленнее, в зависимости от концентрации ионов водорода. Организм, в котором протекают тысячи реакций, должен следить, чтобы концентрация ионов водорода в тканях поддерживалась на нужном уровне.
Что касается крови, то концентрация ионов водорода должна быть такой, чтобы среда оставалась слегка щелочной. В крови только один ион водорода приходится на каждые двести сорок миллиардов молекул воды, это всего одна четверть от того числа, которое должно присутствовать, чтобы кровь была нейтральной.
Это маленькое количество ионов надо сохранить. Если концентрация ионов водорода увеличивается на 35 % или падает на 25 % от исходного уровня, нарушаются химические механизмы регуляции постоянства внутренней среды, и тогда может наступить смерть. В ходе химических реакций постоянно образуются или утилизируются щелочные или кислотные по природе вещества. Они могут попадать в поток крови или выходить из него. В любом случае они изменяют концентрацию ионов водорода в ту или другую сторону, и эти колебания должны быть сведены к минимуму.
Химики представляют концентрацию ионов водорода в растворе величиной pH[2]. Нейтральный уровень pH составляет 7,0. Меньшие значения pH указывают на кислый раствор – чем ниже pH, тем выше кислотность. Большие значения говорят о щелочном растворе. Поскольку pH – это обратный десятичный логарифм, то в растворе с pH, равным 6,0, концентрация ионов водорода в десять раз выше, чем в растворе с 7,0. pH, равный 5,0, свидетельствует о том, что концентрация ионов водорода в десять раз выше, чем при pH, равном 6,0. В растворе с уровнем pH 8,0 концентрация ионов водорода составляет всего одну десятую часть от присутствующих в растворе с pH 7,0. pH крови равен 7,4, он не должен опускаться ниже 7,32 и подниматься выше 7,46.
Одним из самых важных средств защиты от смертельно опасного изменения уровня pH является сочетание в крови углекислого газа, углекислоты и иона бикарбоната.
Предположим, что в процессе химических реакций в кровь попадает некоторое количество кислоты. Она является новым источником ионов водорода, поэтому их концентрация в крови возрастает, а уровень pH падает.
Но как только появляются эти дополнительные ионы водорода, некоторые из них соединяются с бикарбонатными ионами, образуя углекислоту, которая, в свою очередь, расщепляется на воду и углекислый газ, выводящийся через легкие. Таким образом, избыток ионов водорода не приводит к значительным изменениям уровня pH.
Допустим, что в кровь попадает некоторое количество щелочи – вещества, которое вступает в реакцию с ионами водорода и убирает их из раствора, снижая их концентрацию до опасно низкого значения.
Однако, чтобы этого не случилось, вновь на защиту встает углекислый газ, но на этот раз действия происходят в обратном порядке. Углекислота отдает ионы водорода, чтобы заместить потерянные, и переходит в бикарбонатные ионы. Чтобы восстановить содержание углекислоты в крови, углекислый газ, который до этого выходил из крови в легкие, задерживается в ней и, соединяясь с водой, образует угольную кислоту.
Таким образом, углекислый газ защищает кровь от нежелательных изменений уровня pH в крови. Бикарбонатный ион играет роль сухой губки, впитывающей ионы водорода, когда их слишком много. Углекислота действует как влажная губка, из которой можно выжать ионы водорода, когда их слишком мало. Они позволяют сохранить постоянный баланс pH.
Система, состоящая из углекислоты и бикарбонатных ионов, которая поддерживает pH на постоянном уровне, представляет собой пример того, что химики называют буферной системой, или просто буфером.
В крови содержатся и другие буферы, но система углекислоты и бикарбонатных ионов самая важная, потому что она находится под более тщательным контролем, чем остальные. Из всех буферов только этот представляет собой равновесие с газом, который может удаляться быстрее (при учащении дыхания) или медленнее (при замедлении дыхания).
Именно углекислый газ, а не количество кислорода в атмосфере контролирует частоту дыхания. Обычно границу между сферами деятельности этих двух газов провести сложно, поскольку, как правило, если в крови слишком много углекислого газа, то мало кислорода. Если вы начинаете дышать быстрее, чтобы избавиться от двуокиси углерода, то автоматически пополняете запас кислорода. То же самое происходит и в обратном случае.
Так как частота дыхания может регулировать уровень pH в крови, то последний можно изменять посредством изменения первого. Например, можно намеренно заставить себя на какой‑то период времени дышать быстро и глубоко. В результате углекислый газ удаляется из организма, а углекислота очень быстро расщепляется, чтобы возместить потерю. Это, в свою очередь, ведет к тому, что ионы бикарбонатов присоединяют слишком много ионов водорода, чтобы восстановить содержание углекислоты. В итоге в крови снижается концентрация ионов водорода и повышается уровень pH, что приводит к дыхательному алкалозу. Вы как бы пьянеете от кислорода, у вас появляется головокружение. Если продолжать в том же духе, то можно потерять сознание, однако обычно мы не доходим до этого и возвращаемся к нормальному ритму дыхания. Мы начинаем дышать очень медленно, иногда даже задерживаем дыхание, чтобы восстановить в крови прежний уровень двуокиси углерода.
Можно, наоборот, задержать дыхание на пару минут, чтобы в организме увеличилось содержание углекислого газа, что приведет к накоплению углекислоты, в результате чего в кровь попадет больше ионов водорода. В итоге в крови увеличится концентрация ионов водорода и уменьшится уровень pH – разовьется дыхательный ацидоз. И опять вряд ли вы станете терпеть до того момента, когда потеряете сознание, вы в течение нескольких минут будете усиленно дышать, чтобы избавиться от избытка углекислого газа.
Углекислый газ переносится кровью не только в растворенном виде. Гемоглобин, чьей основной функцией является транспорт кислорода, также служит переносчиком углекислого газа.
Углекислый газ может соединяться с аминокислотой лизином, входящей в состав молекулы белка. Такое соединение называется карбаминовым. Гемоглобин не только занимает первое место среди других белков по содержанию в крови, но также содержит больше лизина, чей любой другой из них. Поэтому около одной пятой части всего углекислого газа в венозной крови представлено в виде карбгемоглобина.
Гемоглобин служит не просто средством транспортировки. Он активно способствует переносу углекислого газа в легкие.
Давайте подробнее рассмотрим, что происходит, когда кровь из легочной артерии – голубоватая, лишенная кислорода, полная растворенным в ней углекислым газом, который частично соединился с водой, а частично с гемоглобином, – попадает в альвеолярные капилляры.
Прежде всего кислород проникает сквозь альвеолярные мембраны в кровь и превращает гемоглобин в оксигемоглобин.
Дальше происходят два события. Во‑первых, оксигемоглобин не образует карбаминовые соединения так быстро, как гемоглобин. Около двух третей карбаминовых групп в карбгемоглобине расщепляется немедленно, и высвобождается углекислый газ.
Во‑вторых, оксигемоглобин – более сильная кислота, чем гемоглобин, в его растворах содержится больше ионов водорода. Все белки в какой‑то степени являются кислотами, все они обладают тенденцией к ионизации и высвобождению ионов водорода. Поглощая кислород из легких, кровь внезапно наполняется ионами водорода. В действие вступает буферная система. Ионы бикарбонатов соединяются с избыточными ионами водорода, в результате образуется углекислота, которая распадается до углекислого газа и воды.
Таким образом, превращение гемоглобина в оксигемоглобин двумя различными способами способствует образованию углекислого газа в крови. Увеличение концентрации углекислого газа в капиллярах альвеол есть тот толчок, который заставляет выходить его из крови и проникать сквозь мембраны альвеол в воздух, находящийся в легких. Затем происходит выдох, и организм освобождается от углекислого газа.
Углекислый газ и метаболическая вода – продукты распада, которые состоят из атомов водорода и углерода, находившихся в пище. Помимо них в пище содержатся атомы азота, которые встречаются в основном в белках – один атом азота из двенадцати.
Было бы хорошо, если бы атомы азота могли превращаться в газ и выходить через легкие, как углекислый газ. Возможно, первым вопросом у человека, впервые столкнувшегося с этой областью науки, будет следующий: поскольку водород и углерод соединяются с кислородом и выводятся из организма, то почему азот не может выводиться тем же способом? Ведь различные окиси азота также представляют собой газы.
К сожалению, на этом пути возникает препятствие. Когда водород и углерод соединяются с водой, они теряют много энергии, и выделившаяся энергия используется организмом. Для соединения азота с кислородом, наоборот, требуется энергия, поэтому для образования окисей азота понадобятся ее дополнительные источники. Нам повезло, поскольку благодаря этому свойству кислород и азот в воздухе не взрываются. Различие энергий не позволяет им вступать во взаимодействие, даже если в воздухе содержится избыток тепла от лесного пожара или пылающей печи. Для соединения азота с кислородом требуется удар молнии, и то это происходит только в непосредственной близости от нее, но организм не может тратить столько энергии, чтобы избавляться от продуктов распада.
Почему бы тогда не избавиться от азота как от газа? Препятствий с энергетической стороны проблемы не возникает, однако ни у одного организма выше уровня бактерий (микроорганизмы более разнообразны с химической точки зрения, чем многоклеточные организмы) нет для этого специального химического механизма.
Можно было бы также превратить азот в аммиак, молекула которого состоит из одного атома азота и трех атомов водорода. Это сопровождается потерей энергии, потому что превращение белка в воду, углекислый газ и аммиак сопровождается меньшей затратой энергии, чем превращение его в воду, углекислый газ и азот. Однако затраты меньше всего на 2 %, и небольшое количество дополнительной энергии, создаваемое при превращении азота, очевидно, не стоит того, чтобы у организмов был создан специальный механизм для подобных превращений.
Аммиак – газ, но он хорошо растворим в воде. В 100 миллилитрах холодной воды может раствориться 110 000 миллилитров аммиака. Он может по мере образования растворяться в воде, имеющейся в организме.
Но тут же возникает проблема. Аммиак – очень ядовитое вещество. Если в литре крови растворится всего одна тысячная доля миллиграмма аммиака, наступит смерть.
Поэтому аммиак должен немедленно выводиться из организма. Это можно сделать, только если организм будет постоянно окружен большим количеством воды, куда можно сбрасывать аммиак, чтобы тот все время растворялся в ней и его концентрация в организме не достигала опасной отметки. Это означает, что только существа, обитающие в океанах и другой водной среде, могут позволить себе роскошь избавляться от азота в виде аммиака. Если вам интересно, не переполнится ли за миллиарды лет океан аммиаком и не случилось ли так уже много лет назад, не волнуйтесь. Аммиак используется одноклеточными растениями, населяющими поверхность океана; он перерабатывается ими в белок, которым они питаются и который опять превращают в аммиак. Это часть цикла азота, в результате которого океаны очищаются от аммиака.
Когда жизнь появилась на суше, ей пришлось приспосабливаться к среде, где было мало воды. Она взяла с собой частичку океана в виде кровеносной системы, но это была всего лишь крошечная частичка. Выброс аммиака во «внутренний океан», заключенный в собственном организме, очень быстро привел бы к повышению концентрации аммиака до опасных значений, а из организма нельзя выводить воду столь быстро, чтобы снизить этот уровень, если только не разработать какой‑нибудь способ быстрого восстановления уровня воды. На суше такое восстановление невозможно.
Поэтому азот должен был выводиться в менее токсической форме, нежели аммиак, иначе земля не смогла бы покориться животным. К счастью, решение было найдено. Две молекулы аммиака могли соединяться с молекулой углекислого газа, образуя мочевину. Ее молекула состоит из одного атома углерода, одного атома кислорода, двух атомов водорода и четырех атомов азота.
Мочевина – твердое вещество, но растворяется в воде в два раза легче, чем поваренная соль, так что она без труда попадает в кровь. К тому же, по сравнению с аммиаком, мочевина относительно безопасна. В литре крови, в котором не может без угрозы для жизни содержаться даже одной тысячной доли миллиграмма аммиака, без всяких последствии содержится сорок миллиграммов мочевины.
Когда головастики превращаются в лягушек, они изменяют систему выведения азота с аммиака на мочевину. Этих изменений мы не видим. Мы замечаем потерю хвоста и появление лапок. Превращение жабер в легкие заметно лишь частично. Однако изменение химического механизма, хотя и не такое заметное, является более важным, чем другие трансформации.
В мочевине содержится больше энергии, чем в аммиаке, поэтому животные, избавляющиеся от азота в виде мочевины, теряют часть своей энергии. Однако преимущества такого механизма выведения азота превышают эти ничтожные потери.
Некоторые насекомые, птицы и рептилии проводят первые несколько дней или недель свой жизни на суше в яйцах. Через скорлупу яиц вода не только поступает в очень ограниченных количествах, но и ее запасы нельзя возобновить при помощи питья. Поэтому способ удаления азота опять должен меняться. Если бы мочевина образовывалась в яйцах, концентрация этого вещества достигла бы в них опасного уровня (даже мочевина может представлять угрозу для жизни, если ее слишком много) еще до того, как зародыш вылупится из яйца. Поэтому азот выводится в виде мочевой кислоты – соединения более сложного, чем мочевина, состоящего из фрагментов четырех молекул аммиака и трех молекул углекислого газа. Мочевая кислота довольно плохо растворяется, поэтому не попадает в воду. Вместо этого она откладывается в особых местах внутри яйца, где не мешает развитию зародыша. Мочевая кислота по сравнению с мочевиной вызывает несколько большие потери энергии, но все равно ее преимущества неизмеримо превышают недостатки.
Млекопитающие, в том числе и человек, которые первые недели или месяцы своей жизни развиваются в материнском теле, приобрели более примитивную систему выведения азота. Мочевина, образующаяся у плода, просачивается сквозь плаценту в кровеносные сосуды матери, которая всегда в состоянии пополнить запасы воды, поэтому млекопитающим не нужен механизм выведения азота в виде мочевой кислоты.
Растения, у которых нет циркулирующей жидкости, также должны как‑то избавляться от азота. Некоторые решают эту проблему, вырабатывая сложные азотсодержащие соединения – алкалоиды, которые откладываются в коре, корнях, семенах и листьях. Обычно при попадании внутрь они оказывают мощное воздействие на организм животных и человека, и многие из них вредны для здоровья или смертельно ядовиты, в зависимости от дозировки.
Если бы клетки выбрасывали мочевину в кровеносное русло, то ее количество в крови быстро бы достигло опасной отметки. Однако, совершая свой круговорот в организме, кровь проходит через два органа, имеющих форму бобов и расположенных в области поясницы по обеим сторонам позвоночника, – почки.
Как и легкие, почки представляют собой губчатую ткань, кровеносную систему которых от внешнего мира отделяет лишь тонкая оболочка. Легкие разделяются на крошечные альвеолы, вдоль которых проходит кровь, а почки – на канальцы. Когда кровь проходит по этим канальцам, через их стенку просачивается вода с растворенными в ней мелкими молекулами, в том числе и молекулами мочевины.
Когда раствор двигается по почечным канальцам, некоторое количество воды и почти все вещества вновь возвращаются в кровь. Продукты распада, такие, как мочевина и вода, в которой она растворяется, остаются в канальце. Этот раствор представляет собой мочу. Микроскопические дозы мочи проходят через миллиарды почечных канальцев и попадают в более широкие и длинные каналы (по одному в каждой почке) – мочеточники. По ним моча попадает в мочевой пузырь, где она собирается и откуда периодически выводится. Какую‑то часть мочи представляют пигменты, придающие ей желтоватый цвет.
Клетки организма постоянно вырабатывают мочевину, а почки все время ее выводят, и таким образом количество мочевины в крови поддерживается на низком и относительно постоянном уровне. Если почки из‑за инфекции или других заболеваний не в состоянии постоянно выполнять очистительную функцию, в крови начинает увеличиваться концентрация мочевины. Это состояние называется уремией и может привести к смертельному исходу. Деятельность почек настолько важна, что у них есть собственный механизм поддержания кровообращения. Если по какой‑то причине приток крови замедляется, почка выделяет фермент под названием ренин. Он изменяет один из белков в крови, превращая его в соединение – ангиотезин, который сужает различные кровеносные сосуды, поднимает кровяное давление и ускоряет кровообращение.
В этой главе я упоминал о том, как содержание воды в организме может изменяться посредством выделения более концентрированной мочи в период дефицита воды и более частого мочеиспускания при переизбытке жидкости в организме. Почки управляют этим процессом, контролируя обратное всасывание воды в почечных канальцах. Если в организме не хватает воды, возвращается больше жидкости, при переизбытке – меньше.
Эта функция почек, в свою очередь, управляется химическим веществом – вазопрессином, вырабатываемым в малых количествах гипофизом[3]– маленьким органом, расположенным в основании мозга. У некоторых людей гипофиз не в состоянии выполнять эту функцию. В таком случае вазопрессин не образуется и контроль над деятельностью почек утрачивается.
Следовательно, вода в почечных канальцах плохо всасывается обратно или не всасывается совсем, и у больного человека учащается мочеиспускание – до трех литров в день или больше. Эта болезнь называется несахарным диабетом. Слово «диабет» происходит от греческого «сифон», и, действительно, вода просто откачивается из организма больного, который, постоянно испытывая жажду, много пьет. «Несахарный» указывает на то, что в этом случае моча настолько разбавлена, что представляет собой практически одну воду. Больным несахарным диабетом можно помочь, их состояние можно значительно улучшить (хотя болезнь полностью вылечить нельзя) при помощи инъекций вазопрессина, полученного из гипофиза крупного рогатого скота.
Вазопрессин – это гормон, химическое вещество, вырабатываемое специальным органом – железой, которое попадает в кровь и участвует в химических реакциях в организме. Многие гормоны являются белками и имеют довольно маленькие молекулы. Например, молекула вазопрессина состоит из восьми аминокислот, по сравнению с шестьюстами аминокислотами в молекуле гемоглобина. В 1953 году группа биохимиков из медицинской школы Корнелльского университета в Нью‑Йорке под руководством Винсента дю Виньо синтезировала этот гормон – первый пептидный гормон, полученный не из гипофиза животного.
Синтез вазопрессина стал последним штрихом в доказательстве точной структуры молекулы этого гормона и явился важным шагом к пониманию механизма действия гормонов вообще. Принимая во внимание чрезвычайную важность гормонов для организма, последствия, вызываемые избыточной или недостаточной продукцией того или иного гормона, и их роль в лечении различных заболеваний, изучение гормонов широко и интенсивно продолжается до сегодняшнего дня. За свои открытия в этой и других областях биохимии Винсент дю Виньо в 1955 году получил Нобелевскую премию в области химии.