Опорный конспект
19.11.2020
Тема урока:
Простые вещества – МЕТАЛЛЫ. Строение, физические свойства. Сплавы
Металлическая связь
Особенностью строения атомов металлов является небольшое количество электронов - на последнем энергетическом уровне от 1 до 3. Это валентные электроны. Валентные электроны удерживаются ядрами атомов крайне слабо, и некоторые из них способны к относительно свободному, хаотичному движению. Атомы, оставшиеся без внешних электронов, приобретают положительный заряди, другими словами превращаются в положительно заряженные ионы. Валентные электроны, перемещаясь между атомами и ионами внутри пространства металла, образуют так называемый электронный газ. Совокупность обобществлённых валентных электронов (электронный газ), заряженных отрицательно, удерживает положительные ионы металла в определённых точках пространства - узлах кристаллической решётки, например, металла серебро. Между положительно заряженными ионами и отрицательно заряженными обобществлёнными электронами образуется металлическая связь
Металлическая химическая связь способствует образованию кристаллов с металлической кристаллической решеткой. В узлах кристаллической решетки находятся атом-ионы металлов, а между ними свободно движущиеся электроны. Металлическая связь отличается от ионной, т.к. нет анионов, хотя есть катионы. Отличается она и от ковалентной, т.к. не образуются общие электронные пары.
.

Рисунок 1.
Строение кристаллической решетки металлов
Таким образом, кристаллическая решетка зависит и определяется видом химической связи, но в то же время она определяет определённый набор физических свойств.
Физические свойства простых веществ
Физические свойства металлов определяются именно их строением.
а) твердость – все металлы кроме ртути, при обычных условиях твердые вещества. Самые мягкие – натрий, калий. Их можно резать ножом; самый твердый хром – царапает стекло
б) плотность. Металлы делятся на мягкие (5г/см³) и тяжелые (меньше 5г/см³).
в) плавкость. Металлы делятся на легкоплавкие и тугоплавкие.
г) электропроводность, теплопроводность металлов обусловлена их строением. Хаотически движущиеся электроны под действием электрического напряжения приобретают направленное движение, в результате чего возникает электрический ток.
При повышении температуры амплитуда движения атомов и ионов, находящихся в узлах кристаллической решетки резко возрастает, и это мешает движению электронов, и электропроводность металлов падает.
Следует отметить, что у некоторых неметаллов, при повышении температуры электропроводность возрастает, например, у графита, при этом с повышением температуры разрушаются некоторые ковалентные связи, и число свободно перемещающихся электронов возрастает.
д) металлический блеск – электроны, заполняющие межатомное пространство отражают световые лучи, а не пропускают как стекло. Попадают на узлы кристаллической рещетки. Поэтому все металлы в кристаллическом состоянии имеют металлический блеск. Для большинства металлов в ровной степени рассеиваются все лучи видимой части спектра, поэтому они имеют серебристо-белый цвет. Только золото и медь в большой степени поглощают короткие волны и отражают длинные волны светового спектра, поэтому имеют желтый цвет. Самые блестящие металлы – ртуть, серебро, палладий. В порошке все металлы, кроме Al и Mg, теряют блеск и имеют черный или темно-серый цвет.
е) пластичность
Механическое воздействие на кристалл с металлической решеткой вызывает только смещение слоев атомов и не сопровождается разрывом связи, и поэтому металл характеризуется высокой пластичностью.

Сплавы
Металлы используются человеком уже много тысячелетий. По именам металлов названы определяющие эпохи развития человечества: Бронзовый Век, Железный Век, Век Чугуна и т.д. Ни одно металлическое изделие из числа окружающих нас не состоит на 100% из железа, меди, золота или другого металла. В любом присутствуют сознательно введенные человеком добавки и попавшие помимо воли человека вредные примеси.
Абсолютно чистый металл можно получить только в космической лаборатории. Все остальные металлы в реальной жизни представляют собой сплавы — твердые соединения двух или более металлов (и неметаллов), полученные целенаправленно в процессе металлургического производства.
Рассмотрите рисунок №12.1 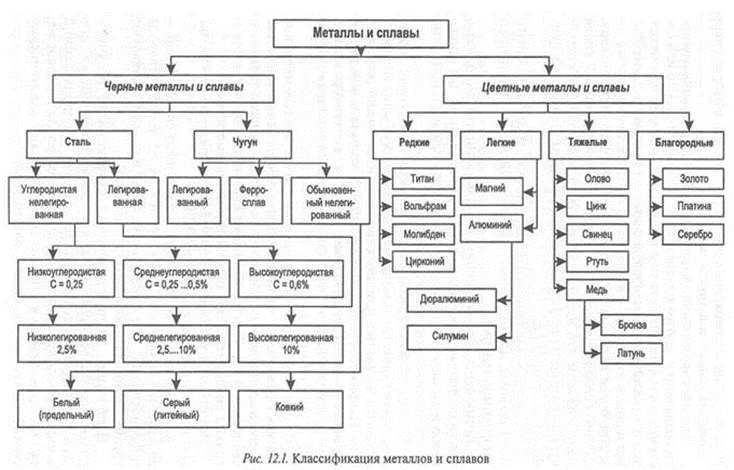
Домашнее задание:
Параграф №6, 7
Заполнить таблицу
Решить задачу №4 страница 38
| Название сплава | Состав | Свойства | Применение |
| Бронза | |||
| Латунь | |||
| Дюралюминий | |||
| Чугун | |||
| Сталь | |||
| Мельхиор | |||
| Сплав Вуда |