При разработке химико-технологических процессов проводятся разнообразные расчеты для количественной оценки протекающих операций, а также для определения оптимальных значений параметров технологического процесса. Во всех случаях при расчетах учитываются законы гидродинамики, тепло- и массопередачи и химической кинетики, поэтому расчеты материальных потоков обычно сочетаются с энергетическими расчетами, для этого составляют материальный и энергетический балансы.
Материальный баланс – это вещественное выражение закона сохранения массы вещества, согласно которому во всякой замкнутой системе масса веществ, вступивших во взаимодействие, равна массе веществ, образовавшихся в результате этого взаимодействия, т.е. приход вещества ΣGприх равен его расходу Σ Gрасх. Таким образом, уравнение материального баланса можно представить в виде:
ΣGприх = ΣGрасх.
Для периодических процессов материальный баланс составляют в расчете на одну операцию, для непрерывных процессов – за единицу времени.
Материальный баланс составляют по уравнению основной суммарной реакции с учетом параллельных и побочных реакций. Он может быть составлен для всех веществ, участвующих в процессе, или только для одного какого-либо вещества. Обычно учитываются не все протекающие реакции и получаемые побочные продукты, а лишь те, которые имеют существенное значение, т.е. материальный баланс носит приближенный характер.
Материальный баланс составляют для процесса в целом или для отдельных его стадий.
Расчет материального баланса основан на 2 объективных законах:
1) закон сохранения массы
2) закон стехиометрических соотношений: если известна масса хотя бы одного участника реакции, можно определить массы всех остальных, предварительно рассчитав молярные массы всех участников реакции.
|
|
Сырье в реальных процессах, протекающих в промышленности, подается на взаимодействие с определенной долей примесей – это сырье называется техническим.
Материальный баланс может быть как в виде уравнения, так и в виде таблицы. В левой части – приход –записываются массы потоков сырья, поступающих на переработку, в правой части (расход) – массы потоков, прошедших переработку. Если процесс протекал в химическом реакторе, то после переработки в графе расход возможны следующие потоки:
1) целевой продукт;
2) побочные продукты;
3) непревращенный остаток сырья;
4) примеси, поступающие вместе с реагентами;
5) потери (сырья, продукта, указанных в исходных данных.)
При проектировании обычно задаются массой целевого продукта; массу сырья и массу побочных продуктов определяют по уравнению материального баланса.
На основании материального баланса рассчитываются расходные коэффициенты, определяются размеры аппаратов и устанавливаются оптимальные значения параметров технологического режима процесса.
Сравнивая фактические и теоретические расходные коэффициенты, можно сделать вывод о совершенстве процесса. Чем ближе эти значения, тем совершеннее производство.
Фактические расходные коэффициенты по сырью увеличиваются, если уменьшаются конверсия, селективность, увеличиваются потери, недостаточная очистка сырья.
Химико-технологические процессы связаны с затратой различных видов энергии – тепловой, механической, электрической. В основу энергетического баланса положен закон сохранения энергии, согласно которому в замкнутой системе сумма энергий всех видов постоянна. Поскольку в ХТ процессах тепловая энергия имеет наибольшее значение, для них обычно составляют тепловой баланс: приход тепла ΣQПPИX в данной технологической операции, равен расходу тепла ΣQPACX в той же операции.
|
|
ΣQПPИX = ΣQPACX
Тепловой баланс составляют по данным материального баланса с учетом тепловых эффектов химический реакций и физических превращений, протекающих в аппарате, учитывается теплосодержание веществ, участвующих в процессе, а также теплота подводимая в аппарат извне и выводимая из аппарата, тепловые потери в данной технологической операции.
Тепловые вклады в баланс рассчитывают по известным формулам.
Тепловой эффект химической реакции:
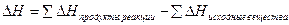
(значения энтальпии продуктов реакции и исходных веществ берутся из таблиц)
Теплосодержание веществ

где m – масса вещества,
c – его теплоемкость,
t – температура.
Теплоту фазовых переходов рассчитывают по формуле:
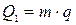
где q – удельная теплота соответствующего фазового перехода (испарения, конденсации, растворения, кристаллизации)
m – масса вещества.
Подвод и отвод теплоты в систему рассчитывают по потере тепла теплоносителем:
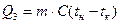
где m – масса теплоносителя,
С – теплоемкость теплоносителя,
tн tк – начальная и конечная температура теплоносителя.
И по формуле теплопередачи через стенку:

где КТ – коэффициент теплопередачи;
F – поверхность телообмена;
tт – температура теплоносителя, обогревающего аппарат;
tпр – температура подогреваемого продукта;
t – время.
Данные теплового баланса используются для определения расхода теплоносителя и хладоагента, расчета поверхности греющих и охлаждающих элементов и подбора оптимального теплового режима процесса.