Цели работы:
1. Ознакомиться с методом термического анализа.
2. Снять кривые охлаждения двухкомпонентных систем смесей различного состава.
3. Построить диаграмму плавкости в координатах температура-состав.
4. Провести анализ полученной диаграммы.
Теоретическая часть
Правило фаз Гиббса
Формулировка: число степеней свободы равновесной термодинамической системы равно числу независимых компонентов системы минус число фаз плюс число внешних факторов, влияющих на равновесие в данной системе (температура, давление, электрическое и магнитное поле, поле тяготения и т.д.).
Формула: 
Термический анализ
Изучение многокомпонентных систем, образующих несколько фаз, производится при помощи физико-химического анализа. Он широко применяется в химии и химической технологии при изучении гетерогенных систем в металлургии, технологии силикатов, при перегонке жидких смесей, минералогии и других областях науки и техники.
Физико-химический анализ основан на изучении функциональной зависимости между физическими свойствами химической равновесной системы и факторами, определяющими её равновесие. В качестве изучаемых физических свойств можно взять тепловые, электрические, оптические, механические и др. свойства систем. Полученные экспериментально зависимости физических свойств системы от её состава изображают в виде диаграмм состояния.
Изучение диаграмм состояния позволяет выяснить характер взаимодействия компонентов системы, а также судить о химическом составе и границах существования фаз и др.
Наиболее простым и распространённым методом физико-химического анализа является термический анализ. Представляет собой совокупность экспериментальных методов определения температуры, при которой в равновесной системе изменяется число фаз.
Одним из основных способов проведения термического анализа является построение кривых охлаждения.
Зависимость температуры системы от времени изображается непрерывной кривой 1 (рис.1).

На основании кривых охлаждения строятся диаграммы зависимости температуры того или иного фазового перехода от состава системы (рис.2).
Кривые, выражающие зависимость температуры кристаллизации и плавления от состава данной системы, называются диаграммами плавкости.

Если компоненты образуют идеальный раствор, то кривые ликвидуса будут подчиняться уравнению Шредера:
 .
.
И, наоборот, если значения теплоты плавления компонентов известны, то можно рассчитать зависимость температуры начала их кристаллизации от состава расплава, температуру кристаллизации эвтектики и её состав:
 .
.
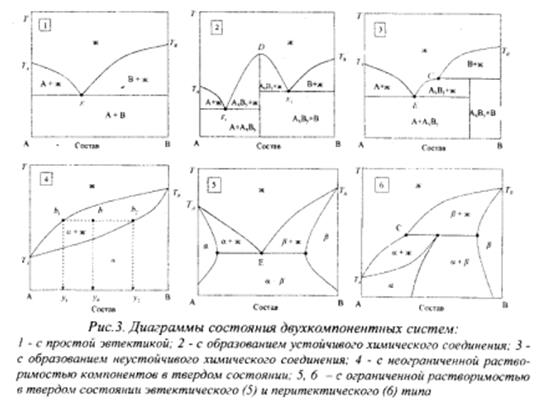
Диаграммы состояния двухкомпонентных систем
Диаграммы состояния двухкомпонентных систем подразделяются на три типа в зависимости от того, какая фаза выделяется из раствора.
В данной лабораторной работе используется первый тип диаграмм. Относятся системы, при кристаллизации которых из жидких растворов выделяются чистые твёрдые компоненты, так называемые неизоморфные смеси.
Соотношение между количествами твёрдой и жидкой фаз определяется по правилу рычага: отношение массы двух различных фаз обратно пропорционально отрезкам, на которые фигуративная точка делит линию, соединяющую составы фаз:
 .
.
Экспериментальная часть
Оборудование и реактивы
1. Пробирки со смесью дифениламина и нафталина различного состава, закрытые пробками. В отверстия пробок вставлены термометры со шкалой 150 – 2000С и проволочные мешалки.
2. Секундомер или часы с секундной стрелкой.
3. Электрическая плитка.
4. Штатив для пробирок.
5. Водяная баня.