КУРСОВАЯ РАБОТА
по дисциплине «Техническая термодинамика»
на тему: «Термодинамический расчет цикла парогазовой установки »
| Выполнил: студент группы ДТЕТБ-21/2 _______ Милосердов Н.Д. (Подпись) (Фамилия, И.О.) “____” _____________2017 | Руководитель: к.т.н., доц. Атдаев Д.И. ________________________ (Подпись) “____” _____________2017 | |
| Курсовая работы выполнена и защищена с оценкой ____________________________ (Оценка) Члены комиссии: ______________________________ Ильин Р.А. (Подпись) (Фамилия, И.О.) _______________________________________ (Подпись) (Фамилия, И.О.) “____” _____________2017 |
Астрахань 2017
АСТРАХАНСКИЙ ГОСУДАРСТВЕННЫЙ ТЕХНИЧЕСКИЙ УНИВЕРСИТЕТ
Кафедра Теплоэнергетика и холодильные машины
ЗАДАНИЕ
На выполнение курсовой работы
Студент: Милосердов Н.Д.
Дисциплина: «Техническая термодинамика»
Тема курсовой работы: «термодинамический расчет цикла парогазовой установки »
Исходные данные: Вариант 12

| Состав газовой смеси | |||
| СО2 | N2 | H2O | O2 |
Для газового цикла:
| Pa , бар | Pc , бар | Pd, бар |  , , 
|
Для парового цикла:
 , бар , бар
| 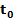 , , 
|  , бар , бар
|  , , 
|
| 0,055 |
Термодинамический расчет цикла ПГУ будет основываться на расчетах двух циклов: газового и пароводяного.
I. Газовый цикл
Цикл отнесен к 1 кг газовой смеси.
Требуется:
1. Определить параметры P,  , T для основных точек цикла.
, T для основных точек цикла.
2. Определить значения средних теплоемкостей 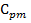 и
и  для каждого процесса.
для каждого процесса.
3. Найти изменения внутренней энергии (ΔU), энтальпии (Δi), энтропии (ΔS) в каждом процессе.
4. Определить теплоту (q) и работу (l) в каждом процессе.
5. Найти суммарную работу за цикл.
6. Определить подведенную  и отведенную
и отведенную 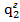 теплоты в цикле.
теплоты в цикле.
7. Определить термический к.п.д. газового цикла.
8. Построить в масштабе на ТS – диаграмме газовый цикл
II. Пароводяной цикл.
1. Определить с помощью iS – диаграммы и таблиц воды и водяного пара параметры P,  , T, i, U, S, Х для основных точек цикла.
, T, i, U, S, Х для основных точек цикла.
2. Определить кратность газа m из уравнения теплового баланса газоводяного подогревателя.
3. Определить удельную полезную работу пароводяного цикла 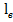 .
.
4. Определить теоретическое удельное количество теплоты, полученное рабочим телом,  .
.
5. Определить теоретический к.п.д. парогазового цикла.
6. Определить термический к.п.д. парогазового цикла.
7. Изобразить в масштабе циклы на Р 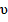 и ТS – диаграммах.
и ТS – диаграммах.
Дата получения задания «» 201 г
Срок предоставления курсовой работы: «» 201 г
Преподаватель: Атдаев Д.И. «» 201 г
Студент: Милосердов Н.Д. «» 201 г
ТЕРМОДИНАМИЧЕСКИЙ РАСЧЕТ ЦИКЛА
ПАРОГАЗОВОЙ УСТАНОВКИ
Цель выполнения курсовой работы по курсу «Техническая термодинамика» – углубление знаний по теории тепловых двигателей и расчету термодинамических процессов в газовых и пароводяных циклах, приобретение навыков использования справочной и учебной литературы, в частности, таблиц теплоемкостей различных газов, таблиц теплофизических свойств воды и водяного пара, а также hS – диаграммы водяного пара.
КРАТКИЕ ТЕОРЕТИЧЕСКИЕ СВЕДЕНИЯ
Парогазовые установки (ПГУ) являются типичными бинарными установками с коэффициентом заполнения цикла, приближающимся к единице. В ПГУ используется тепло продуктов сгорания топлива газотурбинных установок (ГТУ) для подогрева воды, парообразования и перегрева пара. Типичная принципиальная схема ПГУ изображена на рис.1.
Воздух, сжатый в компрессоре 1, подается в камеру сгорания парогенератора 2, работающего на газовом топливе. Часть тепла продуктов сгорания топлива идет на парообразование и перегрев пара. Теплота выхлопных газов после газовой турбины 3 используется для подогрева питательной воды паровой части установки в газоводяном подогревателе 4. Электроэнергия вырабатывается в двух генераторах, приводимых в действие паровой 5 и газовой 3 турбинами, часть мощности газовой турбины расходуется на привод компрессора 1, а часть мощности паровой турбины на привод насоса 7.

Рис.1.Принципиальная схема парогазовой установки:
1- компрессор; 2- парогенератор; 3- газовая турбина;
4- газоводяной подогреватель; 5- паровая турбина;
6- конденсатор; 7- водяной насос.
Термодинамический цикл ПГУ состоит из двух циклов – газового abcda и пароводяного 1234561, изображенных на рис.2.

Рис.2.Термодинамический цикл парогазовой установки.
I. ТЕРМОДИНАМИЧЕСКИЙ РАСЧЕТ ГАЗОВОГО ЦИКЛА
1. Расчет начинается с нахождения термических Р,  , T параметров в характерных точках цикла (a, b, c, d). Если в точке известно два из трех параметров, то третий находится из уравнения состояния идеального газа (уравнение Клапейрона – Менделеева).
, T параметров в характерных точках цикла (a, b, c, d). Если в точке известно два из трех параметров, то третий находится из уравнения состояния идеального газа (уравнение Клапейрона – Менделеева).
Так как в качестве рабочего тела используется смесь идеальных газов, то необходимо сначала найти газовую постоянную смеси газов.
Если в данной точке известен один параметр, то исходя из уравнения соответствующего процесса, например,  =
=  адиабатного, можно найти второй параметр и т.д. Если в исследуемой точке неизвестен ни один из параметров, то необходимо из рис.3, определить один или два параметра, а затем расчет провести, как сказано выше. Полученные данные занести в таблицу 1.
адиабатного, можно найти второй параметр и т.д. Если в исследуемой точке неизвестен ни один из параметров, то необходимо из рис.3, определить один или два параметра, а затем расчет провести, как сказано выше. Полученные данные занести в таблицу 1.
Таблица 1.1.Параметры газового цикла.
| Точка/Параметры | P, бар | υ,  /кг /кг
| T, K | t, 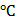
| 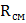 , , 
|
2. Средняя массовая изобарная теплоемкость смеси газов для каждого процесса находится по формуле:
 n
n 
 =
= 

 i= 1
i= 1 
где  - массовая доля i – ого компонента газовой смеси;
- массовая доля i – ого компонента газовой смеси;

 - средняя массовая изобарная теплоемкость i-го компонента в интервале температур от
- средняя массовая изобарная теплоемкость i-го компонента в интервале температур от  до
до  , определяемая по формуле:
, определяемая по формуле:

 =
= 

 - средняя массовая изобарная теплоемкость i-го компонента при данной температуре, которую можно найти в таблице 2. Если в таблице нет вашего значения
- средняя массовая изобарная теплоемкость i-го компонента при данной температуре, которую можно найти в таблице 2. Если в таблице нет вашего значения  или
или  , то нужно произвести интерполяцию, т.е. найти промежуточное значение величины данной таблицы по некоторым известным значениям.
, то нужно произвести интерполяцию, т.е. найти промежуточное значение величины данной таблицы по некоторым известным значениям.
Таблица 2.Средняя массовая теплоемкость различных газов  .
.

| 
| 
| 
| CO | 
| 
| 
| воздух |
| 0,9148 | 1,0392 | 14,195 | 1,0396 | 0,8148 | 0,607 | 1,8594 | 1,0036 | |
| 0,9232 | 1,0404 | 14,352 | 1,0417 | 0,8658 | 0,636 | 1,8728 | 1,0061 | |
| 0,9353 | 1,0434 | 14,421 | 1,0463 | 0,9102 | 0,662 | 1,8937 | 1,0115 | |
| 0,9500 | 1,0488 | 14,448 | 1,0538 | 0,9487 | 0,687 | 1,9192 | 1,0191 | |
| 0,9651 | 1,0567 | 14,477 | 1,0634 | 0,9826 | 0,708 | 1,9477 | 1,0283 | |
| 0,9793 | 1,0660 | 14,509 | 1,0748 | 1,0128 | 0,724 | 1,9778 | 1,0387 | |
| 0,9927 | 1,0760 | 14,542 | 1,0861 | 1,0396 | 0,734 | 2,0092 | 1,0496 | |
| 1,0048 | 1,0869 | 14,587 | 1,0978 | 1,0639 | 0,754 | 2,0419 | 1,0605 | |
| 1,0157 | 1,0974 | 14,641 | 1,1091 | 1,0852 | 0,762 | 2,0754 | 1,0710 | |
| 1,0258 | 1,1076 | 14,706 | 1,1200 | 1,1045 | 0,775 | 2,1097 | 1,0815 | |
| 1,0350 | 1,1179 | 14,776 | 1,1304 | 1,1225 | 0,783 | 2,1436 | 1,0907 | |
| 1,0434 | 1,1271 | 14,853 | 1,1401 | 1,1384 | 0,791 | 2,1771 | 1,0999 | |
| 1,0509 | 1,1359 | 14,934 | 1,1493 | 1,1530 | 0,795 | 2,2106 | 1,1082 | |
| 1,580 | 1,1447 | 15,023 | 1,1577 | 1,1660 | - | 2,2429 | 1,1166 | |
| 1,0647 | 1,1526 | 15,202 | 1,1656 | 1,1762 | - | 2,2743 | 1,1242 | |
| 1,0714 | 1,1602 | 1,1731 | 1,1895 | - | 2,3048 | 1,1313 |
Например, найдем теплоемкость кислорода при температуре 170 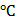 . Так как значения температуры 170
. Так как значения температуры 170 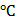 в таблице нет, то выпишем ближайшие значения:
в таблице нет, то выпишем ближайшие значения:
100 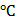
 = 0,9232
= 0,9232 
200 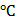
 = 0,9353
= 0,9353 
Теперь проинтерполируем между этими значениями:
170 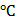 100
100 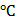
 =
=  +
+ 
 70 = 0,9232 +
70 = 0,9232 + 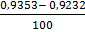
 70 = 0,9317
70 = 0,9317 
0 0
Среднюю массовую изохорную теплоемкость можно найти по формулам термодинамических процессов:
Адиабатный; 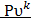 = const, S=const, dq=0:
= const, S=const, dq=0:  Из уравнения Майера:
Из уравнения Майера: 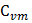 =
=  –
– 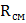
Изохорный;  =const: Из уравнения Майера:
=const: Из уравнения Майера: 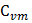 =
=  –
– 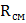
Изотермический; T=const: 
Изобарный; P=const:  =
=  –
– 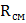
Политропный;  =const:
=const:  =
=  –
– 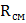
3. Изменения внутренней энергии ΔU и энтальпии Δi для каждого процесса цикла рассчитываются по формулам:
Δ  =
=  (
( –
–  ); Δ
); Δ  =
=  (
( –
–  )
)
Изменение энтропии ΔS для каждого процесса цикла можно найти из следующих формул:
Для адиабатного: Δ  = 0
= 0 
Для изохорного: Δ  =
=  ln
ln  =
=  ln
ln 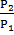
Для изотермического Δ  =
= 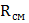 ln
ln  =
= 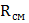 ln
ln 
Для изобарного: Δ  =
=  ln
ln  =
= 
Для политропного: Δ  =
=  ln
ln  =
= 
Т.к. U, i и S являются функциями состояния, то за весь цикл:
n
 i=1
i=1
|
n
 0
i=1 0
i=1
|
 ;
;
i=1
4. Теплота и работа в каждом процессе определяются по следующим формулам:
Адиабатный:  = 0;
= 0; 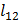 = - Δ
= - Δ 
Изохорный:  = Δ
= Δ  =
=  (
( –
–  );
); 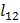 = 0
= 0 
Изотермический:  =
= 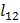 =
= 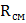 T ln
T ln  =
=  T ln
T ln 
Изобарный:  =
=  =
=  (
( –
–  );
); 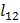 = P (
= P ( -
- 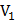 )
)
Политропный:  =
= 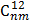 (
( –
–  ), где
), где  =
=  ;
;
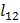 =
=  (
( )
)  =
=  (
( –
–  )
)
Таблица 1.2. Результаты расчета газового цикла
| Процессы | n | 
| 
| Δ 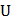 , ,

| Δ 

| Δ 

| q, 
| l, 
| |

| |||||||||
| a-b | |||||||||
| b-c | |||||||||
| c-d | |||||||||
| d-a | |||||||||

| |||||||||
5. Определим подведенную (в процессе расширения рабочего тела) теплоту  и отведенную (в процессе сжатия) теплоту
и отведенную (в процессе сжатия) теплоту  и суммарную работу за цикл с учетом правила знаков для работы (работа расширения положительна, сжатия – отрицательна).
и суммарную работу за цикл с учетом правила знаков для работы (работа расширения положительна, сжатия – отрицательна).
 =
= 
 =
=  –
– 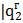 |
|
 =
= 

 =
= 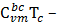

Согласно первому закону термодинамики для цикла:  =
= 
6. Термический к.п.д. цикла:
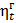 =
= 
 =
= 
7. Изобразим на ТS - диаграмме, в масштабе, газовый цикл. Первая точка строится полу произвольно, по оси ординат откладываем температуру  , а по оси абсцисс точку откладываем произвольно. Дальнейшие точки строятся строго в соответствии со значениями температур и ΔS для каждого процесса.
, а по оси абсцисс точку откладываем произвольно. Дальнейшие точки строятся строго в соответствии со значениями температур и ΔS для каждого процесса.
II. ТЕРМОДИНАМИЧЕСКИЙ РАСЧЕТ ПАРОВОДЯНОГО ЦИКЛА
1. Определяем с помощью iS – диаграммы и таблиц воды и водяного пара термические p,  , T и калорические i, U, S параметры в характерных точках цикла и заносим их в таблицу 3.
, T и калорические i, U, S параметры в характерных точках цикла и заносим их в таблицу 3.
Таблица 3. Параметры пароводяного цикла
| Точка/Параметры | P, бар | V,  /кг /кг
| t, 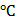
| 

| 

| 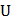 , ,

| X |
2. Определяем кратность газа m из уравнения теплового баланса для газоводяного подогревателя 4, в котором процесс 4-5 нагрева питательной воды до состояния кипения осуществляется за счет теплоты отработавших газов газового цикла (процесс b-c):
m  =
=  m =
m = 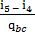
3. Удельная полезная работу ( ) пароводяного цикла:
) пароводяного цикла:  =
= 
4. Теоретическое удельное количество теплоты ( ), полученное рабочим телом:
), полученное рабочим телом:
 =
= 
5. Определим теоретический к.п.д. парогазового цикла.  =
= 
Для пароводяного цикла  = 1 – T1/T2
= 1 – T1/T2
6. Определим термический к.п.д. парогазового цикла.

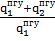 ;
;  =
=  +
+ 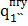 ;
;  =
=  +
+  ;
; 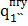 =
=  ;
; 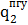 =
=  =
= 
Вариант 12
I. Расчет газового цикла:
1). Определим параметры рабочего тела (р, υ, T) для основных точек цикла.
| a |
| b |
| c |
| d |
| P |
| V |
| dq=0 |
| P=const |
| T=const |
Определяем газовую постоянную смеси,
 =
=  ; R=
; R=  ; где k=8314,2,
; где k=8314,2, 
 =
=  = 138,57
= 138,57 
 =
= 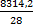 = 319,78
= 319,78 
 =
= 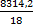 = 461,9
= 461,9 
 =
=  = 259,8
= 259,8 
rCO 2 = 0,16; rCO 2 = 0,75; rCO 2 = 0,05; rCO 2 = 0,04
 = 1 / ((0,16/189) + (0,75/292,75) + (0,05/461,9) + (0,04/259,82)) =
= 1 / ((0,16/189) + (0,75/292,75) + (0,05/461,9) + (0,04/259,82)) =
= 272,04 
Точка a:
Pa = 6*105 Па
ta = td = 149,2 oC = 422,35 K
υa = (Rсм/Ta)/Pa = (272,04/422,35)/6*105 = 0,1912 м3/кг
Точка b:
Рb = Рс = 4*105 Па
υb = υa/(Pb/Рa)1/k = 0,191/(4*105/6*105) = 0,26 м3/кг
tb = (Pb* υb)/ Rсм = (4*105 * 0,26)/272,04 = 381,93 K = 108,8 oC
Точка c:
Pc = 4*105 Па
tc = 100 oC = 373,15 K
υc = (Rсм * tc)/ Pc = (273,04*373,15)/4*105 = 0,25 м3/кг
Точка d:
Рd = 7*105 Па
υd = υс/(Pd/Рc)1/k =0,25/(7*105/4*105) = 0,164 м3/кг
td = (Pd* υd)/ Rсм = (7*105 *0,164)/272,04 = 422,35 K = 149,2 oC
Результаты расчета заносим в табл. 1.1.
Таблица 1.1. Параметры газового цикла
| Точка/Параметры | P, бар | υ,  /кг /кг
| T, K | t, 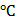
|  , , 
|
| a | 0,1912 | 422,35 | 149,35 | 272,04 | |
| b | 0,26 | 381,93 | 108,8 | 272,04 | |
| c | 0,25 | 373,15 | 272,04 | ||
| d | 0,164 | 422,35 | 149,35 | 272,04 |
2). Определим значения средних теплоемкостей  и
и  для каждого процесса.
для каждого процесса.
Процесс a-b: адиабатный;  = const, S=const, dq=0
= const, S=const, dq=0
 n
n 
 =
= 
 , значения
, значения  при данной температуре находим по
при данной температуре находим по
 i= 1
i= 1 
линейной интерполяции по таблице средних массовых теплоемкостей различных газов.
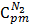 =
=  =
=  =
=  =
=
=1,0454 
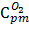 =
=  =
= 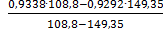 =
=  =
=
=0,91686 
 =
=  =
= 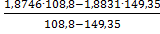 =
=  =
=
=1,906 
 =
= 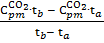 =
= 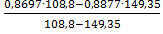 =
=  =
=
=0,936 
 = 0,698;
= 0,698;  = 0,042;
= 0,042; 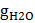 = 0,03;
= 0,03;  = 0,231
= 0,231
 =
=  +
+  +
+  +
+  = 1,0454
= 1,0454  + 1,906
+ 1,906 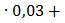 0,93
0,93  1,0416
1,0416 
 =
=  –
–  = 1041,6 – 272,04 = 768,35
= 1041,6 – 272,04 = 768,35 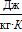 =0,77
=0,77 
Процесс b-c: изобарный; P =const
 =
=  =
=  =
=  = 1,0088
= 1,0088 
 =
=  =
=  =
=  =
=
= 1,0542 
 =
=  =
=  =
=  =
=
= 1,895 
 =
=  =
=  =
=  = 0,914
= 0,914 
 =
=  +
+  +
+  +
+  = 1,0088
= 1,0088  + 1,895
+ 1,895 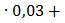 0,914
0,914  = 1,0164
= 1,0164 
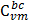 =
=  –
–  = 1016,4 – 272,04 = 744,363
= 1016,4 – 272,04 = 744,363 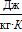 = 0,74
= 0,74 
Процесс c-d: адиабатный;  = const, S=const, dq=0
= const, S=const, dq=0
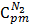 =
=  =
=  =
=  =
=
=1,0388 
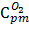 =
=  =
=  =
=  =
=
=0,9413 
 =
=  =
=  =
=  =
=
=1,904 
 =
= 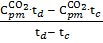 =
=  =
=  =
=
=0,9321 
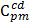 =
=  +
+  +
+  +
+  = 1,0388
= 1,0388  + 1,904
+ 1,904 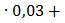 0,9321
0,9321  1,037
1,037 
 =
= 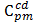 –
–  = 1037,05 – 272,04 = 765,01
= 1037,05 – 272,04 = 765,01 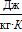 =0,765
=0,765 
Процесс d-a: изотермический; T=const
При t = 149,35 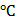 :
:
 = 1,0419
= 1,0419 
 = 0,9292
= 0,9292 
 = 1,8831
= 1,8831 
 = 0,8877
= 0,8877 
 =
=  +
+  +
+  +
+  = 1,0
= 1,0 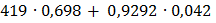 + 1,8831
+ 1,8831 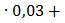 0,8877
0,8877 

 =
= 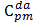 –
–  = 1027,8 – 272,04 = 755,78
= 1027,8 – 272,04 = 755,78  = 0,755
= 0,755 
3). Найдем изменения внутренней энергии (ΔU), энтальпии (Δi), энтропии (ΔS) в каждом процессе.
Процесс a-b: адиабатный;  = const, S=const, dq=0
= const, S=const, dq=0
Δ