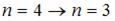| A)Полосатые спектры характерны для…
B) Линейчатые спектры характерны для…
| атомарных газов
жидкостей
твердых тел
молекулярных газов
|
| Выберите верные утверждения:
| 1. состояние электрона в атоме характеризуется тремя квантовыми числами;
2. принцип Паули справедлив только для фермионов;
3. магнитное спиновое квантовое число может иметь только два значения 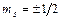 . .
|
| Выберите верные утверждения:
| 1. инверсная населенность – это такое заполнение электронами энергетических уровней, при котором нарушается принцип Паули;
2. инверсная населенность – это состояние, при котором возбужденных атомов в веществе больше, чем невозбужденных;
3. когерентность лазерного излучения обусловлена индуцированными переходами.
4. когерентность лазерного излучения обусловлена спонтанными переходами.
|
При переходах электрона в атоме с одного уровня на другой закон сохранения момента импульса накладывает определенные ограничения (правило отбора). В энергетическом спектре атома водорода запрещенным переходом является...
A)  B) B)  C)
C) 
| A)
3s-2s
3p-2s
4f-3d
4s-3р
B)
3s-2s
3d-2p
3s-2p
4s-3p
C)
4s-3р
2р-1s
3d-2p
4d-2s
| |
На рисунке изображены стационарные орбиты атома водорода согласно модели Бора, а также переходы электрона с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой - серию Бальмера, в инфракрасной - серию Пашена.
 Наибольшей частоте кванта в серии Лаймана соответствует переход...
Наибольшей частоте кванта в серии Лаймана соответствует переход...
|
n = 2 → n = 1
n = 5 → n = 3
n = 3 → n = 2
n = 5 → n = 1
| |
На рисунке дана схема энергетических уровней атома водорода, а также условно изображены переходы электрона с одного уровня на другой, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой области – серию Бальмера, в инфракрасной области – серию Пашена и т.д.  Отношение максимальной частоты линии в серии Пашена Отношение максимальной частоты линии в серии Пашена  к минимальной частоте линии в серии Бальмера к минимальной частоте линии в серии Бальмера 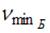 равно … равно …
|
|
Собственные функции электрона в атоме водорода  содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Орбитальное квантовое число l определяет содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Орбитальное квантовое число l определяет
| |
| 1.модуль орбитального момента импульса электрона
| |
| 2.энергию электрона в атоме водорода
| |
| 3.проекцию орбитального момента импульса
электрона на некоторое направление
| |
| 4.модуль собственного момента импульса электрона
|
|
На рисунке дана схема энергетических уровней атома водорода.  Наибольшая длина волны спектральной линии (в нм) серии Лаймана равна …(h = 6,63·10-34 Дж·с) Наибольшая длина волны спектральной линии (в нм) серии Лаймана равна …(h = 6,63·10-34 Дж·с)
|
|
На рисунке схематически изображены стационарные орбиты электрона в атоме водорода согласно модели Бора, а также показаны переходы электрона с одной стационарной орбиты на другую, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой – серию Бальмера, в инфракрасной – серию Пашена.  Наибольшей частоте кванта в серии Пашена (для переходов, представленных на рисунке) соответствует переход … Наибольшей частоте кванта в серии Пашена (для переходов, представленных на рисунке) соответствует переход …
|
|
На рисунке изображена схема энергетических уровней атома водорода. Показаны состояния с различными значениями орбитального квантового числа. Запрещенными правилом отбора для орбитального квантового числа являются переходы…

| 
|
Собственные функции электрона в атоме водорода 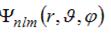 содержат три целочисленных параметра n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным и магнитным квантовыми числами соответственно. Магнитное квантовое число m определяет… содержат три целочисленных параметра n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным и магнитным квантовыми числами соответственно. Магнитное квантовое число m определяет…
| 1.модуль орбитального момента импульса электрона
2.проекцию орбитального момента импульса электрона на некоторое направление
3.модуль собственного момента импульса электрона
4.энергию электрона в атоме водорода
|
На рисунке дана схема энергетических уровней атома водорода, а также условно изображены переходы электрона с одного уровня на другой, сопровождающиеся излучением кванта энергии. В ультрафиолетовой области спектра эти переходы дают серию Лаймана, в видимой области – серию Бальмера, в инфракрасной области – серию Пашена и т. д. Отношение минимальной частоты серии Лаймана к максимальной частоте серии Бальмера равно…

|
5,4
7,2
|
На рисунке изображена схема энергетических уровней атома водорода. Показаны состояния с различными значениями орбитального квантового числа. Серию Бальмера дают переходы…

| 
|
| | | | |
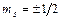 .
.
 B)
B)  C)
C) 
 Наибольшей частоте кванта в серии Лаймана соответствует переход...
Наибольшей частоте кванта в серии Лаймана соответствует переход...
 Отношение максимальной частоты линии в серии Пашена
Отношение максимальной частоты линии в серии Пашена  к минимальной частоте линии в серии Бальмера
к минимальной частоте линии в серии Бальмера 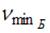 равно …
равно …
 содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Орбитальное квантовое число l определяет
содержат три целочисленных параметра: n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным (азимутальным) и магнитным квантовыми числами соответственно. Орбитальное квантовое число l определяет
 Наибольшая длина волны спектральной линии (в нм) серии Лаймана равна …(h = 6,63·10-34 Дж·с)
Наибольшая длина волны спектральной линии (в нм) серии Лаймана равна …(h = 6,63·10-34 Дж·с)
 Наибольшей частоте кванта в серии Пашена (для переходов, представленных на рисунке) соответствует переход …
Наибольшей частоте кванта в серии Пашена (для переходов, представленных на рисунке) соответствует переход …


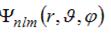 содержат три целочисленных параметра n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным и магнитным квантовыми числами соответственно. Магнитное квантовое число m определяет…
содержат три целочисленных параметра n, l и m. Параметр n называется главным квантовым числом, параметры l и m – орбитальным и магнитным квантовыми числами соответственно. Магнитное квантовое число m определяет…