Минеральные вещества, соли, ионы.
Большая часть неорганических веществ в клетке, находится в виде солей:
- либо диссоциированных на ионы
- либо в твёрдом состоянии.
Среди диссоциированных имеют большое значение катионы: К, Na, Са, Mg 2+,NH3 +, анионы CI, NO3, угольной, фосфорной кислот. По солевому составу вне - и внутриклеточные жидкости резко отличаются: в клетках высоко содержание К, Mg и фосфатов, вне клеток - Na, Ca, Cl. Концентрация калия внутри клетки очень высокая, а натрия – низкая. В окружающей среде наоборот. В мышечных клетках калия в 30 раз выше, чем в крови, и наоборот, содержание натрия в 10 раз ниже, чем в окружающей среде. Повышение содержания калия снаружи клетки оказывает токсичное действие на сердечную и другие мышцы. Пока клетка жива, эти различия в концентрации калия и натрия между клеткой и межклеточной средой стойко удерживаются работой мембранных насосов (Na+ - K+ насос).
Внутри клеток ионы также распределены неравномерно: Na больше в ядре, чем в цитоплазме, а Ca больше в митохондриях. В организме имеются солевые депо – в костной ткани находится в основном Ca, в печени могут депонироваться ряд ядовитых микроэлементов свинец, мышьяк, а затем удаляются в виде безвредных белковых органических соединений. У млекопитающих основным органом регуляции баланса солей и воды служат почки.
Ионная асимметрия обеспечивает:
· трансмембранный потенциал,
· раздражимость, ответные реакции организмов в форме тропизмов, таксисов, рефлексов
· проницаемость клеточных мембран
Ионы обеспечивают также сцепление клеток между собой и упорядоченное их расположение в тканях, (межклеточный кальций входит в состав «цемента»)
От концентрации солей внутри клетки зависят:
|
|
· 1. буферные свойства клетки,
· 2. осмотическое давление - в клетках наземных – 8 атм, морских беспозвоночных 38 атм, растительных клетках от 5 – до 20 атм, Осмотическое давление жидкостей организма человека и большинства, млекопитающих равно давлению 0,85 % - 0,9 % раствора хлорида натрия NaCI. Растворы с таким давлением называются и з о т о н и ч е с к и м и, более концентрированные – г и п е р т о н и ч е с к и е, а менее концентрированны – г о п о т о н и ч е с к и м и.
Величина осмотического давления возрастает с увеличением концентрации раствора.
· 3. поступление воды в клетку,
· 4. поддерживается форма, объём клеток,
· 5. обеспечивается работа нервных и мышечных клеток.
· 6. накопление воды в тканях.
Изменение их концентрации может вызвать определённые нарушения. Например, снижение содержания кальция в крови млекопитающих вызывает судороги и смерть.
Для работы сердечной мышцы необходимо определённое соотношение Na, K, Ca. При изменении баланса этих ионов работа сердечной мышцы нарушается.
Буферность - это способность клетки поддерживать слабощелочную реакцию своего содержимого на постоянном уровне, т.е. способность клетки сохранять определённую концентрацию водородных ионов (рН) Буферные растворы характеризуются тем, что внесение в них или образование в процессе обмена веществ небольших количеств кислоты или щелочи не влияет на значение рН вследствие образования соединений с карбонатами, фосфатами или неорганическими кислотами.
Анионы слабых кислот и щелочей связывают ионы водорода и гидроксила, благодаря чему кислотно-щелочное равновесие внутри клетки практически не меняется.
|
|
Внутри клетки буферность обеспечивается главным образом анионами фосфорной кислоты (Н2РО -, НРО42-) – фосфатная буферная система рН 6,9.
Во внеклеточной жидкости в крови роль буфера играют анионы угольной кислоты (Н2СО3 и НСО3-),
создают рН 7,4.
Нерастворимые минеральные соли, например, фосфорнокислый и углекислый кальций входят в состав межклеточного вещества костной ткани, раковин моллюсков, обеспечивая их прочность. Причём прочность и твёрдость костной ткани обеспечивается фосфатом Ca, а раковин моллюсков – карбонатом Ca.
ВОДА
ВОДА – это универсальная дисперсионная среда живой материи. Вода химическое соединение водорода с кислородом. В природе вода встречается не в чистом виде, и всегда содержит различные органические и неорганические соединения. Вода, выпадающая в виде осадков, содержит вещества, которые уносит из атмосферы. В поверхностных и подземных, пресных водах количество растворённых солей не превышает 1 -1,5 г/л, при большем их содержании вода называется минеральной. В морской воде в среднем содержится 35 г/л солей. Вода является не только необходимым компонентом живых клеток, но и для многих средой обитания. Поступает в организм из внешней среды, у животных может образовываться при расщеплении жиров, углеводов, белков.
В тканях живых организмов на долю воды приходится 70 – 80%. Вода самое простое химическое соединение, входящие в состав живых организмов. По количественному содержанию в протоплазме она стоит на первом месте. Например, вода составляет 95 % массы медузы, бактерий 76 – 86 %. Около 2\3 – 60% массы человека приходится на воду. Внутриклеточная вода составляет около – 40%, межклеточная жидкость – 16%, внутрисосудистая 4,5 %
|
|
В зависимости от функциональной активности тканей количество воды в них различно:
· Эмбриональные клетки содержат - 90 95 %
· Клетки молодого организма – 80 %
· Клетки стареющего организма – 60 %
· Серое вещество мозга – 86 %
· Белое вещество мозга – 75 %
· Клетки почек – 83 %
· Клетки печени – 70 %
· В мышцах сердца – 79 %
· Наименьшее количество воды в: костях – 22 %, эмали зубов – 10 %, клетках семян
При снижении интенсивности обмена количество воды уменьшается, поэтому можно провести параллелизм между интенсивностью обмена веществ и содержанием воды в органах и тканях. Так же с возрастом её содержание снижается.
Интенсивность обновления воды в организме зависит от условий окружающей среды, к обитанию в которой приспособлен данный вид. Обновление воды, равное объёму организма у амёбы, осуществляется за 1 неделю, у человека – за 1 месяц, у черепахи – за 1 год, у кактуса – за 29 лет.
Вода в клетке находится в двух формах: связанной и свободной.
Связанная вода. На её долю приходится 4-5 % её массы.
Различают две формы связанной воды – г и д р а т а ц и о н н у ю и о б м е н н у ю.
Связанная вода не вытекает из клеток при их повреждении.
Гидратационная вода. Её составляют те молекулы воды, которые водородными связями прочно соединены с молекулами белков. Мельчайшие частицы веществ, окружённых молекулами воды, образуют коллоидные растворы – это цитоплазма, кариоплазма, межклеточные жидкости. В коллоидном растворе различают непрерывную фазу – дисперсионную среду (вода) и коллоидные частицы – дисперсную фазу. Коллоидной частицей протоплазмы чаще всего являются молекулы белка, т.к. их размеры соответствуют размерам коллоидных частиц.
Вокруг белка в коллоидном растворе образуются водные или с о л ь в а т н ы е (от лат. solvare - распускать) оболочки. Сольватная связанная вода прочно удерживается коллоидными частицами белков. Молекулы воды, создавая оболочки вокруг белков, препятствуют образованию крупных частиц. Такое состояние называется д и с п е р с н ы м (рассеянным, раздробленным).
Дисперсность (степень раздробленности) обратно пропорциональна размерам коллоидных частиц d = 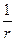 , где d - дисперсность, r – размер коллоидной частицы. Коллоидные частицы как бы взвешены в дисперсионной среде, где создаётся огромная поверхность, на которой происходит оседание, адсорбция веществ поступающих в клетку и течение разнообразных биохимических реакций.
, где d - дисперсность, r – размер коллоидной частицы. Коллоидные частицы как бы взвешены в дисперсионной среде, где создаётся огромная поверхность, на которой происходит оседание, адсорбция веществ поступающих в клетку и течение разнообразных биохимических реакций.
Коллоидные растворы бывают в двух состояниях: в виде золя ( растворённый) и геля ( студень, более вязкий ).
В состоянии гель вытянутые белковые молекулы, соприкасаясь, друг с другом образуют остов из сетки, заполненный жидкостью.
Когда белковые молекулы (коллоидные частицы) расходятся, коллоид переходит в золь. Эти процессы обратимы и в клетке совершаются непрерывно. При сокращении мышцы золь быстро переходит в гель и наоборот. При образовании псевдоподий у амёбы наблюдается переход геля в золь.
Такой переход из одного состояния в другое можно наблюдать на растворе желатина, который при нагревании - жидкий (золь), а при остывании становится студнеобразным (гель).
Коллоидное состояние определяет вязкость. Вязкость повышается, а дисперсность уменьшается, например, при повреждении клеток, размеры коллоидных частиц укрупняются, за счёт набухания и их агрегации. В яйцеклетках при оплодотворении так же повышается вязкость.
Обменная вода. Она находится между молекулами белка, мембранами, волокнами.
Особенностями связанной воды являются то, что она не растворяет солей, замерзает при температуре близкой к минус - 400 С.
Функции связанной воды:
1. Изолирует белковые молекулы друг от друга;
2. Препятствует агрегации белковых молекул;
3. Способность образовывать коллоидные структуры цитоплазмы
4. Определяет конформацию и функциональную активность ферментов
5. Обеспечивает пространственную организацию и активность структурных белков клеточных мембран
6. Влияет на структурную организацию и функции органоидов.
Свободная вода.
Основная масса около 95 % воды в клетке находится в свободном состоянии. Она входит в состав протоплазмы, вакуолей, кариоплазмы ядра, межклетниках: плазмы крови, тканевой жидкости, лимфы, ликвора (спинномозговой жидкости), находится в моче, поте, слезах. Содержится в соках желудочно-кишечного тракта: слюне, желудочном соке, соке поджелудочной железы, кишечном соке. Свободная вода вытекает из клеток при их повреждении.
Большое биологическое значение имеют физические свойства воды, обусловленные: размерами молекул воды, их формой и асимметричным строением её молекулы, определяющей полярность. Молекула воды электронейтральна. В ней центры тяжести положительных и отрицательных зарядов не совпадают, поэтому молекула воды является маленьким постоянным электрическим д и п о л е м. Так как центры положительных (+) и отрицательных (-) зарядов не совпадают, а разнесены в пространстве.

 Н+ Н+
Н+ Н+
 2 - О Н+ ------ 2 - О
2 - О Н+ ------ 2 - О
 водородная
водородная
связь
Н+
Физические свойства воды:
· 1. Высокая удельная теплоёмкость. Теплоёмкость водыв 4 раза превышает теплоёмкость воздуха. Это означает, что при изменении температуры воды на 1 0 выше или ниже она должна забрать или отдать большое количество энергии. Объясняется это образованием водородных связей между молекулами воды. Например, большое количество тепловой энергии, сообщённой воде, очень незначительно повышает её температуру. Происходит это потому, что большое количество энергии тратится на разрыв водородных связей между молекулами воды. При этом температура в клетке поддерживается на относительно постоянном уровне. Например, если температура окружающей среды ниже температуры тела, то в клетке возникают ассоциации из молекул воды, возникают между ними водородные связи, выделяется тепло и в клетке сохраняется постоянная температура. При повышении температуры окружающей среды часть тепловой энергии затрачивается на разрыв водородных связей между молекулами воды, при этом температура внутренней среды практически не меняется. Поэтому высокая теплоёмкость воды поддерживает тепловой баланс термостабильность в организме. Это очень важно, так как позволяет организмам содержать воду или обитать в воде в широком диапазоне температур. Благодаря высокой удельной теплоёмкости воды, колебания температуры в окружающей среде не сильно вредят биохимическим реакциям, протекающим в клетке, и они происходят в меньшем интервале температур, с более постоянной скоростью и опасность нарушения этих процессов не очень высока.
· 2. Теплопроводность – это скорость передачи тепла. Теплопроводность водызначительно выше в 5 раз по сравнению с другими жидкостями, выше, чем у воздуха в 10 раз, но меньше в 1000 раз по сравнению с металлами. Воздух плохой проводник тепла (воздушная прослойка защищает организм от перегрева и охлаждения), как и вода. Благодаря низкой теплопроводности воды организм медленно теряет или поглощает тепло. Поэтому при низких температурах не так быстро переохлаждается, и не перегревается в жару. Теплопроводность воды и кровообращение дают возможность равномерно распределять тепло между тканями тела.
· 3. Высокая теплота образования и низкая температура замерзания. Это так же объясняется существованием водородных связей между молекулами воды. Температура кипения воды выше, чем у многих других веществ. Для испарения воды необходима большая энергия. Таким образом, испарение сопровождается охлаждением организма, что предохраняет организм от перегрева. Это явление у животных используется при потоотделении, при тепловой одышке у млекопитающих и некоторых рептилий, например, крокодилов, которые сидят на солнце, открыв рот. У растений этот процесс осуществляется за счёт - т р а н с п и р а ц и и – испарения воды листьями. Это свойство воды предохраняет организм от перегрева.
Чтобы замёрзнуть, вода должна отдать большое количество энергии, что сильно снижает возможность образования льда внутри клеток.Кристаллы льда губительны для живого, когда они образуются внутри клеток.
Благодаря этим особенностям вода с минимальными изменениями собственной температуры хорошо предохраняет протоплазму от резких изменений температуры, обеспечивает равномерное распределение тепла в клетке и во всём организме, а также дают возможность значительно охладиться при минимальной потере воды.
· 4. Вода является хорошим растворителем. Дипольным свойством молекулы воды объясняется её способность ориентироваться в электрическом поле, присоединяться к различным молекулам и участкам молекул (благодаря полярности молекул веществ), несущим заряд. В результате чего образуются гидраты. Способностью воды образовывать гидраты, обусловливают её универсальные растворяющие свойства. Вода растворяет полярные молекулы других веществ. Если энергия притяжения молекул воды к молекулам какого-либо вещества больше, чем энергия притяжения между молекулами воды, то вещество растворяется.
Вещества растворимые в воде, называются гидрофильными, так как имеют функциональные полярные группировки, отличающиеся гидрофильностью, т.е. способностью молекул воды образовывать с ними водородные связи: к ним относятся соли, кислоты, щёлочи, спирты, моно и дисахариды, газы. В водном растворе поступают вещества в клетку и выводятся многие продукты жизнедеятельности. Соли в водном растворе распадаются на ионы. На примере молекулы NaCI можно отметить, что диполи воды, окружающее положительный ион Na, обращены к нему отрицательными полюсами, а к отрицательному иону CI – положительными. Происходит электрическая диссоциация веществ, такой раствор проводит электрический ток. Тогда как бессолевой раствор – би- или дистиллированная вода электрический ток не проводят.
Нерастворимые – гидрофобные (неполярные – жиры, масла, жироподобные вещества – витимины: А,Д,Е,К, гормоны – коры надпочечников – гидрокортизон, половые – андрогены(муж), эстрогены(жен), фосфолипиды входящие в состав мембранных структур; органические растворители – бензол, эфир; полисахариды – крахмал, гликоген). Неполярные части молекул отталкиваются водой и не смешиваются с водой, образуя при встряхивании эмульсии. Например, липиды могут разделять водные растворы на отдельные зоны, отсеки, подобно тому, как их разделяют мембраны. Гидрофобные взаимодействия обеспечивают стабильность мембран, белковых молекул, нуклеиновых кислот. В присутствии воды неполярные молекулы притягиваются друг к другу, например, как мелкие капельки масла сливаются в более крупные капли.
Кроме воды растворителями могут быть жиры и спирты.
5. Молекулы воды находятся в постоянном движении, сталкиваясь, друг с другом в жидкой фазе, что обеспечивает явление осмоса: поступление воды из почвы, и п л а з м о л и з – выход воды из клеток в гипертоническом растворе;
6. Плотность воды. Вода может находиться в трёх состояниях: жидком, твёрдом и газообразном, что определяет её плотность. В жидком состоянии вода обладает большей плотностью, чем в твёрдом.При охлаждении движение молекул воды замедляется. Количество водородных связей между молекулами становится максимальным. Наибольшей плотности вода достигает при температуре 40 С. При замерзании вода расширяется (необходимо место для образования водородных связей) и её плотность уменьшается, поэтому лёд плавает. Лёд образуется при замерзании сначала на поверхности воды и лишь под конец в придонных слоях. Лёд покрывает толщу воды, как одеялом, выполняя функцию теплоизоляции, это даёт возможность организмам выжить в замерзающей воде, сохранение зимой биоценозов. То обстоятельство, что плотность воды зависит от температуры, обуславливает перемещение и перемешивание воды в водоёмах. Слои воды имеющие температуру ниже 40 С, поднимаются вверх, вместе с водой циркулируют находящиеся в ней питательные вещества, поэтому водоёмы заселяются живыми организмами на большую глубину.
7. Сцепление и поверхностное натяжение. Самое большое поверхностное натяжение из всех жидкостей у воды. Водородные связи обуславливают сцепление (к о г е з и я) её молекул друг с другом и с молекулами других веществ. Благодаря силам сцепления молекул на поверхности воды создаётся поверхностное натяжение. Это свойство используют растения, осуществляя транспорт воды по сосудам – восходящие и нисходящие токи, а также капиллярный кровоток, ток крови и лимфы. Водные растворы являются средством передвижения веществ в организме. Обладая большой силой сцепления, вода у растений поднимается на 10 м.Многие мелкие организмы, благодаря этому удерживают своё тело и могут скользить
на поверхности воды.
8. Вода практически несжимаемая жидкость, что определяет физические свойства клетки: тургор – упругость, её объём, поддержание формы сочных органов и тканей организмов, а тургорное давление обеспечивает необходимое положение органов и частей организма в пространстве.
9. Вязкость воды. Является смазочным материалом - в суставах (синовиальная жидкость), в околосердечной сумке (перикардиальная), между лёгкими и грудной клеткой (плевральная жидкость). Жидкости уменьшают трение при движении суставов, дыхании, работе сердца. Участвует в образовании слизей, облегчающих передвижение веществ по кишечнику, создают влажную среду на слизистых оболочках дыхательных путей. Входит в состав секретов и соков в организме: слюны, желчи, спермы.
Входит в состав жидкостей, образующих, жидкую внутреннюю среду организмов: кровь, тканевая жидкость, лимфа
10. Прозрачность. Для воды характерна полная прозрачность в видимом участке спектра, что дает возможность фотосинтеза, и, следовательно, возможность существования связанных с ним пищевых цепей.
Физиологические функции воды:
· 1. Участвует в процессах пищеварения, входит в состав пищеварительных соков.
· 2. Обеспечивает усвоение пищи – всасывание в кишечнике растворимых мономеров (аминокислот, моно - дисахаридов, глицерина, высших карбоновых кислот),
· 3. Обеспечивает всасывание электролитов,
· 4. Обеспечивает поступление солей в кровь
· 5. Участвует в выделение продуктов обмена
· 6. Участвует в кроветворении,
· 7. Определяет вязкость – разжижение или сгущение крови
· 8. Вода активно участвует в регуляции осмотического давления в клетках. Проникновение молекул растворителя через полупроницаемую мембрану, называется о с м о с о м. Давление, с которым растворитель (вода) проникает через мембрану, называется о с м о т и ч е с к и м.
·
Метаболические функции воды:
· 1. Синтез живого вещества в клетках организма – белков, жиров, углеводов
· 2. Участвует в реакциях гидролиза: гидролиз биополимеров до мономеров:
белки + вода = аминокислоты; крахмал + вода = глюкоза; жир + вода = глицерин + жирные кислоты
· 3. Является средой для химических реакций, протекающих в клетках
· 4. Вода используется в качестве источника кислорода в процессе фотосинтеза.
· 5. Вода является донором электронов в ходе световых реакций фотосинтеза
· 6. Вода источник атомарного водорода для восстановления НАД+, НАДФ+ в НАДН2,, НАДФН2
· 7. Источник протонов водорода для работы протонных насосов в реакциях синтеза АТФ в митохондриях и хлоропластах
В воде может содержаться ряд вредных токсичных для человека веществ (свинец, мышьяк) попавших при сбросе промышленных сточных вод.
В воде содержится небольшие количества минеральных солей в основном углекислых и сернокислых солей кальция, магния, железа. Считается, что вода является мягкой при их незначительном содержании и жёсткой при высоком. В жёсткой воде плохо развариваются овощи и мясо из-за образования солями кальция воды нерастворимых соединений с белками пищевых продуктов, которые плохо усваиваются организмом.
Вода может служить источником распространения инфекционных заболеваний – холеры, брюшного тифа, паратифа, дизентерии, туляремии, бруцеллёза, гельминтозов.
Вода, участвуя в обмене веществ и непрерывно выделяясь из организма через почки, кожу, лёгкие и кишечник, должна пополняться, иначе могут возникнуть расстройства жизненных функций. При потери 10% воды наблюдается обезвоживание, а 20% - смерть. Человек без воды может прожить несколько дней. Взрослый человек в сутки в обычных условиях выделяет 2 - 2,5 л воды, то же количество воды организм должен получить с пищевыми продуктами и питьевой водой. В условиях жаркого климата, а также при физической работе необходимое суточное количество воды для человека доходит до 5 – 6 литров и более, в условиях пустыни – 11 л.
Недостаток воды является одним из главных факторов естественного отбора.