В растворе или расплаве электролиты распадаются на ионы - диссоциируют. Распад электролитов на ионы при растворении их в воде называется электролитической диссоциацией.
В процессе электролитической диссоциации (распаде электролитов на ионы) большую роль играют молекулы воды. Между атомами водорода и кислорода имеются расположенные под углом около 105 ковалентные сильнополярные связи. Поэтому молекулы воды полярны и представляют собой диполи: 
При растворении в воде веществ с ионной связью, например, хлорида натрия, молекулы воды притягиваются своими отрицательными полюсами к положительно заряженным ионам натрия, а положительными полюсами – к отрицательно заряженным хлорид-ионам. В результате связь между ионами ослабляется, и кристаллическая решетка разрушается (рис.1). Таким образом, все ионы в растворе связаны с молекулами воды. Такие ионы называются гидратированными, а процесс их образования гидратацией. Положительно заряженные ионы называются катионами, а отрицательно заряженные – анионами.

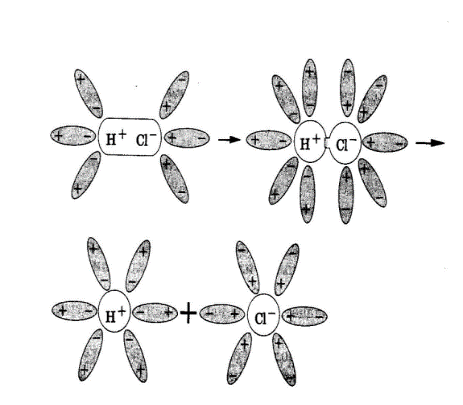
Рис.1. Диссоциация NaCl Рис.2. Диссоциация HCl.
Теория электролитической диссоциации:
1. При растворении в воде (или расплавлении) электролиты распадаются на положительно и отрицательно заряженные ионы (подвергаются электролитической диссоциации).
2. Под действием электрического тока катионы (+) двигаются к катоду (-), а анионы (-) – к аноду (+).
3. Электролитическая диссоциация - процесс обратимый (обратная реакция называется моляризацией).
4. Степень электролитической диссоциации (a) зависит от природы электролита и растворителя, температуры и концентрации. Она показывает отношение числа молекул, распавшихся на ионы (n) к общему числу молекул, введенных в раствор (N).
a = n / N 0<a<1
6.Электролиты и неэлектролиты:
Электролитическая диссоциация веществ, идущая с образованием свободных ионов, объясняет электрическую проводимость растворов.
Процесс электролитической диссоциации принято записывать в виде схемы, не раскрывая его механизма и опуская растворитель (H2O), хотя он является основным участником.
CaCl2 = Ca2+ + 2Cl-
KAl(SO4)2 = K+ + Al3+ + 2SO42-
HNO3 = H+ + NO3-
Ba(OH)2 = Ba2+ + 2OH-
Из электронейтральности молекул вытекает, что суммарный заряд катионов и анионов должен быть равен нулю.
Электролиты - это вещества, растворы которых проводят электрический ток.
Электролиты при растворении в воде распадаются на ионы. (положительные- катионы, отрицательные- анионы), которые могут взаимодействовать друг с другом, но вновь образовывать молекулы, поэтому этот процесс обратимый.
Сильные электролиты: Это вещества, которые при растворении в воде практически полностью распадаются на ионы. Как правило, к сильным электролитам относятся вещества с ионными или сильно полярными связями: все хорошо растворимые соли, сильные кислоты (HCl, HBr, HI, HClO4, H2SO4,HNO3) и сильные основания (LiOH, NaOH, KOH, RbOH, CsOH,Ba(OH)2,Sr(OH)2,Ca(OH)2).
В растворе сильного электролита растворённое вещество находится в основном в виде ионов (катионов и анионов); недиссоциированные молекулы практически отсутствуют.
Слабые электролиты: Вещества, частично диссоциирующие на ионы. Растворы слабых электролитов наряду с ионами содержат недиссоциированные молекулы. Слабые электролиты не могут дать большой концентрации ионов в растворе.
К слабым электролитам относятся:
1) почти все органические кислоты (CH3COOH, C2H5COOH и др.);
2) некоторые неорганические кислоты (H2CO3, H2S и др.);
3) почти все малорастворимые в воде соли, основания и гидроксид аммония (Ca3(PO4)2; Cu(OH)2; Al(OH)3; NH4OH);
4) вода.
Неэлектролиты: Вещества, водные растворы и расплавы которых не проводят электрический ток. Они содержат ковалентные неполярные или малополярные связи, которые не распадаются на ионы. Электрический ток не проводят газы, твердые вещества (неметаллы), органические соединения (сахароза, бензин, спирт).
Степень диссоциации.
Степень диссоциации (a) - отношение числа распавшихся на ионы молекул (n) к общему числу растворенных молекул (N): a = n / N и выражается в долях единицы или в % (a = 0,3 – условная граница деления на сильные и слабые электролиты).
7.Химические свойства воды:
Вода — весьма реакционноспособное вещество. При обычных условиях она взаимодействует со многими основными и кислотными оксидами, а также со щелочными и щелочно-земельными металлами. Вода образует многочисленные соединения - кристаллогидраты.
Под действием электрического тока вода разлагается на водород и кислород:
2H2O электрический ток= 2H2↑+ O2↑
Вода реагирует с щелочными металлами с выделением водорода:
2Na + 2H2O = H2 + 2NaOH (бурно)
2K + 2H2O = H2 + 2KOH (бурно)
Реакция гидратации:
В органической химии реакция гидратации - химическая реакция, в которой вода добавлена к ненасыщенному основанию. Обычно, основание - алкен или alkyne. Этот тип реакции используется промышленно, чтобы произвести этанол, изопропиловый спирт, и с 2 бутанолами. Несколько миллиардов килограммов этиленового гликоля ежегодно производятся гидратацией этиленовой окиси.
Контроль знаний:
1. Виды растворов. Истинные растворы. Классификация веществ по их растворимости в воде.
3.Факторы, от которых зависит растворимость веществ в воде.
4.Значение водных растворов для организма человека.
5.Дать характеристику механизма электролитической диссоциации.
6.Дать определение: электролиты и неэлектролиты. Степень электролитической диссоциации.
Литература:
1.Габриелян О.С. Химия. 11 класс. Базовый уровень: учеб. для общеобразоват. учреждений. – М., 2010,
2. Габриелян О.С. Химия: учеб. для студ. сред. проф. учеб. заведений.- 2-е издание / О.С. Габри елян, И.Г. Остроумов. – М., 2013.
3. https://ru.wikipedia.org - энциклопедия
4..Рудзитис Г.Е., Фельдман Ф.Г, химия. 10 класс: учебник для общеобразовательных учреждений (базовый уровень). – М.: Просвещение, 2016.
 Самостоятельная работа № 4.
Самостоятельная работа № 4.
Тема: Гидролиз органических и неорганических соединений. Необратимый гидролиз. Обратимый гидролиз солей. Практическое значение гидролиза для получения гидролизного спирта и мыла. Биологическая роль гидролиза в пластическом и энергетическом обмене веществ и энергии в клетке.
Окислительно-восстановительные реакции. Степень окисления. Понятие об окислительно-восстановительных реакциях. Окисление и восстановление, окислитель и восстановитель.
Электролиз. Электролиз как окислительно-восстановительный процесс. Электролиз расплавов и растворов на примере хлорида натрия. Практическое применение электролиза. Электролитическое получение алюминия.
Основные понятия и термины по теме: гидролиз и его виды, электролиз, окислительно-восстановительные реакции, степень окисления, окислитель, восстановитель.
План изучения темы:
(перечень вопросов, обязательных к изучению):
1.Понятие гидролиза и его виды.
2.Практического значение гидролиза.
3.Окислительно-восстановительные реакции. Степень окисления.
4.Электролиз как окислительно-восстановительный процесс. Практическое применение электролиза.
Содержание:
Гидролизом называют разложение вещества с водой, что приводит к образованию слабого электролита. Эта реакция является обратной к реакции нейтрализации.
Гидролизу подвергаются как неорганические, так и органические вещества в результате обменной реакции между молекулами воды и вещества. Реакции гидролиза могут протекать как обратимо, так и необратимо. Гидролиз имеет большое практическое значение и основан на теории, а именно теории протекания химических явлений, теории растворов.
Причиной гидролиза является электролитическая диссоциация соответствующих солей и воды. Вода незначительно диссоциирует на ионы Н+ и ОН–, но в процессе гидролиза один или оба из этих ионов могут связываться ионами, образующимися при диссоциации соли, в малодиссоциированные, летучие или труднорастворимые соединения (молекулы или сложные ионы). Происходит изменение реакции среды.
Электролиты – вещества, проводящие электрический ток в растворенном или расплавленном состоянии. К электролитам относятся вещества, имеющие ионную связь: соли, основания, полярные молекулы кислот.
Гидролиз соли - взаимодействие ионов соли с водой, когда образуется слабый электролит [H+] = [OH-] - среда нейтральная, [H+] > [OH-] - среда кислая, [OH-] > [H+] - среда щелочная.
Процесс гидролиза протекает до тех пор, пока не установится равновесие между ионами соли, водой и продуктами гидролиза.
Чтобы точно определить продукты гидролиза, мы должны знать силу кислот и оснований.
В зависимости от своего состава соли по-разному реагируют с водой, поэтому можно выделить 4 типа гидролиза солей.
| 1. Соль образована катионом слабого основания и анионом сильной кислоты. (CuCl2, NH4Cl, Fe2(S04)3 — гидролиз по катиону) CuCl2D Cu2+ + 2Сl- Н2О D Н+ + ОН- Cu2+ + 2Сl- + Н+ + ОН-D CuОН+ + Н+ + 2Сl- Выводы: [ Н+] > [ОН-] _ pH < 7 _ среда раствора кислая _ окраска индикаторов изменяется | 2. Соль образована катионом сильного основания и анионом слабой кислоты. (К2С03, Na2S — гидролиз по аниону) К2С03D 2К+ + С032- Н2О D Н+ + ОН- 2К+ + С032-+ Н+ + ОН - D НСО3- + 2К+ + ОН- Выводы: [ Н+] < [ОН-] _ pH > 7 _ среда раствора щелочная _ окраска индикаторов изменяется |
| 3. Соль образована катионом слабого основания и анионом слабой кислоты. ((NH4)2CO3, CH3COONH4, Na2CO3 — гидролиз по катиону и по аниону) Fe2 (C03)3D 2Fe 3+ + 3C032- Н2О D Н+ + ОН- 2Fe 3+ + 3C032-+ Н+ + ОН-D Fe (ОН)3$+ C02# + Н2О идёт до конца Выводы: Характер среды определяется относительной силой кислоты и основания. | 4. Соль образована катионом сильного основания и анионом сильной кислоты. (гидролизу не подвергаются (NaCl, К2SО4, Ba(N03)2). NaCl D Na+ + Сl- Н2О D Н+ + ОН- Na+ + Сl- + Н+ + ОН- D Na+ + Сl- + Н+ + ОН Выводы: [ Н+] = [ОН-] _ pH = 7 _ среда раствора нейтральная _окраска индикаторов не изменяется |
Процесс гидролиза количественно характеризуется степенью гидролиза (h) и константой гидролиза (К г). Степенью гидролиза называется отношение числа молекул, подвергшихся гидролизу (С гидр.), к общему числу растворенных молекул (С общ.):
 Степень гидролиза зависит от следующих факторов:
Степень гидролиза зависит от следующих факторов:
1. природы соли;
2. ее концентрации;
3. температуры раствора.
Гидролизу подвергаются только те соли, которые образуют при диссоциации ион от слабого электролита. Соли, образованные сильными основаниями и сильными кислотами гидролизу, не подвергаются.
Разбавление раствора равноценно увеличению концентрации одного из реагирующих веществ (воды) и приводит к усилению гидролиза. Усилению гидролиза способствует: увеличение концентрации исходных веществ, продуктов, добавление спирта, кислоты.
Гидролиз концентрированных растворов происходит слабее. Процесс гидролиза эндотермичен, поэтому с повышением температуры протекает полнее. Следовательно, при гидролизе соблюдается принцип Ле-Шателье.
Роль гидролиза в природе и жизни человека:
в процессах формирования и преобразования земной коры; в создании среды для развития жизни в мировом океане; в народном хозяйстве для производства продуктов из непищевого сырья; в повседневной жизни человека, гидролиз спирта и мыла (стирка, борьба с жесткостью воды, процессы пищеварения), в организме человека: биологическая роль гидролиза в пластическом и энергетическом обмене веществ и энергии в клетке.