И все же в некоторых случаях цвет одного и того же вещества зависит вовсе не от структуры. Точнее, не от типа кристаллической решетки. Нет в природе таких веществ, чтобы их структура была совершенна. Человек пытается исправить эту природную «недоработку» и выращивает кристаллы, близкие к идеальным. Без таких кристаллов немыслима современная оптика. Однако природные кристаллы поражают разнообразием цвета и его оттенков. В этом можно убедиться, если посмотреть на кристаллы даже таких простых веществ, как встречающиеся в земле поваренная соль или карбонаты.
В окрестностях польского городка Велички есть соляные разработки, где обширные коридоры и огромнейшие валы, вырубленные в Пластах каменной соли, тянутся галереей на десятки километров. В нишах по бокам галереи можно видеть фигуры, сделанные из соли, и удивительной формы кристаллы. Слабо освещенные, они производят фантастическое впечатление. Иногда они окрашены в синий или фиолетовый цвет. Откуда берется эта окраска в гигантской массе бесцветной соли? Цвет кристаллов, построенных из бесцветных ионов и атомов, появляется в результате нарушений идеальности кристаллической решетки. Несовершенства бывают нескольких видов.
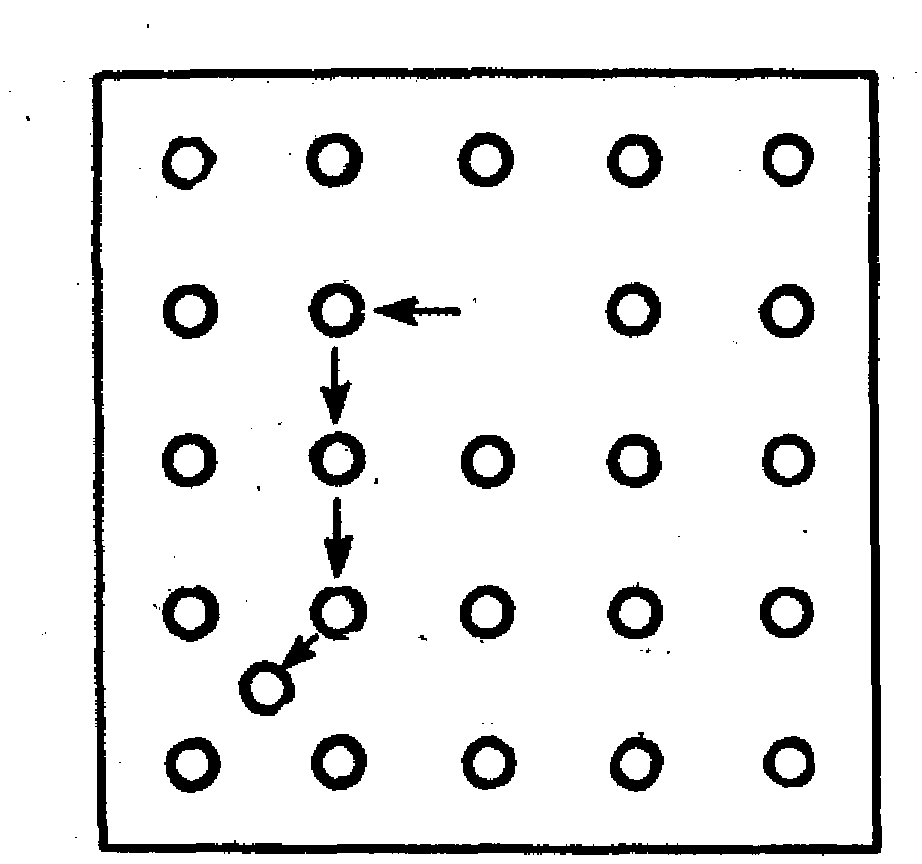
Рис. 9. Дефекты кристаллической структуры: образованно вакансии и появление атома между узлами кристаллической решетки.
Во-первых, из-за неправильного расположения атомов, составляющих кристаллическую решетку (рис. 9). Атомы отсутствуют там, где они должны быть — в узлах кристаллической решетки; возникают незанятые места — вакансии. Смещенные атомы могут появиться в промежутках между теми, которые сохраняют свое нормальное положение. В кристаллические несовершенства включаются и крупные нарушения порядка. Большинство кристаллических тел имеет мозаичное или блочное строение. Между такими блоками (зернами) правильное расположение во многих случаях нарушено. Размеры блоков чаще всего бывают от 1000 до 10000 атомных диаметров, а на их границах образуется область с неправильным расположением атомов. Такие несовершенства обусловливают наличие в кристалле центров окраски из-за того, что в этих местах нарушается нормальное взаимодействие электромагнитного поля, создаваемого ионами и электронами с электромагнитным падающим потоком квантов. Подобный тип окрашенных соединений широко распространен в природе.
Во-вторых, окраску бесцветных веществ определяет наличие атомов посторонних элементов и случайных примесей. Инородные атомы могут быть рассеяны по всему кристаллу или группироваться вместе. И в этом и в другом случае они искажают кристаллическую решетку. Синий или фиолетовый цвет бесцветной каменной соли возникает из за выделения под влиянием радиоактивного излучения металлического натрия. Иногда наряду с хлоридом натрия в ней содержатся и частицы других солей, которые нарушают структуру так же, как металлический натрий.
Совсем недавно для всеобщего обозрения открыта Новоафонская пещера, поражающая своими размерами. В залах, высота которых достигает 100 м, с потолка свешиваются огромные сталактиты. Навстречу им со дна пещеры в виде столбиков поднимаются сталагмиты. Порой и те и другие соединяются вместе, образуя причудливой формы колонны. Убранство залов, подобно убранству подземных дворцов Хозяйки Медной горы из сказки П. П. Бажова, сверкает разноцветием. Откуда же берется эта фантазия красок? Ведь основной составляющий компонент сталактитов и сталагмитов — кальцит, который является одной из двух кристаллических бесцветных форм карбоната кальция СаСОз. Цвет кристаллов вызван включениями посторонних молекул и ионов, часть из которых имеет собственную окраску. Ионы и атомы натрия и калия придают подземным украшениям голубой, синий или фиолетовый оттенок; рубидий и цезий красный или оранжевый. Различные сочетания этих элементов образуют всю красочную полигамию кристаллов, образующих сталактиты, сталагмиты, сталагматы.
Цвет полярных молекул
Когда катионы попадают в поле действия анионов, то возникает взаимное влияние (рис. 10). Результаты зависят от способности электронных оболочек ионов к деформации. Эта способность обусловлена природой иона и силой, с которой данный ион может воздействовать на оболочки соседей. Как правило, ионы малого радиуса и большого положительного заряда деформируются слабо: очень крепко в таком случае положительное ядро притягивает электроны. Деформируемость и связанная с ней поляризация невелика и в том случае, если внешняя электронная оболочка иона подобна оболочке инертного газа, т. е. завершено ее заполнение электронами.
Если молекула состоит из ионов с заполненными электронными оболочками (MgO, ZnS), то возможность перехода электрона практически исключена, так как ему, попросту говоря, некуда переходить. Тогда из всего спектра видимого света молекула не отдает предпочтения ни одному участку. Такие молекулы не имеют окраски. В растворе они бесцветны, а в твердом состоянии белые. К такому типу красящих веществ относятся оксид цинка, оксид магния, фосфат и сульфид цинка, сульфат бария. Как видите, это все соединения элементов II группы периодической системы
Страницы: 1 2 3
Похожие рефераты:
Периодический закон и периодическая система химических элементов Д. И. Менделеева на основе представлений о строении атома
Формулировка периодического закона Д. И. Менделеева в свете теории строения атома. Связь периодического закона и периодической системы со строением атомов. Структура периодической Системы Д. И. Менделеева.
Синтез и свойства комплексов железа (II) и железа (III)
Физические свойства элементов VIIIB группы и их соединений, в частности, соединений железа. Анализ комплексных соединений железа (II) и железа (III) с различными лигандами с точки зрения теории кристаллического поля. Строение цианидных комплексов железа.
Электронное строение атома. Периодический закон
Теория строения атома: микрочастица и волна. Явление дифракции электромагнитного излучения и волновая природа атома: подтверждение гипотезы де Бройля. Уравнение Шредингера и волновая функция. Физическая основа структуры периодической системы элементов.
Оксогидроксид марганца (III) MnO(OH) и его синтез
Общая характеристика, основные физические и химические свойства оксогидроксида марганца (III), триоксалатоманганата (III) калия, диоксалатодиакваманганата (III) калия, порядок их образования и сферы применения. Синтез MnO(OH) и других соединений.
Молекулярные спектры
Спектральный переход в атоме или в молекуле, поглощение (испускание) электромагнитного излучения. В области оптической спектроскопии излучение разделяют с помощью дифракционных решёток, призм, линз. Диапазоны излучения, области молекулярной спектроскопии.
Спектральные методы анализа
Методы, основанные на определении химического состава и строения веществ по их спектру. Методы эмиссии, абсорбции, рассеяния и преломления. Способы воздействия на вещество для получения его спектра. Спектры оптического диапазона. Возбуждение атома.
Углерод. Аллотропные модификации
Углерод: положение в таблице Менделеева, нахождение в природе, свободный углерод. Атомы углерода в графите. Фуллерены как класс химических соединений, молекулы которых состоят из углерода. Первый способ получения твердого кристаллического фуллерена.
Строение и свойства вещества
Министерство путей сообщения Российской Федерации Дальневосточный Государственный Университет путей сообщения КАФЕДРА «Химия» Курсовой проект
Развитие периодического закона. Зависимость свойства элементов от ядра его атома
Изучение атома и его состава и радиоактивности. Характеристика ядерной модели атома. Зависимость свойств элементов и свойств образуемых им веществ от заряда ядра. Анализ квантовой теории света, фотоэлектрического эффекта, электронной оболочки атома.
К вопросу о металлической связи в плотнейших упаковках химических элементов
К вопросу о металлической связи в плотнейших упаковках химических элементов Г.Г.Филипенко Гродно АННОТАЦИЯ. Обычно в литературе металлическая связь описывается, как осуществленная посредством обобществления внешних электронов атомов и не обладающая свойством направленности. Хотя встречаются поп...
Строение атома
Реферат по химии на тему "Строение атома" Существование закономерной связи между всеми химическими элементами, ярко выраженное в периодической системе, наталкивает на мысль о том, что в основе всех атомов лежит нечто общее, что все они находятся в близком родстве друг с другом. Однако д...
Твердофазная полимеризация 1,4-бис-(л-ацетиламинофенил)бутадиина, оптические и фотоэлектрические свойства образующегося полимера
Исследование полимеризации диацетиленовых мономеров, полимеризующихся только в кристаллическом состоянии с образованием полимеров, состоящих из вытянутых цепей с сопряженными связями. Термическая полимеризация и полимеризация под действием Y излучения.
Основы оптической спектроскопии
Сущность и применение методов оптической спектроскопии. Зависимость поглощения света веществом от электролитической структуры молекул. Определение и характеристика групп атомов, обуславливающих поглощение в видимой и ультрафиолетовой областях спектра.
Строение и свойство материалов. Кристаллическое строение. Влияние типа связи на структуру и свойства кристаллов
Понятие строения вещества и основные факторы, влияющие на его формирование. Основные признаки аморфного и кристаллического вещества, типы кристаллических решеток. Влияние типа связи на структуру и свойства кристаллов. Сущность изоморфизма и полиморфизма.
Строение атома
Протоны и нейтроны как составляющие атомного ядра. Атомный номер элемента. Изотопы, ядерная и квантово-механическая модели атома. Волновые свойства электрона. Одноэлектронные и многоэлектронные атомы, квантовые числа. Электронная конфигурация атома.
Химическая связь и строение вещества
Типы химической связи: ковалентная, ионная и металлическая. Донорно-акцепторный механизм образования и характеристики ковалентной связи. Валентность и степень окисления элементов. Молекулы химических соединений. Размеры и масса атомов и молекул.
Кванты излучения и переходы. Уровни энергии и спектральные переходы в атоме водорода
Изучение электронного строения атомно-молекулярных и полимерных систем в квантовой химии. Частицы и волны в классической механике. Свойства света и корпускулярно-волновая природа излучения. Атом водорода, уровни и переходы, частоты и спектральные серии.
Абсорбционные оптические методы
Методы анализа, основанные на поглощении электромагнитного излучения анализируемыми веществами. Атомно-абсорбционный анализ. Молекулярно-абсорбционный анализ. Схема фотометрических исследований. Метод стандартных серий и колориметрического титрования.
Химическая связь
Основные условия образования химической связи. Потенциал ионизации. Ковалентная связь. Перекрывание атомных орбиталей. Процесс смещения электронной пары к наиболее электроотрицательному атому. Координационная связь. Межмолекулярное взаимодействие.
Атомно-кристаллическое строение металлов
Строение металлов в твердом состоянии. Энергетические условия взаимодействия атомов в кристаллической решетке вещества. Атомно-кристаллическое строение. Кристаллические решетки металлов и схемы упаковки атомов. Полиморфные (аллотропические) превращения.
Феновталиин:
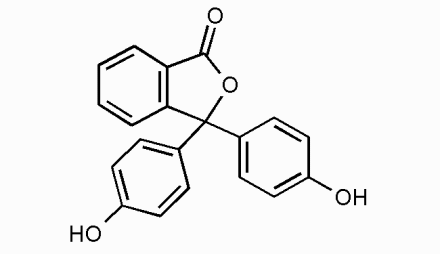 C₂₀H₁₄O₄
C₂₀H₁₄O₄