I. Основные требования к материалам для изготовления ОВ:
· прозрачность в диапазоне рабочих длин волн;
· способность к вытягиванию в виде тонких нитей;
· распространенность и дешевизна.
Наибольшее применение получили ОВ на основе стекла: кварцевого, фторидного, халькогенидного и т.д.

Рис. 1. Рабочие диапазоны оптических волокон на основе различных материалов:
1 – кварцевое стекло, 2 – фторидные стекла, 3 – халькогенидные стекла, 4 – полимерные материалы, 5 – галогениды таллия, серебра и т.д.
Агрегатные состояния вещества: газообразное, жидкое и твердое.
Твердые вещества: кристаллические или аморфные.
Кристаллическое состояние:
- характерен геометрически строгий порядок расположения частиц.
- кристаллическое состояние является стабильным
- характеризуется наиболее низкой внутренней энергией.
- имеют четкие геометрические формы,
- определенные температуры плавления,
- в большинстве случаев проявляют анизотропию физических свойств.
Стеклообразное состояние вещества:
- аморфная разновидность твердого состояния
-характеризуется избытком внутренней энергии (является метастабильным).
- пространственное расположение частиц вещества является неупорядоченным.
Определение стекла согласно комиссии по терминологии АН СССР (1932 г.): стеклом называются все аморфные тела, получаемые путем переохлаждения расплава независимо от их состава и температурной области затвердевания и обладающие, в результате постепенного увеличения вязкости, механическими свойствами твердых тел, причем процесс перехода из жидкого состояния в стеклообразное должен быть обратимым.
Свойства стекла:
1. Стекла рентгеноаморфны.
В структуре стекла отсутствует дальний порядок, т. е. систематическая повторяемость элементарных объемов структуры, характерная для кристаллических веществ.
Основная структурная единица кварцевого стекла:
кремнекислородный тетраэдр:

Рис. 2. Тетраэдрическая группировка (SiO4)-4 (а) и схематическое изображение на плоскости сочленения тетраэдров в структуре кристаллического (б) и стеклообразного кварца (в), а также силикатного стекла (г)
Характеристики структуры:
- отношение rk/ra = 0,29, что приводит к тетраэдрическому расположению атомов;
- произвольное варьирование угла связи Si-O-Si между соседними тетраэдрами, приводящее к искажению кристаллической решетки;
- группировка [SiO4]-4 имеет избыточный отрицательный заряд (-4), но каркасная сетка из тетраэдров в целом электронейтральна;
- наличие кислородных мостиков;
- имеются свободные полости, так как структуры кристаллической и стеклообразной форм SiO2 не являются плотноупакованными;
- в связи с этим наблюдается высокая газопроницаемость кварцевого стекла по сравнению с другими силикатными стеклами;
Основные стеклообразователи ( компоненты, которые способны самостоятельно образовывать непрерывную структуру стекла): SiO2, GеO2, P2O5, B2O3 и т.д.
Модификаторы: обычно оксиды элементов I и II групп периодической системы элементов Д.И.Менделеева.
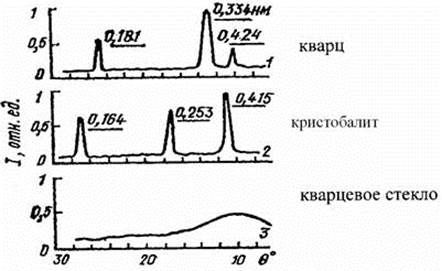
Рис. 3. Рентгенограммы кристаллического кварца (а), кристобалита (б) и кварцевого стекла
2. Стекла изотропны, при условии однородности по составу и отсутствии внутренних напряжений и дефектов.
3. Стекла не имеют определенной температуры затвердевания или плавления.
При охлаждении: расплав переходит из жидкого в пластическое состояние, и только затем в твердое (процесс стеклования).
При нагревании: стекло переходит из твердого в пластическое состояние, а при более высокой температуре - в жидкое (размягчение стекла).
Процессы размягчения стекла или затвердения стекломассы являются однофазными.
Температурный интервал (интервал стеклования) ограничен двумя температурами: со стороны высоких температур – Tf ( в немецкоязычной литературе от слова flussig – жидкий) или Ts (в англоязычной литературе от слова "soft" -мягкий), cо стороны низких температур – Tg (от слова "glass" – стекло):
- при Tg стекло обладает свойствами твердого упругого тела с возможностью хрупкого разрушения.
- температура Tf (Ts) это граница пластического и жидкого состояния
- при Tf удается вытягивать из стекломассы тонкие нити.
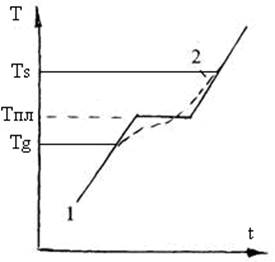
Рис. 4. Зависимость температуры образца от времени повышения температуры нагрева: 1 – для кристаллов, 2 – для стекол
Tg соответствует вязкости стекломассы, равной 1012 Па×с (или 1013 пз); Tf – вязкости 108 Па×с (или 109пз).
Для кварцевого стекла Tg≈1100˚С, Tf ≈1600˚С
При вязкости более 1012 Па×с (< Tg) стекло представляет собой твердое хрупкое тело, а при T>Tf стекломасса находиться в расплавленном состоянии.
Отжиг стеклянных заготовок происходит вблизи Тg, а вытяжка волокна в области Tf
4. Свойства стекол зависят от скорости переохлаждения (или нагревания).
Малая скорость охлаждения - при достижении Ткр. происходит кристаллизация расплава.
Высокая скорость охлаждения - расплав может миновать Ткр. без кристаллизации и находиться в «метастабильном» состоянии «переохлажденной жидкости».
Обычно в стекле существуют 2 фазы:
при кристаллизации - кристаллическая и стекловидная;
при ликвации (явление расслоения расплава на две несмешивающиеся жидкости) – 2 стекловидные с различными составом соединений компонентов.
5. Стекла расплавляются и отвердевают обратимо.
Стадии кристаллизации при переохлаждении:
1 -образование центров (ОЦ) кристаллизации (зародышей) в результате локальных флуктуаций состава и структуры или на примесных включениях.
2- рост кристаллов (РК) на них.
Скорости ОЦ и РК зависят от температуры (или переохлаждения).

Рис. 5. Скорость образования центров кристаллизации (СОЦ) и скорости роста кристаллов (СРК) как функция степени переохлаждения вязкого расплава
Экспериментально установлено: стеклообразное состояние более устойчивое для систем, у которых эти максимумы раздвинуты широко и малы по величине.
Чем больше количество стеклообразователя (высоковязкого компонента), тем сильнее выражена склонность системы к стеклообразованию.
Таблица 2. Вязкость веществ при температурах плавления
| Вещество | Температура плавления, 0С | Вязкость, пз |
| Na Fe H2O Al2O3 LiCl SiO2 GeO2 B2O3 As2O3 BeF2 | 0,01 0,07 0,02 0,6 0,02 107 105 105 106 106 |