Органическая химия
Методические указания и контрольные задания для студентов заочного отделения
специальности 18.02.10 «Коксохимическое производство»
среднего профессионального образования базовой подготовки
Макеевка, 2019
Методические указания и контрольные задания для студентов заочного отделения
разработаны на основе государственного образовательного стандарта среднего профессионального образования по профессии 18.02.10 Коксохимическое производство утвержденного приказом Министерства образования и науки ДНР от 17.07.2015 г. № 325
Организация-разработчик: ГПОУ Макеевский промышленно-экономический колледж
Разработчик Некращук Т.Н. преподаватель-методист высшей квалификационной категории
Пояснительная записка
Органические соединения прочно вошли в качестве сырья в различные отрасли промышленности и составляют основу таких отраслей, как производства искусственных и синтетических волокон, нетканых материалов, синтетических каучуков и резин, клеев, красителей, натуральных и синтетических моющих средств, моторного и дизельного топлива, смазочных материалов, лаков, растворителей, пластмасс и т. д.
Курс органической химии состоит из двух частей: теоретической (лекционный курс) и практической (лабораторные занятия). В целях проверки самостоятельного усвоения теоретической части органической химии студентам заочной формы обучения предлагается выполнить контрольную работу. Данные методические указания содержат всевозможные варианты заданий контрольной работы, которые студенты находят, руководствуясь специальной таблицей.
При выполнении работы студенты должны соблюдать следующие безусловные требования:
1. На обложке отдельной тетради, выделенной для контрольной работы, написать изучаемый предмет, фамилию, имя и отчество студента (все полностью), а также указать номер зачетной книжки.
2. Приводить номера и полные тексты задач. Не сокращать и не изменять условия задач (вопросов).
3. Исправления в работах, возвращенных для доработки, необходимо делать в той же самой тетради после подписи рецензента в объеме, указанном для исправления рецензентом.
4. Избегать длинных описаний, решение обязательно должно содержать формулы и химические уравнения. Необходимо указывать условия, при которых осуществляется та или иная реакция.
5. Все органические соединения необходимо изображать с помощью сокращенных структурных формул (например, СН3СН-2NH-2, СН3СН-2СН-2СООН). Перенос химических формул не допускается.-
6. Для всех исходных и конечных органических соединений в химических реакциях, которые были использованы для решения задач, указать либо тривиальные, либо систематические названия.
7. С наружной стороны страниц оставлять широкие чистые поля для замечаний рецензента.
ПРИМЕРЫРЕШЕНИЯ ЗАДАЧ
Решение любой задачи, посвященной синтезу соединений, обычно начинается с рассмотрения целевого (конечного) продукта. Разбирается: из чего может образоваться подобная структура, кратная связь или функциональная группа? Если найден способ получения конечного продукта, то ведется поиск превращения в промежуточное вещество исходного соединения. Иногда приходится рассмотреть несколько имеющихся вариантов и выбрать единственно правильный.
Поменять место кратной связи или функциональной группы в углеродной цепи обычно удается при использовании в синтезах правил отщепления (А. М. Зайцев) и присоединения (В. В. Марковников, М. Караш) галогеноводородов или воды.
Укорочение углеродных цепей в соединениях обычно происходит при термических процессах (например, при декарбоксилировании некоторых солей карбоновых кислот) и при перегруппировках (в частности, из амидов кислот по А. Гофману). Увеличение углеродных цепей осуществляется, если к функциональной группе (чаще всего к галоидной или магнийгалоидной) или кратной связи можно присоединить углеродсодержащую группу (KCN, CO2, CO, карбонильные соединения и некоторые др.). После укорочения или увеличения углеродной цепи уже стремятся видоизменять функциональные группы на требуемые в задании.
При синтезе ароматических соединений с несколькими заместителями (функциональными группами) из бензола (или нафталина) необходимо воспользоваться правилами ориентации (П. Кернер, Ф. Ф. Бейльштейн) и в нужной последовательности провести реакции.
Но самый обычный тип задач – это получить из чего-нибудь заданный продукт и написать для него ряд реакций. Такие задачи легко решаются, если известны основные способы получения и главные химические свойства заданного вещества.
После нижеприводимых примеров решения типовых задач даются правила, которые важно знать для успешного написания задач.
Задача 1. Из 1-бутанола синтезировать 1-бутин.
Решение. Известно, что алкины (и в их числе 1-бутин) можно получить действием спиртового раствора щелочи на вицинальные дигалогенпроизводные (т. е. в нашем случае можно взять 1,2-дибром-бутан). Последнее вещество образуется при действии молекулярного брома на 1-бутен. В свою очередь, 1-бутен легко получается дегидратацией (отщеплением воды) из 1-бутанола. Эти превращения могут быть выражены следующей схемой реакций (названия под каждой формулой не указаны, так как в тексте решения они все приведены):
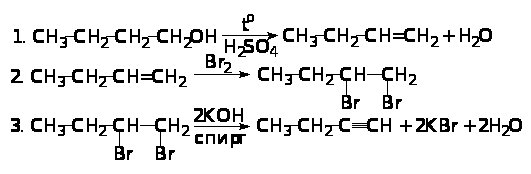
Задача 2. Напишите схемы получения всех изомерных нитрохлорбензолов из бензола.
Решение. При наличии в бензольном ядре двух заместителей возможно получение трех изомеров: о -, м - и п -нитрохлорбензолов. Синтез из бензола того или иного изомера зависит от последовательности введения заместителей NO2- и Cl-. Хлор – заместитель первого рода, нитрогруппа – заместитель второго рода. Если сначала бензол прохлорировать, затем промежуточный продукт (хлорбензол) пронитровать, то получится смесь о - и п -нитрохлорбензолов:
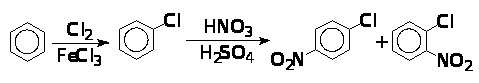
Если же бензол сначала пронитровать, а полученный нитробензол подвергнуть хлорированию, то образуется м -нитрохлорбензол.
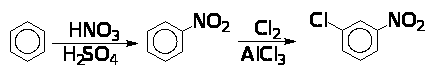
Названия соединений под формулами в реакциях отсутствуют, так как все они употреблены в ходе решения задачи.
Задача 3. Из этилового спирта получить пропионовую кислоту, для последней написать реакции с пятихлористым фосфором, гидроксидом кальция и изопропиловым спиртом.
Решение. Углеродный скелет в этиловом спирте содержит два углерода, а в пропионовой кислоте – три. Есть два способа получения кислот, идущих с увеличением углеродной цепи: оксосинтез кислот из алкенов и магнийорганический синтез из магнийалкилгалогенидов и диоксида углерода. Возможно получение кислот также из нитрилов, которые сами образуются из галоидных алкилов и цианистого натрия (при этом происходит рост углеродной цепи). В любом из трех вариантов надо исходное соединение превращать в промежуточный продукт (алкен или галоидный алкил). Выбираем один из вариантов:
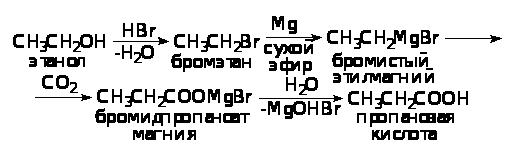
Во второй части задачи надо написать три реакции и назвать получающиеся соединения:
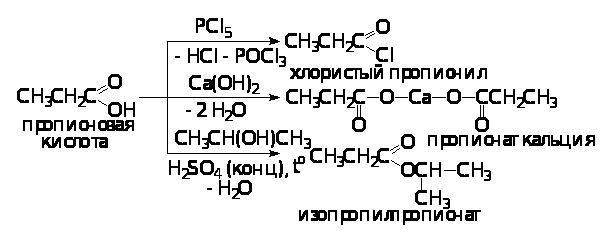
СОВРЕМЕННЫЕ ФОРМУЛИРОВКИ ОСНОВНЫХ ПРАВИЛ
1. Правило замещения атомов водорода в алканах: прочность связей С–Н уменьшается в ряду Сперв–Н > Cвтор–H > Cтрет–Н.
2. Правило С. В. Лебедева для алкенов и изолированных диенов: чем меньше заместителей у двойной связи, тем легче протекает ее гидрирование.
3. Правило В. В. Марковникова для непредельных углеводородов: протон реагента НХ присоединяется к более гидрированному атому углерода у кратной связи, т. е. к тому атому углерода, у которого меньше алкильных электронодонорных заместителей.
Наблюдаются исключения из правила, если имеется электроноакцепторный заместитель у кратной связи или если механизм присоединения меняется с ионного на радикальный (эффект М. Караша).
4. Правило А. М. Зайцева в реакциях отщепления с образованием кратной связи: более легко отщепляется протон от соседнего наименее гидрированного атома углерода к атому углерода с функциональной группой (образуется алкен с большим числом заместителей). Исходные продукты: галогеноуглеводороды и спирты.
Наблюдается исключение из правила (вариант А. Гофмана), когда отщепляется третичный амин от четвертичного аммониевого соединения (соли или гидроксида), имеющего одну длинную углеводородную цепь (из этой цепи образуется алкен).
5. Правило А. А. Петрова для изолированных енинов: галогены присоединяются по двойной связи соединения, а галогеноводород – по тройной.
6. Правила ориентации в бензольном ядре: заместители первого рода облегчают электрофильную атаку (кроме галогенов) и посылают реагент в о - и п -положения, а заместители второго рода затрудняют электрофильное замещение и направляют реагент в м -положения.
7. Правило П. Кернера о числе аренов с одинаковыми заместителями в реакциях: из о -изомера образуются два тризамещенных соединения, из м -изомера – три, из п -изомера – одно.
8. Правило Ф. Ф. Бейльштейна для гомологов бензола: вместо атома водорода в присутствии катализатора галогены вводятся в ядро, а в отсутствии катализатора они вступают в боковую цепь.
9. Правило Ф. Ф. Бейльштейна о несогласованной ориентации: в присутствии двух заместителей первого рода реагент в основном направляет в о - и п -положения сильнейший из них, при наличии двух заместителей второго рода – слабейший из них; если в ядре два заместителя разных родов, то ориентацию ведет заместитель первого рода.
10. Правило Р. Эрленмейера о спиртах: у одного атома углерода не удерживается более одной гидроксильной группы.
11. Правило А. П. Эльтекова – Р. Эрленмейера о енольной перегруппировке: енол превращается в карбонильное соединение, при этом атом водорода гидроксильной группы переходит к наиболее удаленному от него атому углерода двойной связи.
12. Правило А. Н. Попова – Е. Е. Вагнера для окисления кетонов: действие окислителя в основном направлено на разрыв связи между атомом углерода карбонильной группы и соседним наименее гидрированным атомом углерода, причем степень окисления этих атомов углерода – максимально возможная.
13. Электродонорность заместителей I рода уменьшает в ряду NR2 > NHR > NH2 > OH > OR > CH3 > C2H5 > CH2R > (CH3)2CH > F > Cl > Br > I > NHCOR > CH2X. В этом ряду убывает сила насыщать электронной плотностью ароматическое ядро (бензол, нафталин).
14. Электроноакцепторность заместителей II рода уменьшается в ряду NO2 C≡N> > SO3H > COOH > COOR > CHO > CF3 > CCl3 > COR. В этом ряду убывает сила оттягивать электронную плотность от ароматического ядра (от бензола, нафталина).
15. Правила номенклатуры. В основу названия алифатического соединения берется название самой длинной и самой разветвленной углеводородной цепи, имеющей максимально возможное число функциональных групп, кратных связей и углеводородных заместителей. Структурные элементы в порядке убывания старшинства: Функции-суффиксы (записываются окончаниями) > Кратные связи > Функции-префиксы (обозначаются приставками) > Углеводородные заместители. Цифрами перед именами структурных элементов в названии соединения показывается их положение в цепи (их нет для суффиксов карбоксильных и альдегидных групп). Нумерация цепи начинается с того ее конца, к которому ближе старшая функция-суффикс. Если таких структурных элементов в цепи нет, то порядок нумерации определяют кратные связи (= или ≡). При отсутствии функций-суффиксов и кратных связей нумерация основана на позициях в цепи суффиксов-префиксов и углеводородных заместителей. Сумма их положений в цепи должна быть минимальной. Все буквенные обозначения пишут слитно, между цифрами ставят запятые, между буквами и цифрами – дефисы. Старшинство функций-суффиксов (основных характеристических групп) убывает в следующем ряду: -COOH > -SO3H > -COOR > -CONH2 > -C≡N > -CHO > -COR > -OH. Старшинство функций-префиксов (младших функций) и углеводородных заместителей устанавливается по алфавитному порядку.
1. Напишите структурные формулы и названия всех одновалентных радикалов (алкилов): а) метана и этана; б) пропана; в) бутана и изобутана. Поясните как по колличеству электронов радикалы отличаются от соответствующих углеводородов.
2. Напишите эмпирическую формулу этиленовых углеводородов с шестью атомами углерода. Выведите все изомерные углеводороды этого состава (тринадцать) и назовите каждый по систематической номенклатуре.
3. Напишите формулы углеводородов и назовите их по рациональной номенклатуре: а) 2,2 –диметил-пектин-3; б) 3-метил-пектин-1; в) 2,6-диметил-гептин-3; г)2,2,5,5-тетраметил-гексин-3.
4. Напишите формулы следующих углеводородов: а)пропадиен; б) бутадиен-1,3; в)2-метил-бутадиен-1,3; г) гексадиен-2,4; д)гексадиен-1,5; е) 2,3-диметил-бутадиен-1,3. Какие из них относятся к диенам с кумупированными, какие с сопряженными и какие с изолированными двойными связями? Отметьте соединения, являющиеся изомерами.
5. Напишите схемы реакций и укажите условия гидрирования следующих углеводородов: а) 2-метил-пентен-2; б) 2,4-диметилпентен-2; в) 2,4-диметилгексен-3. Назовите образующиеся углеводороды.
6. Напишите реакции дегидрирования: а)этана; б) изобутана; в) бутана; г) 2-метилбутана.
7. Какие из ниже перечисленных углеводородов способны образовывать ацетилениды: а) диэтилацетилен; б)2-метилпентин-4; в)2-метилпентин-3? Напишите соответствующие реакции с аммиачным раствором окиси серебра.
8. Напишите схемы полимеризации по питу 1,4-присоединения для соответствующих диенов: а)дивинил; б) изопен; в) 2,3-диметилбутадиен-1,3. Обозначьте в полимерных цепях звенья исходных момомеров.
9. Как получить этиленовый углеводород: а) из бромистого изопропила; б) из бромистого пропила. Напишите схемы реакции. Назовите продукты.
10. Из каких бром- или ийодпроизводных могут быть получены по реакции Вюрца углеводороды: а) 4,5-диметилокатан; б) 2,3,4,5-тетраметилгексан. Напишите схемы реакций. Назовите исходные галогеналкилы.
11. Напишите реакции получения ацетиленновых углеводородов из следующих галогенпроизводных, действиес раствора щелочи: а)1,1-дибромбутан; б) 4,5-дихлор-2-метилпентан.
13. Определите молекуярную формулу углеводорода, который содержит 85,7% углерода и имеет плотность по водороду 21.
14. Каков объем 8% раствора гидроксида натрия (плотность 1,04 г/см3) потребуется для поглощения оксида углерода (IV), полученного при полном сгорании 11,2 л пропана.
15. На полное гидрирование 2,8 г этиленового углерода израсходовано 0,898 л водорода (н.у.). вычислите молекулярную массу и напишите структурную формулу этого соединения, имеющего нормальную цепь углеродных атомов.
16. Для сжигания 20 м3 смеси пропана и бутана израсходовали 124 м3 кислорода. Определите объемную долю (в%) каждого компонента в смеси.
17. Выведите и назовите все изомерные: а) триметилбензолы; б) метилдиэтилбензолы.
18. Выведите и назовите все углерорды ряда бензола, имеющие состав С9Н12 (восемь изомеров).
19. выведите формулы всех изомерных фенолов состава С7Н80. Дайте им названия.
20. Напишите для бензола реакции присединения: а) трех молекул брома; б) трех молекул хлора. Укажите условия реакций. Назовите продукты.Напишите реакции получения фенолов: а) из бромбензола; б) из о-хлортолуола. Назовите фенолы.
21. Исходя из бензола и испльзуя предварительно необходимые реакции, получите6 а) о- и к-бромнитробензолы; б) м-бромнитробензол.
22. Исходя из толуола, получите М-нитробензольную кислоту.
23. Напишите и объясните реакции нитрования (одной нитроподгруппы): а) толуола; б) нитробензола; в)п-нитротолуола.
24. Напишите реакции получения следующих углеводородов по способу Фриделя –Крафтса: а) этилбензола; б) изобутетанола.
25. При взаимодействии 156 кг бензола с концентрированной азотной кислотой получено 160 кг нитробензола. Рассчитайте выход продукта.
26. Какая масса бромбензола получится при взаимодействии 156 кг бензола ос 110 мл брома (плотность 3,1 г/см3) в присутствии бромида железа (111), если выход составляет 90% от теоретического.
27. В лабораторных условиях путем нитрования бензола массой 0,117 кг избытком нитрующей смеси был получен нитробензол массой 0,166 кг. Вычислите выход нитробензола (в%).
28. В результате дегидроциклизации 2-метилгексана массой 0,2 кг получен метилбензол массой 0,176 кг. Вычислите выход продукта (в%).
29. Какой продукт и какой массы образуется при взаимодействии бензола массой 15,6 кг и смеси 60% азотной кислоты объемом 0,1 м3 (плотностью 1373 кг/м3) и концентрированной серной кислоты.
30. В лаборатории из 25,2 м3 ацетилена получили 18,72 кг бензола. Рассчитайте выход продукта (в %).
31. Напишите структурные формулы всех изомерных спиртов, имеющих молекулярную брутто-формулу С4Н10О. Укажите и назовите первичные, вторичные и третичные спирты. Как окисляются первичные, вторичные и третичные спирты?
32. Из 1-бутена получите соответствующий спирт. Назовите его и подвергните окислению сильным окислителем.
33. Напишите структурные формулы изомерных спиртов, имеющих молекулярную брутто-формулу С5Н12О. Укажите первичные, вторичные и третичные спирты, назовите их по систематической номенклатуре. Напишите уравнения реакций внутримолекулярной и межмолекулярной дегидратации третичного спирта.
34. На 2-пентанол последовательно подействуйте натрием, а затем 2-хлорпен- таном. Укажите, к какому классу соединений относится конечный продукт. Получите конечный продукт межмолекулярной дегидратацией 2-пентанола.
35. Из пропена реакцией гидратации получите соответствующий спирт. Назовите его и напишите для него следующие реакции: а) с пентахлоридом фосфора; б) с масляной кислотой (в присутствии концентрированной серной кислоты).
36. На 2-хлорпентан подействуйте водой (среда щелочная). Для полученного соединения напишите следующие реакции: а) с натрием; б) с пентахлоридом фосфора; в) с уксусной кислотой (в присутствии концентрированной серной кислоты).
37. Напишите структурные формулы спиртов и назовите их по номенклатуре IUPAC.
а) метилвтор-бутилкарбинол;
б) диэтилизопропилкарбинол;
в) бутилтрет-пентилкарбинол;
г) изопропилизобутилнеопентилкарбинол.
38. Какие спирты образуются в результате следующих реакций:
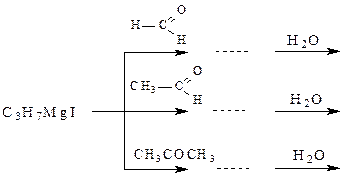
39. Получите этиленгликоль всеми известными способами.
40. Осуществите внутри- и межмолекулярное взаимодействие изопропилового спирта и пентанола-2.
41. Каким путем можно осуществить переход:
а) пропиловый спирт ® изопропиловый спирт
б) (С2Н5)2СН-СН2-ОН ® (С2Н5)2С(ОН)-СН3
42. Какие продукты образуются при окислении этиленгликоля, изопропилового спирта, третбутилового спирта.
43. Напишите структурную формулу соединения состава С4Н10О, которое реагирует с металлическим натрием с выделением водорода, а при окислении образует кетон.
44. Два амиловых спирта (I) и (II) дают при действии PI3 соответствующие монойодпроизводные; при дегидройодировании последних получается один и тот же алкен – 2-метилбутен-2, напишите структурные формулы этих веществ.
45. Установите строение вещества состава С8Н18О2, которое обладает следующими свойствами:
а) реагирует с метилмагнийиодидом с выделением 2 моль метана
б) при окислении йодной кислотой образуется только метилэтилкетон (йодная кислота – НIO4 характерный агент на 1,2-гликоли, расщепляет С-С-связь с образованием альдегидов или кетонов)
46. Установите строение вещества состава С5Н12О, которое при взаимодействии с йодистым метилмагнием выделяет метан, а при окислении образует альдегид, обладающий оптической активностью.
47. Осуществите превращения:
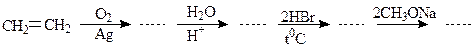
48. Установите состав вещества С5Н12О если:
а) при нагревании с уксусной кислотой в присутствии серной кислоты дает соединение состава С7Н14О2;
б) при окислении образуется кетон, последующее окисление которого по правилу Попова дает смесь уксусной и пропионовой кислот.
49. Спирт, строения С7Н16О вступает в реакцию этерификации; при нагревании с Al2O3 образует соединение состава С7Н14, озонолизом которого получены метилэтилкетон и пропионовый альдегид. Установите строение спирта.
50. Напишите структурную формулу соединения состава С5Н12О, если известно, что оно реагирует с металлическим натрием с выделением водорода, при окислении дает кетон состава С5Н10О, а при дегидратации образует 2-метил-2-бутен.
51. Синтезируйте спирт, при окислении которого сначала образуется кетон состава С5Н10О, а при дальнейшем окислении – ацетон и уксусную кислоту
52. Назовите соединения по систематической и рациональной номенклатуре:
а)
б) 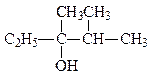
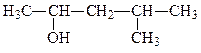
в)
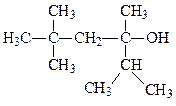
г)
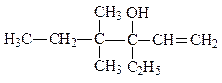
53. Напишите структурные формулы всех предельных одноатомных вторичных спиртов нормального строения, содержащих 3,4,5 и 6 атомов углерода. Назовите их по рациональной номенклатуре.
54. Напишите структурные формулы и назовите по номенклатуре IUPAC ненасыщенные спирты: аллиловый, пропаргиловый, винилэтилкарбинол.
55. Напишите структурные формулы всех изомерных двухатомных спиртов молекулярной формулы С4Н10О2. Назовите их.
56. Какие спирты образуются в результате щелочного гидролиза: а) бромистого этила; б) йодистого изопропила; в) хлористого изобутила? Напишите схемы реакций.
57. Напишите схемы получения следующих производных этиленгликоля: а) диметилового эфира; б) моноацетата; в) динитрата; г) этиленхлоргидрина.
58. Напишите структурные формулы простых эфиров состава С4Н10О. Назовите их.
59. Назовите следующие соединения:
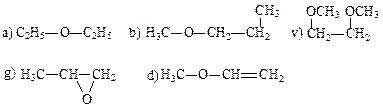
60. Напишите структурные формулы соединений: а) 1-метоксипентана; б) моноэтилового эфира этиленгликоля; в) окиси симм- диметилэтилена.
61. Напишите структурные формулы следующих соединений: изопропилбромида; втор-бутилхлорида; трет-бутилйодида; йодистого амила; хлористого гексила; 1,3-дихлорпропана; 1,2-дибром-3-метилгептана.
62. Напишите структурные формулы всех изомерных соединений С4Н9Br. Назовите их по рациональной и систематической номенклатуре.
63. Напишите схему реакции пропана с хлором. Укажите условия. Разберите механизм.
64. Осуществите превращения:

65. Синтезируйте приведенные соединения исходя из бромистого аллила:
СН2=СН-СН2-СН2-СН=СН2; 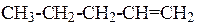
66. Напишите структурную формулу вещества C4H9Br, если известно, что при нагревании с металлическим натрием он образует 3,4-диметилгексан.
67. Напишите структурную формулу соединения С4H9Сl, образующего при гидролизе продукт состава С5Н12О. последний при дегидратации и последующем озонолизе превращается в смесь формальдегида и метилэтилкетона.
68. С помощью реакции Вюрца-Фиттига получите следующие соединения:
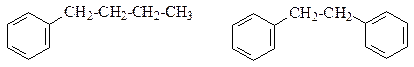
69. Каково строение соединения С6Н4BrСl, которое при последовательной обработке магнием в абсолютном эфире, диоксидом углерода и разбавленной HCl дает м-хлорбензойную кислоту.
70. Из иодистого изопропила получите:
а) магнийиодизопропил; б) 2,3-диметилбутан; в) 2-нитропропан.
71. Сколько ароматических изомеров состава С7Н7Cl можно написать. Назовите их по номенклатуре ИЮПАК.
72. Напишите структурную формулу соединения С7Н7Br, если известно, что при взаимодействии с бромистым аллилом образуется 4-фенилбутен-1.
73. Назовите соединения:
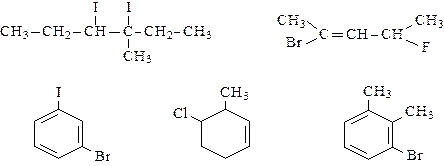
74. Напишите структурную формулу вещества состава С3Н7Cl, если известно, что при нагревании с металлическим натрием он образует н-гексан.
75. Как изменяются длины связей в ряду C-F, C-Cl, C-Br, C-I. Почему иодистые алкилы обладают большей реакционной способностью.
76. Осуществите превращение:
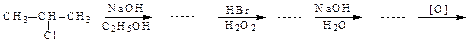
77. Какова структурная формула соединения С8Н6Сl4, при гидролизе которого образуется 3-метил-4-хлорбензойная кислота.
78. Напишите структурные формулы и назовите все возможные изомеры для 2-бромбутена-2.
79. По методу Вюрца-Фиттига получите:
а) 1,6-дифенилгексан
б) пентен-1
в) пропилбензол
80. Сколько монохлорпроизводных можно произвести от н-пентана, напишите структурные формулы. Назовите каждое из соединений по номенклатуре ИЮПАК.
81. Назовите соединения:
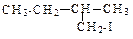
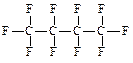
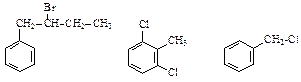
Для первого соединения напишите и назовите все изомеры.
82. Напишите структурную формулу вещества С4Н9Br, образующего при гидролизе первичный спирт, а при дегидробромировании и последующем гидробромировании третичное бромпроизводное.
83. Напишите схему бромирования пропилбензола в боковую цепь. Какими способами можно инициировать данную реакцию? Разберите механизм.
84. Осуществите цепочку превращений:
Бензол ® А ® Б ® пара -Бромэтилбензол® В ® пара -Гидроксибензойная кислота
85. Напишите уравнения реакций бензилхлорида:
а) с водным раствором гидроксида натрия
б) цианидом натрия
в) этилатом натрия
г) аммиаком
86. Напишите структурную формулу ароматического углеводорода состава С9Н12, при моногалогенировании которого получают только одно галогензамещенное производное.
87. Напишите все соединения, изомерные 3-хлорпентину-1.
Назовите все полученные соединения по систематической номенклатуре ИЮПАК.
88. Какое строение имеет алкилгалогенид состава C4H9Br, если после его дегидрогалогенирования в спиртовом растворе щелочи образуется алкен С4Н8 который после озонирования дает уксусный альдегид? Напишите уравнения реакций.
89. Из 1-хлорпропана, через стадию образования нитрила получите масляную (бутановую) кислоту. Как эта кислота реагирует:
а) с гидроксидом бария;
б) с пентахлоридом фосфора?
90. Окислите пропаналь. На продукт окисления подействуйте последовательно гидроксидом натрия, а затем 2-хлорпропаном.
91. 1,1,1-Трихлорбутан гидролизуйте. На полученное соединение подействуйте следующими реагентами: а) аммиаком; б) 2-пропанолом в присутствии концентрированной серной кислоты.
92. На хлорэтан подействуйте цианидом калия. Продукт реакции гидролизуйте (среда кислая). Полученное соединение обработайте пентахлоридом фосфора.
93. Напишите структурные формулы всех карбоновых кислот состава С5Н10О2. Назовите их.
94. Какое соединение получится в результате следующих превращений: 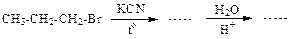
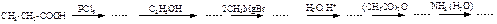
95. Осуществите переходы:
а) пропен → диметилуксусная кислота
б) этилэтилен → бутановая кислота
96. Установите строение соединения С4Н8О2, обладающее следующими свойствами:
а) реагирует с водным раствором соды с выделением СО2
б) при сплавлении со щелочью образует пропан
в) с Са(ОН)2 дает соль при пиролизе которой получается изопропилкетон
97. 1,4-Бутандиол энергично окислите. На полученное соединение подействуйте последовательно пентахлоридом фосфора, а затем этилатом натрия (реактивы брать в избытке).
98. На 2-хлорпропан подействуйте цианидом калия. Полученное соединение гидролизуйте (среда щелочная). Как продукт гидролиза взаимодействует с 2-хлорпропаном?
99. Из бромэтана получите: а) уксусную кислоту (в качестве промежуточного соединения должен быть получен соответствующий спирт); б) пропионовую кислоту (в качестве промежуточного соединения должен быть получен соответствующий нитрил). Как указанные кислоты реагируют с аммиаком?
100. Осуществите превращения:
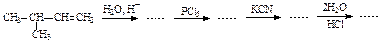
101. 2-Метил-1-пропанол энергично окислите. Продукт окисления введите в следующие реакции: а) с пентахлоридом фосфора, а затем с аммиаком; б) с гидроксидом серебра.
102. Как получить из 4-метил-пентанона-2:
а) изовалериановую кислоту;
б) изомасляную кислоту
103. На 1,2-дибромпропан подействуйте избытком цианида калия. Продукт реакции подвергните исчерпывающему гидролизу (среда кислая). На продукт гидролиза подействуйте избытком 2-пропанола в присутствии концентрированной серной кислоты.
104. Назовите соединения по рациональной номенклатуре и номенклатуре ИЮПАК. К какому классу соединений относятся каждое из них:
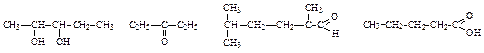
105. Из 1-хлорбутана через стадию образования соответствующего спирта получите масляную кислоту. Полученную кислоту превратите в ее ангидрид. На масляный ангидрид подействуйте аммиаком.
106. Вещество С9Н18О2 при прокаливании с гидроксидом натрия превращается в углеводород С8Н18, который идентичен соединению, образующемуся при электролизе соли триметилуксусной кислоты. Каково строение исходного соединения. Назовите С9Н18О2.
107. Окислите 2,3-диметилбутаналь. На продукт окисления подействуйте реагентами: а) гидроксидом кальция; б) 2-пропанолом в присутствии водоотнимающего реагента.
108. Из 1-хлорпропана получите:
а) пропионовую кислоту (в качестве промежуточного соединения должен быть получен соответствующий спирт); б) масляную кислоту (в качестве промежуточного соединения должен быть получен соответствующий нитрил).
109. Из пропаналя получите пропионовую кислоту. Как пропионовая кислота будет взаимодействовать с гашеной известью? Подвергните пиролизу полученный продукт.
110. Приведите два способа получения ангидрида уксусной кислоты. На полученный ангидрид подействуйте: а) 2-пропанолом; б) аммиаком.
111. Из адипиновой кислоты получите ее полный изопропиловый эфир. На полученный продукт подействуйте последовательно избытком раствора гидроксида натрия, а затем избытком 1-хлорпропана.
112. Установите состав вещества С5Н12О если:
а) при нагревании с уксусной кислотой в присутствии серной кислоты дает соединение состава С7Н14О2;
б) при окислении образуется кетон, последующее окисление которого по правилу Попова дает смесь уксусной и пропионовой кислот.
113. На глицерин подействуйте масляной кислотой (3 моля). На полученное соединение подействуйте избытком разбавленного раствора гидроксида натрия.
114. Приведите два способа получения амида пропионовой кислоты. Полученный амид введите в реакцию с оксидом фосфора (V) при нагревании.
115. Ангидрид масляной кислоты нагрейте с водой. Полученный продукт последовательно введите в реакции с пентахлоридом фосфора, а затем — с аммиаком.
116. Получите ангидрид пропионовой кислоты. Из ангидрида пропионовой кислоты получите: а) амид пропионовой кислоты; б) изопропиловый эфир пропионовой кислоты.
117. Напишите структурные формулы соединений и назовите их по номенклатуре IUPAC:
а) триметилуксусная кислота;
б) винилизобутилуксусная кислота;
в) дитрет-пентилуксусная кислота;
г)аллилдипропилуксусная кислота.
118. Из акриловой кислоты получите хлорангидрид акриловой кислоты. Полученный продукт введите в реакцию с этилатом натрия. Напишите схему реакции полимеризации полученного продукта.
119. Из аммиака и соответствующего галогенопроизводного получите 2-аминобутан. Полученное соединение введите в реакции: а) с серной кислотой; б) с ангидридом пропионовой кислоты.
120. Нитрил уксусной кислоты прогидрируйте (в присутствии катализатора). На продукт реакции последовательно подействуйте 2-йодпропаном, а затем аммиаком. Как конечное соединение реагирует с хлорангидридом уксусной кислоты?
121. 2-Нитропропан восстановите активным водородом. На продукт восстановления подействуйте: а) хлороводородной кислотой; б) 1-хлорпропаном, а затем аммиаком.
122. Из аммиака и соответствующего галогеналкана получите диизопропиламин. Полученное соединение введите в реакции: а) с бромоводородной кислотой; б) с азотистой кислотой.
123. 1-Аминопропан введите в реакции: а) с 2-йодпропаном (с последующей обработкой аммиаком); б) с азотистой кислотой; в) с уксусным ангидридом.
124. Из аммиака и соответствующих галогеналканов последовательно получите пропиламин, а затем пропилизопропиламин. На конечный продукт реакции подействуйте азотистой кислотой.
125. Из метиламина через ряд последовательных реакций получите метилэтилпропиламин. Полученное соединение введите в реакцию с серной кислотой.
126. 2-Амино-2-метилпропан введите в реакции:
а) с хлорэтаном (с последующей обработкой аммиаком); б) с ангидридом пропионовой кислоты; в) с азотистой кислотой.
127. 2-Цианпропан прогидрируйте (в присутствии катализатора). На полученное соединение подействуйте реагентами: а) 1-хлорпропаном; б) ангидридом масляной кислоты.
128. Из этиламина получите этилизопропиламин. Полученное соединение введите в реакции: а) с хлороводородной кислотой; б) с азотистой кислотой.
129. Из аммиака и соответствующих галогеналканов последовательно получите изопропиламин, а затем этилизопропиламин. Конечный продукт реакции введите во взаимодействие с ангидридом пропионовой кислоты.
130. 1-Нитро-2-метилпропан восстановите активным водородом. Полученное соединение введите в реакции: а) с азотистой кислотой; б) с 1-йодпропаном (с последующей обработкой аммиаком).
131. Из аммиака и соответствующих галогеналканов последовательно получите бутиламин, а затем бутилизопропиламин. Как конечный продукт реакции реагирует с азотистой кислотой?
132. Из пропиламина через ряд промежуточных реакций получите метилэтилпропиламин. Как этот амин реагирует с серной кислотой?
133. 2-Аминопропан введите в следующие реакции: а) с ангидридом пропионовой кислоты; б) с 2-йодпропаном (с последующей обработкой аммиаком; в) с азотистой кислотой.
134. Из нитрила пропионовой кислоты получите пропиламин. Для пропиламина напишите уравнения реакций: а) с 2-йодбутаном; б) с бромоводородной кислотой.
135. Из аммиака и соответствующих галогеналканов последовательно получите этиламин, а затем этилбутиламин. Полученные амины введите в реакцию с анг