Тема «Закон авогадро и сдедствия из него»
Задания:
1. Ознакомиться с теоретическим материалом.
2. Составить конспект (основное выделено зелёным цветом)
3. Ркшить задачи:
Задача 1. Рассчитайте, какой объем занимают 5 моль аммиака (н. у.).
Задача 2. Рассчитайте, какой объем при нормальных условиях займет оксид углерода(IV) массой 5,6 г.
Задача 3. Определите массу 5 л аммиака (н. у.). Какое количество вещества аммиака заключено в этом объеме?
Задача 4. Определите, какой объем занимают 1,204 · 1023 молекул кислорода (н. у.).
Теоретический материал
Закон Авогадро: в равных объёмах различных газов при одинаковых условиях (температуре и давлении) содержится одинаковое число молекул. (1811 г, итальянский учёный Амедео Авогадро)
Cледствия из закона Авогадро:
1 следствие:
Одинаковое число молекул различных газов при одинаковых условиях занимает одинаковый объём.
Так, 6,02 ∙ 1023 молекул (1 моль) любого газа и любой смеси газов при (н.у.) занимает объём равный 22,4 л.
Такой объём называется молярным объёмом и обозначается Vm
Молярный объём – это постоянная величина для веществ – газов при нормальных условиях (н.у.):
| Vm = 22,4 л/моль н.у. – это p = 1амт (101325 Па) t = 0 ˚C (273 К) |
Взаимосвязь молярной массы, молярного объёма, числа Авогадро и количества вещества:
υ = V / Vm = N / Na = m / M
M = ρVm
2 следствие:
Отношение масс одинаковых объёмов различных газов при одинаковых условиях равно отношению их молярных масс (поскольку в равных объёмах газов при одинаковых условиях содержится одинаковое число молекул и, следовательно, одинаковое число молей):
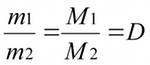
Это отношение называется относительной плотностью D (или d) одного газа по другому.
|
|
D – показывает во сколько раз один газ тяжелее или легче другого и является безразмерной величиной.
Например,
DO2 (газа)= Mr(газа)/Mr(O2)=Mr(газа)/32;
DH2 (газа)= Mr(газа)/Mr(H2)=Mr(газа)/2;
Dвоздуха (газа)= Mr(газа)/Mr(воздуха)=Mr(газа)/29.
Задача
Образец: Найдите относительную плотность газа N2 по воздуху?
| Дано: N2 М(воздуха) = 29 | Решение: Dвоздуха (N2)= Mr(N2)/Mr(воздуха)=Mr(N2)/29. Mr(N2) = 2·Ar(N) = 2· 14 = 28 г/моль Dвоздуха (N2)= Mr(N2)/Mr(воздуха)=Mr(N2)/29=28/29= 0,97 Ответ: Газ азот легче воздуха в 0,97 раз Dвоздуха (N2)= 0,97 |
| Найти: Dвоздух -? |
Закон объемных отношений
Гей-Люссак, 1808 г.
"Объемы газов, вступающих в химические реакции, и объемы газов, образующихся в результате реакции, относятся между собой как небольшие целые числа".
Следствие. Стехиометрические коэффициенты в уравнениях химических реакций для молекул газообразных веществ показывают, в каких объемных отношениях реагируют или получаются газообразные вещества.
V1:V2:V3 = ν1:ν2:ν3.
Коэффициенты, стоящие перед химическими знаками и формулами, показывают не только число молекул или формульных единиц, но и число молей, участвующих в реакции. Поэтому уравнения реакций между газами можно записать и так:
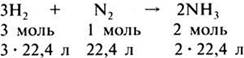
Если разделить указанные численные значения объемов реагирующих и образующихся газов на 22,4, то получатся простые целые числа, показывающие объемные отношения газов: 3: 1: 2. Следовательно, реакции между газообразными веществами подчиняются определенным закономерностям: при неизменном давлении объемы реагирующих и образующихся газов относятся между собой как небольшие целые числа.
Коэффициенты в уравнениях реакций показывают число объемов реагирующих и образующихся веществ:
|
|
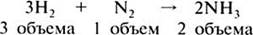
Далее на конкретном примере дается алгоритм решения типовой задачи.
Задача. Вычислите объем углекислого газа (оксида углерода(IV)), который выделится при сгорании 2 л метана (н. у.).

Какой объём кислорода (н.у.) потребуется для полного сгорания 10 м3 пропана С3Н8 (н.у.)?
| Дано: V(С3Н8) = 10 м3 | Решение: 1. Запишем УХР С3Н8 + 5О2 → 3СО2+ 4Н2О 1моль 5моль 2. Согласно закону объёмных отношений для газов: V(С3Н8):V(О2) = ν(С3Н8):ν(О2) = 1: 5 10 м3:V(О2) = 1: 5 V(О2) = (10 · 5) /1= 50 м3 Ответ: Для сжигания 10 м3 пропана потребуется 50 м3 кислорода. |