Заполните рабочую тетрадь по данной теме.
Проведите расчёт пипетки.
3. Увеличьте объем рабочего раствора на 10%. Проведите расчет концентрации с полученным объемом.
Сделайте вывод о качестве лекарственной формы
При необходимости произведите расчеты по исправлению лекарственной формы
Выполненные задания присылать в личном сообщении ВК в виде фото или скринов (не перевернутые). Под своим именем.
Срок сдачи: до 16-00 05.10.2021г
ИНСТРУКЦИЯ К ПРАКТИЧЕСКОМУ ЗАНЯТИЮ
Предмет: МДК 02.02. Контроль качества лекарственных средств
Тема: Лекарственные средства гетероциклических соединений. Анализ фурацилина в таблетках.
Цель: Научиться проводить анализ некоторых показателей фурацилина в таблетках согласно ДФУ.
Tabulettae Furacilini 0,02
Состав на одну таблетку: Фурацилина 0,02 г
Натрия хлорида 0,8 г
Основное действующее вещество: Фурацилин Nitrofuralum
5- нитрофурфурола семикарбазон
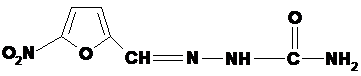
С6Н6N4O4 М. м. 198,14
Описание
Таблетки желтого или зеленовато-желтого цвета.
Подлинность
Теоретическая часть
Являясь производным 5-натрофурана фурацилин с водным раствором натрия гидроксида образует ацисоль, окрашенную в оранжево-красный цвет.

При нагревании в растворе натрия гидроксида происходит разрыв фуранового цикла и образуется карбонат натрия, гидразин и аммиак. Наличие аммиака обнаруживается по изменению окраски влажной лакмусовой бумаги.
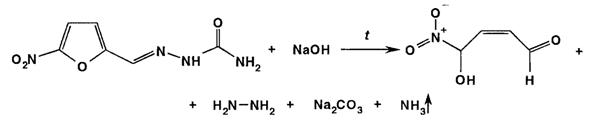
Так как в таблетках в качестве вспомогательного вещества содержится натрия хлорид, то препарат дает характерную реакцию на хлориды.
Ход анализа
1. Таблетки растирают в ступке в порошок. 1,2 г порошка растертых таблеток помещают в коническую колбу на 50 см3 и растворяют в 5 см3 воды и 5 см3 раствора натрия гидроксида. Должно появиться оранжево-красное окрашивание.
При нагревании полученного раствора на водяной бане выделяется аммиак, обнаруживаемый по запаху или по посинению влажной индикаторной бумаги, внесенной в пары кипящей жидкости.
2. 0,1 г порошка растертых таблеток помещают в коническую колбу на 50 см3 растворяют в 10 см3 воды, прибавляют 0,5 см3 разведенной азотной кислоты и 0,5 см3 раствора аргентум нитрата, образуется белый творожистый осадок.
Количественное определение
Теоретические основы
Для определения содержания лекарственных веществ в таблетках следует брать определенную массу порошка растертых таблеток. Для получения средней пробы необходимо растирать не менее 20 таблеток и из этой смеси брать точную навеску.
Количественное определение фурацилина в препарате выполняют йодометрическим методом, основанном на окислении препарата йодом в щелочной среде. Предварительно для улучшения растворимости препарата, смесь подогревают. Титрованный раствор йода в щелочной среде образует гипойодид:

Гипойодид окисляет фурацилин до 5-нитрофурфурола:
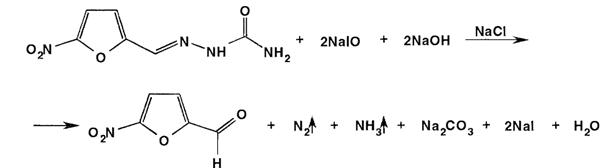
По окончании процесса окисления раствор подкисляют и титруют выделившийся избыток йода тиосульфатом натрия:
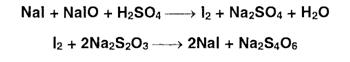
Ход анализа.
Около 0,8 г (точная навеска) порошка растертых таблеток помещают в мерную колбу емкостью 100 см3, прибавляют 70 см3 воды и растворяют на водяной бане при 70 - 80ºС до получения прозрачного раствора.
Раствор охлаждают и доводят водой до метки и перемешивают.
В коническую колбу вместимостью 50 см3 помещают 5 см3 раствора йода с молярной эквивалентной концентрацией 0,01 моль/дм3, прибавляют 0,1 см3 раствора NaOH и 5 см3 приготовленного раствора препарата.
Через 1-2 минуты к раствору прибавляют 2 см3 разведенной серной кислоты и выделившийся йод титруют из микробюретки раствором натрия тиосульфата с молярной эквивалентной концентрацией 0,01 моль/дм3 в присутствии индикатора крахмала
Расчеты содержания фурацилина проводят по формуле обратного титрования.
0,0004954 – масса С6Н6N4O4, в граммах, которая соответствует 1 см3 раствора йода с эквивалентной молярной концентрации 0,01 моль/дм3;
Масса основного вещества в одной таблетке должна быть 0,018 – 0,022 г, вычисляют ее по формуле:

Реактивы и оборудование.
1. Раствор натрия гидроксида.
2. НNO3 разведенная.
3. Раствор аргентум нитрата.
4. Индикаторная бумага.
5. H2SO4 разведенная.
6. Раствор йода с молярной эквивалентной концентрацией 0,01 моль/дм3.
7. Раствор Na2S2O3 молярной эквивалентной концентрацией 0,01 моль/дм3.
8. Колбы конические на 50 см3.
9. Колбы мерные на 100 см3
10. Пипетки на 1,2 и 5 см3.
11. Микробюретка.
Вопросы для самостоятельного изучения (письменно)
1. Привести формулу 5-нитрофурана, производным которого является фурацилин. К какому классу органических веществ относится данное соединение.
2. В каких еще лекарственных формах находит применение фурацилин.