1 вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства хлорида алюминия, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор хлорида алюминия, а также набор следующих реактивов: водные растворы нитрата бария, гидроксида натрия, нитрата серебра, сульфата магния и металлический цинк.
2) К раствору силиката калия массой 22,45 г и массовой долей 10% прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой:
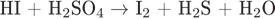
Определите окислитель и восстановитель.
2 вариант
1) Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства нитрата серебра, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор нитрата серебра, а также набор следующих реактивов: водные растворы соляной кислоты, бромида калия, нитрата магния, ацетата свинца и уксусной кислоты.
2) К раствору сульфата алюминия массой 75 г и массовой долей 15% прилили избыток раствора хлорида бария. Вычислите массу образовавшегося осадка
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
3 вариант
1) Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства металлического цинка, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан металлический цинк, а также набор следующих реактивов: водные растворы аммиака, гидроксида натрия, сульфата магния, соляной кислоты и нитрата калия.
2) Вычислите объём газа (н. у.), который выделится при действии избытка сульфида железа(II) на 490 г 15%-ного раствора серной кислоты.
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
4 вариант
1) Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства металлической меди, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дана металлическая медь, а также набор следующих реактивов: водные растворы хлорида натрия, нитрата серебра, азотной кислоты, сульфата магния и фосфата натрия.
2) Через 42 г раствора с массовой долей гидроксида натрия 12% пропустили сернистый газ. При этом образовался сульфит натрия. Вычислите объём (н. у.) вступившего в реакцию газа.
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
5. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства гидроксида алюминия, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан порошкообразный гидроксид алюминия, а также набор следующих реактивов: водные растворы хлорида натрия, нитрата бария, гидроксида натрия, сульфата калия и серной кислоты.
2) Раствор соляной кислоты массой 125 г и массовой долей 16% добавили к избытку сульфида магния. Вычислите объём (н. у.) выделившегося газа.
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
6. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства гидроксида цинка, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан порошкообразный гидроксид цинка, а также набор следующих реактивов: водные растворы гидроксида натрия, нитрата калия, сульфата натрия, соляной кислоты и ацетата натрия.
2) К раствору карбоната калия массой 120 г и массовой долей 18% прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
7. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства гидроксида кальция, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор гидроксида кальция, а также набор следующих реактивов: газообразный оксид углерода(IV), водные растворы гидроксида натрия, фосфорной кислоты, нитрата бария и металлический цинк.
2) После пропускания через раствор гидроксида калия 2,24 л сернистого газа (н. у.) получили 265 г раствора сульфита калия. Вычислите массовую долю соли в полученном растворе.
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
8. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата меди(II), и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор сульфата меди(II), а также набор следующих реактивов: водные растворы гидроксида калия, хлорида калия, нитрата бария, бромида калия и ацетата калия.
2) Вычислите объём углекислого газа (н. у.), который выделится при действии на избыток карбоната кальция 820 г 15%-ного раствора соляной кислоты.
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
9.вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства карбоната кальция, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан порошкообразный карбонат кальция, а также набор следующих реактивов: водные растворы соляной кислоты, нитрата калия, гидроксида натрия, хлорида натрия и насыщенный водный раствор оксида углерода(IV) в воде.
2) К раствору карбоната калия массой 28,6 г и массовой долей 12% прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
10. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства нитрата аммония, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан порошкообразный нитрата аммония и набор следующих реактивов: водные растворы гидроксида калия, сульфата калия, нитрата калия, ацетата калия, а также спиртовая горелка.
2) При взаимодействии 12,0 г оксида серы(VI) с избытком раствора гидроксида калия получили 175 г раствора средней соли. Вычислите массовую долю соли в полученном растворе.
3) Используя метод электронного баланса, составьте уравнение реакции:

Определите окислитель и восстановитель.
11. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства фосфата натрия, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор фосфата натрия, а также набор следующих реактивов: водные растворы гидроксида калия, нитрата серебра, хлорида бария, порошкообразный гидроксид калия и металлический цинк.
2) Вычислите объём аммиака (н. у.), необходимого для полной нейтрализации соляной кислоты массой 130 г и массовой долей  10%.
10%.
3) Используя метод электронного баланса, составьте уравнение реакции по схеме:

Определите окислитель и восстановитель
12. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства бромида бария, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор бромида бария, а также набор следующих реактивов: водные растворы хлорида калия, нитрата магния, нитрата серебра, сульфата натрия и соляной кислоты.
2) В 85 г соляной кислоты с массовой долей  15% поместили избыток цинка. Вычислите объём выделившегося газа (н. у.).
15% поместили избыток цинка. Вычислите объём выделившегося газа (н. у.).
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
13. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства хлорида кальция, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор хлорида кальция, а также набор следующих реактивов: водные растворы карбоната калия, нитрата магния, нитрата серебра, гидроксида бария и металлический цинк.
2) К 90 г раствора хлорида бария с массовой долей растворённого вещества 15% добавили избыток раствора серной кислоты. Вычислите массу выпавшего осадка.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
14. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата аммония, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор сульфата аммония, а также набор следующих реактивов: водные растворы карбоната калия, хлорида бария, фосфата натрия, гидроксида калия и соляной кислоты.
2) При взаимодействии 251 г раствора нитрата свинца с небольшим избытком раствора иодида калия выпало 13,45 г осадка. Рассчитайте массовую долю нитрата свинца в исходном растворе
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
15. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства нитрата меди(II), и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор нитрата меди(II) и набор следующих реактивов: водные растворы сульфата калия, хлорида бария, ацетата магния, гидроксида калия, а также спиртовая горелка.
2) При растворении 9г технического цинка в избытке разбавленной соляной кислоты выделилось 2,1 л (н. у.) водорода. Определите массовую долю примесей в этом образце цинка.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
16. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства бромида магния, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор бромида магния, а также набор следующих реактивов: водные растворы нитрата натрия, нитрата серебра, гидроксида калия, хлорида натрия и бромида натрия.
2) Рассчитайте массу осадка, который выпадет при взаимодействии избытка карбоната калия с 25 г раствора нитрата бария с массовой долей последнего 23%.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
17. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства фосфата аммония, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор фосфата аммония, а также набор следующих реактивов: водные растворы хлорида натрия, хлорида магния, гидроксида натрия, сульфата калия и бромида калия.
2) При взаимодействии 52 г руды, содержащей карбонат железа(II), с избытком соляной кислоты выделилось 4,52 л углекислого газа. Определите массовую долю карбоната железа в руде.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
18. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфида натрия, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор сульфида натрия, а также набор следующих реактивов: водные растворы нитрата свинца(II), нитрата аммония, соляной кислоты, сульфата калия и фосфата калия.
2) При растворении 220 г известняка в избытке азотной кислоты выделилось 35,22 л (н. у.) углекислого газа. Определите массовую долю карбоната кальция в данном образце известняка.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
19. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата железа(III), и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор сульфата железа(III) и набор следующих реактивов: водные растворы гидроксида натрия, нитрата натрия, бромида магния, хлорида цинка, хлорида кальция.
2) Определите объём (н. у.) углекислого газа, выделяющегося при растворении 230 г известняка, содержащего 95% карбоната кальция, в избытке азотной кислоты.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
20.вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата железа(II), и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор сульфата железа(II) и набор следующих реактивов: водные растворы гидроксида натрия, нитрата натрия, бромида магния, хлорида цинка и бромид бария.
2) В избытке соляной кислоты растворили 1,620 г руды, содержащей 57% карбоната железа(II). Определите объём углекислого газа, выделившегося при этом.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
21. вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства сульфата магния, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор сульфата магния, а также набор следующих реактивов: цинк, соляная кислота, растворы гидроксида натрия, хлорида бария и нитрата калия.
2) При взаимодействии избытка раствора карбоната калия с 15%-ным раствором нитрата бария выпало 4,5 г осадка. Определить массу взятого для опыта раствора нитрата бария.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой

Определите окислитель и восстановитель
22 вариант
1)Используя только реактивы из приведённого перечня, запишите молекулярные уравнения двух реакций, которые характеризуют химические свойства хлорида алюминия, и укажите признаки их протекания. Разберите с т.зр ТЭД(напишите полные и сокращенные ионные уравнения)
Дан раствор хлорида магния, а также набор следующих реактивов: водные растворы нитрата бария, гидроксида натрия, нитрата серебра и металлический цинк.
2) К раствору силиката калия массой 30 г прилили избыток раствора нитрата кальция. Вычислите массу образовавшегося осадка.
3) Используя метод электронного баланса, расставьте коэффициенты в уравнении реакции, схема которой:
Mg+HCl →MgCl2+H2
Определите окислитель и восстановитель.