Химия
Апреля
Спирты. Метанол и этанол.
До настоящего времени мы изучали простейшие органические соединения — углеводороды. В молекулах углеводородов атомы водорода могут замещаться на атомы других элементов или на группы атомов. Эти группы атомов придают соединению определенные свойства и называются функциональными группами.
Мы рассмотрим органические соединения со следующими функциональными группами, в которые входят атомы кислорода.
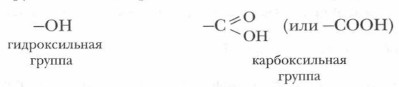
Их называют кислородсодержащими органическими соединениями.
Спирты — это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильную группу. Гидроксильная группа —ОН является функциональной группой спиртов, которая определяет их свойства.
Спирты по количеству ОН-групп подразделяются на одноатомные и многоатомные:
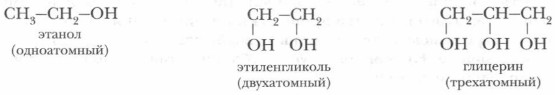
Предельные одноатомные спирты. Рассмотрим предельные одноатомные спирты, общая формула которых СnН2n+1ОН, или R—ОН, где R — предельный радикал (СnН2n+1).
По международной номенклатуре названия спиртов производят от названий соответствующих углеводородов, прибавляя суффикс -ол, в случае необходимости указывают номер атома углерода, с которым связана группа —ОН.
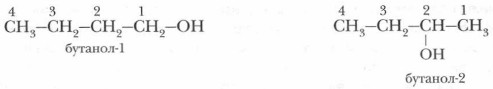
По рациональной номенклатуре — от названий соответствующих радикалов — метиловый спирт СН3ОН и др. (табл. 31).
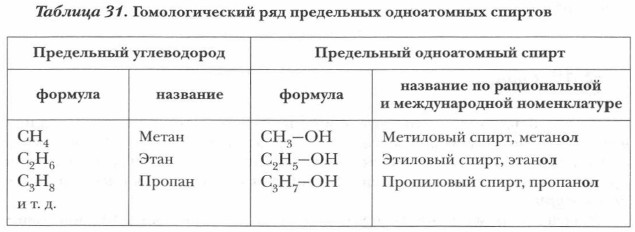
Широкое распространение получили первые представители гомологического ряда спиртов — метиловый (метанол) и этиловый (этанол) спирты.
Физические свойства. Метанол СH3ОН — бесцветная жидкость со своеобразным запахом, хорошо растворяется в воде, кипит при температуре 67,7 °С. Этанол C2H5OH— бесцветная жидкость со своеобразным запахом, легче воды (плотность 0,78 г/см3), смешивается с водой (в любых соотношениях), кипит при температуре +78 °С.
|
|
| Спирты токсичны. Метанол — это яд! Употребление даже небольшого количества этого вещества приводит к потере зрения и к смерти. Этанол быстро всасывается в кровь и возбуждающе действует на организм человека. Неумеренное употребление этанола может привести к смертельному исходу. |
Метанол СН3ОН широко используется в органическом синтезе. Его получают из синтез-газа:
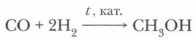
Наиболее широкое применение находит этанол С2Н5ОН. Его используют как растворитель и как сырье в органическом синтезе, в фармацевтической промышленности и медицине, а также как горючее. Этанол образуется при спиртовом брожении глюкозы в присутствии дрожжей:
C6H12O6 → 2С2Н5ОН + 2СO2↑
Так получают пищевой спирт. Для технических целей этиловый спирт получают реакцией гидратации этилена при нагревании и повышенном давлении с участием катализатора:
Н2ССН2 + Н2О → Н3С-СН2ОН
Рассмотрим химические свойства спиртов на примере этанола.
Спирты
До настоящего времени мы изучали простейшие органические соединения — углеводороды. В молекулах углеводородов атомы водорода могут замещаться на атомы других элементов или на группы атомов. Эти группы атомов придают соединению определенные свойства и называются функциональными группами.
Мы рассмотрим органические соединения со следующими функциональными группами, в которые входят атомы кислорода.
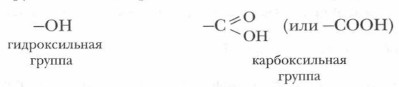
Их называют кислородсодержащими органическими соединениями.
Спирты — это производные углеводородов, в молекулах которых один или несколько атомов водорода замещены на гидроксильную группу. Гидроксильная группа —ОН является функциональной группой спиртов, которая определяет их свойства.
|
|
Спирты по количеству ОН-групп подразделяются на одноатомные и многоатомные:
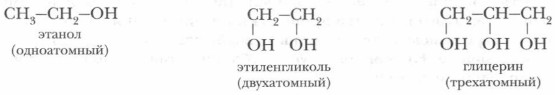
Предельные одноатомные спирты. Рассмотрим предельные одноатомные спирты, общая формула которых СnН2n+1ОН, или R—ОН, где R — предельный радикал (СnН2n+1).
По международной номенклатуре названия спиртов производят от названий соответствующих углеводородов, прибавляя суффикс -ол, в случае необходимости указывают номер атома углерода, с которым связана группа —ОН.
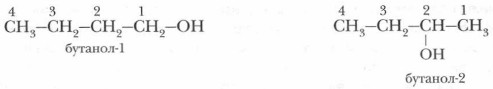
По рациональной номенклатуре — от названий соответствующих радикалов — метиловый спирт СН3ОН и др. (табл. 31).

 Какое влияние оказывают предельные одноатомные спирты на человеческий организм?
Какое влияние оказывают предельные одноатомные спирты на человеческий организм?
От чего зависят общие свойства спиртов?
Широкое распространение получили первые представители гомологического ряда спиртов — метиловый (метанол) и этиловый (этанол) спирты.
Физические свойства спиртов.
Метанол СH3ОН — бесцветная жидкость со своеобразным запахом, хорошо растворяется в воде, кипит при температуре 67,7 °С.
Этанол — бесцветная жидкость со своеобразным запахом, легче воды (плотность 0,78 г/см3), смешивается с водой (в любых соотношениях), кипит при температуре +78 °С.
| Спирты токсичны. Метанол — это яд! Употребление даже небольшого количества этого вещества приводит к потере зрения и к смерти. Этанол быстро всасывается в кровь и возбуждающе действует на организм человека. Неумеренное употребление этанола может привести к смертельному исходу. |
Метанол СН3ОН широко используется в органическом синтезе. Его получают из синтез-газа:
|
|
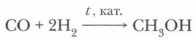
Наиболее широкое применение находит этанол С2Н5ОН. Его используют как растворитель и как сырье в органическом синтезе, в фармацевтической промышленности и медицине, а также как горючее. Этанол образуется при спиртовом брожении глюкозы в присутствии дрожжей:
C6H12O6 → 2С2Н5ОН + 2СO2↑
Так получают пищевой спирт. Для технических целей этиловый спирт получают реакцией гидратации этилена при нагревании и повышенном давлении с участием катализатора:
Н2ССН2 + Н2О → Н3С-СН2ОН
Рассмотрим химические свойства спиртов на примере этанола.