Этот выбор, даже для случая, когда все подлежащие разделению белки известны и, более того, имеются в чистом виде, оказывается делом непростым, требующим немалого опыта, понимания физических процессов, лежащих в основе фракционирования и даже определенной интуиции. Очень рискованно (с точки зрения потери ценного препарата) пытаться слепо повторять условия хроматографии, описанные в научной литературе даже для точно такого же или очень похожего случая. Реальные характеристики ионообменника той же марки (они варьируют от партии к партии) или используемых реактивов могут оказаться иными. Равно как и особенности исходных препаратов. Приняв к сведению описанную процедуру, исследователь должен сам продумать и спланировать свой хроматографический эксперимент. Сюда войдут, как минимум:
1. Выбор ионообменника (его силы, размера гранул, пористости).
2. Выбор геометрии колонки (длина и диаметр).
3. Выбор рН буфера с позиций как наиболее выгодных условий фракционирования, так и сохранения биологической активности всех белков смеси, например ферментов.
4. Выбор концентраций соли (контрионов) в элюенте.
5. Выбор типа элюции: изократической (с неизменной концентрацией соли), ступенчатой или градиентной (и какой формы градиента!)
6. Выбор скорости элюции.
Все эти условия надо подбирать одновременно, с учетом их взаимосвязи с целью оптимизации результатов фракционирования. Было бы слишком громоздко излагать здесь способы выбора каждого из названных параметров хроматографического процесса. Для иллюстрации остановлюсь на пунктах 4 и 5 — выборе концентрации соли и способах манипуляции этой концентрацией.
Выше было показано, что продвижение хроматографических зон связывания белков по колонке обусловлено, в частности, их десорбцией в местах первоначального и всех последующих закреплений на матрице в гранулах. За счет десорбции восстанавливается динамическое равновесие концентраций молекул в неподвижной и подвижной фазах слоя гранул, нарушенное вытеканием элюента, окружавшего этот слой. Десорбция первоначально сор-бированных молекул белка определяется концентрацией соля в жидкости внутри гранул. Если она слишком мала, то десорбции практически не происходит. Наоборот — открытые ионогенние группы матрицы как бы «высасывают» из элюента и закрепляют на себе молекулы белка. Если же концентрация соли в элюенте (а значит и внутри гранул) слишком велика, то практически все молекулы белка десорбируются с матрицы в жидкую среду, их концентрации в неподвижной и подвижной фазах уравниваются, как при гель-фильтрации.
|
|
Имея это в виду проведем мысленно следующий предварительный опыт. Выбранный ионообменник, уравновешенный уже выбранным буфером разольем равными порциями в 10 пробирок. Гранулы обменника, естественно, сядут на дно. Затем серией «декантаций«(т. е. сливом надосадочной жидкости, заменой ее на тот же буфер, но с определенной концентрацией соли, встряхиванием, осаждением — и так несколько раз) добиваемся того, чтобы концентрация соли внутри гранул постепенно увеличивалась от первой пробирки к десятой в определенных пределах (их придется подобрать для каждого белка). Затем во все пробирки внесем одинаковое количество концентрированного водного раствора одного из белков, входящих в состав подлежащей фракционированию смеси. Встряхиваем пробирки, даем отстояться осадку и по ультрафиолетовому поглощению (или ферментативной активности) оцениваем концентрацию белка в каждом из десяти супернатантов.
|
|
Находим первую пробирку, в супернатанте которой наш белок только-только появляется. Тем самым определяем концентрацию соли, при которой динамическому равновесию соответствует минимальная десорбция белка с матрицы. В последующих пробирках по мере увеличения концентрации соли, белка будет становиться все больше — десорбция при установлении динамл-ческого равновесия будет все значительнее. Наконец, придем к такой ситуации, когда концентрация белка в супернатанте окажется максимальной и при дальнейшем увеличении концентрации соли возрастать уже не будет. Концентрация соли в первой из этих пробирок укажет момент полной десорбции белка с матрзицы. В процентах от этой концентрации оценим и степень десорбции в промежуточных точках нашего анализа и построим зависимость процента десорбции данного белка от концентрации соли в условиях динамического равновесия. То же самое проделаем для всех остальных белков будущей смеси и получим серию кривых такого типа, как показана на рис.
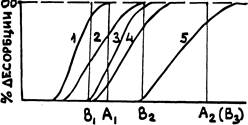
Рис.
Рассматривая эту серию кривых, можно заключить, что при изократической элюции буфером с неизменной солевой концентрацией, например, соответствующей точке Ар можно надеяться разделить белки 1—4. Белок 1 будет сразу же полностью десорбиpoвать и выйдет в первую очередь — с током элюента. За ним последуют в порядке возрастания прочности сорбции белки 2, 3 и 4. Зона связывания каждого последующего из них будет двигаться по колонке медленнее, чем зона предыдущего белка. Белок 5 в этих условиях вовсе не выйдет из зоны первоначального нанесения препарата на колонку. Его можно снять отдельно, увеличив концентрацию соли в элюенте до значения Ag. Это уже будет «двухступенчатая» элюция.
|
|
Если окажется, что при концентрации Аg белки 3 и 4 разделяются плохо, можно воспользоваться трехступенчатой элюцией, выбирая концентрации соли в точках Вр Bg и Bg. Тогда сначала выйдут хорошо разделившиеся белки 1 и 2, затем также неплохо разделенные белки 3 и 4 и, наконец, белок 5.
Литература:
1 Курашвили Л.В., Бобылева Л.Н. Определение триглицеридов во фракции липопротеидов высокой плотности /Лабораторное дело. - N 7. - 1991. - С.7576.
2 Курашвили Л.В., Владимирова А.А. Содержание триглицеридов в ЛПВП у больных ишемической болезнью сердца //Кардиология. - 7-8. - 1992. - С.35-38.
3 Курашвили Л.В., Волков А.С. Прогностическая значимость определения холестерина в фракции липопротеидов высокой плотности у доноров крови // Гематология и трансфузиология. - N 5. - 1993. - С.39-41.