Согласно квантовой теории энергия электронов в атоме может принимать не любые, а только некоторые определенные значения, образующие дискретный набор. Состояния с различными значениями энергии называются уровнями. Переход электрона с более высокого энергетического уровня на более низкий сопровождается появлением отдельной линии в спектре атома. Вся совокупность линий образует линейчатый спектр атома, который можно разделить на группы линий (серий). Каждая серия есть результат перехода электрона из всевозможных более высоких уровней энергии на один фиксированный с меньшей энергией. В видимой области спектра испускания атома водорода находится серия, для которой нижний уровень характеризуется квантовым числом 2. Эта группа линий получила название серия Бальмера.
Частоты испускаемых атомами водорода линий находятся между собой в определенных соотношениях и могут быть выполнены по формуле:
 ,
,
где  и
и  - значения энергии электрона, соответствующие уровням энергии с номерами n и m;
- значения энергии электрона, соответствующие уровням энергии с номерами n и m;
h - постоянная Планка;
nn,m - частота испущенного кванта света.
Для атомной системы, состоящей из ядра и одного электрона (атом водорода), энергия электрона на уровнях n и m может быть записана в виде:
 и
и 
 ,
,
где R – постоянная Ридберга, равная 1,1´107 м-1,
с – скорость распространения электромагнитного излучения в вакууме, равная 3´108 м/с.
Учитывая выражения для энергий уровней n и m, для частоты испускаемого света при переходе электрона с уровня m на уровень с номером n, получим:
 (14.1)
(14.1)
Из этой формулы видно, что все линии спектра атома водорода могут быть объединены в серии. Для водорода основными являются серии:
n = 1 – Лаймана, n = 2 – Бальмера, n = 3 – Пашена, n = 4 – Брэккета, n = 5 – Пфунда.
В данной работе необходимо исследовать серию Бальмера (видимая область спектра) и в частности определить длины волн l линий этой серии. Учитывая, что 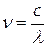 , из выражения (14.I) получим рабочую формулу
, из выражения (14.I) получим рабочую формулу
 .
.
Зная диапазон длин волн видимой области спектра 400нм - 760 нм, меняют значения m  3, и определяют те длины волн, которые входят в этот диапазон.
3, и определяют те длины волн, которые входят в этот диапазон.

Рис.14.1.
Для проведения исследований спектра атомов используется установка, схема которой приведена на рис. 14.1. В работе используется только оптическая система стилометра.
При калибровке барабана монохроматора световой поток от ртутной лампы поступает через щель коллиматорной трубы на линзу L1. Затем параллельный пучок падает на основную часть спектроскопа - призму Р, разлагающую свет по длинам волн. Линза L2 собирает в плоскости щели S1. Если бы лампа излучала волны всевозможных длин, то линии слились бы в сплошной спектр. Ртутная лампа испускает лишь определенные длины волн, поэтому в данной работе наблюдается линейчатый спектр - цветные линии пространственно разделены.
Поворотом призмы Р в щель S2 можно поместить любую цветную линию. Поворот этот осуществляется при помощи барабана с делениями. Каждому положению барабана соответствует определенная S2длина волны выходящего из щели S2 света. Зависимость длины волны l света в щели S2 от делений барабана N призмы Р и есть градуировочный график спектроскопа. По этому графику можно определить длины волн в спектре излучения любого другого источника света, определив по барабану соответствующее значениеN.