Грипп занимает одно из ведущих мест в структуре инфекционной патологии человека. Во всех странах мира основной экономический ущерб от инфекционных заболеваний наносят именно грипп и острые респираторные вирусные инфекции (ОРВИ). В России на их долю приходится примерно 90% всей регистрируемой инфекционной заболеваемости. По данным официальной статистики в РФ ежегодно регистрируется от 900 тысяч до 3,5 млн случаев гриппа, при этом умирает от 20 до 53 тысяч человек в год.
Заболеваемость гриппом существенно колеблется в разное время года, увеличиваясь, как правило, в осенне-зимнее время. Тем не менее, случаи гриппа могут регистрироваться даже в межэпидемический период. История изучения гриппа уходит своими корнями еще в средние века. Первая эпидемия, о которой мы знаем, имела место в 1889-1890 гг. и была вызвана подтипом вируса гриппа А (H2N8). Благодаря уникальным свойствам вируса гриппа А и прежде всего его способности к изменению антигенной структуры, специфический иммунитет, приобретенный после перенесенного заболевания, практически не защищает от инфицирования новым штаммом вируса гриппа. Во время ежегодных вспышек и эпидемий гриппа и других ОРВИ заболевает каждый 10-й взрослый и каждый 3-й ребенок. По данным ВОЗ, во время сезонных эпидемий, вызванных различными вирусами гриппа, в мире ежегодно умирают от 250 до 500 тысяч (большинство из них в возрасте старше 65 лет), причем в некоторые годы число смертей может достигать миллиона. Пандемии гриппа возникают каждые 30-40 лет и характеризуются высокими показателями заболеваемости и смертности.
В настоящее время существуют различные противовирусные препараты для лечения гриппа. Их можно разделить на три группы: этиотропные - ингибиторы нейраминидазы (осельтамивир, занамивир, перамивир), блокатор ионного канала, образованного белком М2 (Ремантадин, Альгирем), ингибиторы NP-белка (Ингавирин), ингибитор гемагглютинина (Арбидол); препараты интерферона (рекомбинантные альфа/гамма-интерфероны); индукторы интерферонов (Кагоцел, Амиксин, Циклоферон). Наиболее эффективна противовирусная терапия, начатая в первые 24-48 часов от начала заболевания, которая позволяет существенно сократить продолжительность лихорадки и других клинических симптомов заболевания.
|
|
Именно поэтому необходимость точной и своевременной диагностики гриппа не вызывает сомнений. На сегодняшний день в клинической практике чаще всего используется метод прямой иммунофлуоресценции (ИФ) и, намного реже, метод полимеразной цепной реакции (ПЦР).
Как известно, метод ИФ предложил А. Кунс еще в 1941 г. Реакция ИФ основана на связывании антигена с антителом, конъюгированным с флуоресцентной меткой (флуорохромом, например, флюоресцеина изотиоционатом (FITС), тетраметилродамин изотиоционатом (TRITC) и др.). Сегодня для проведения этой реакции используют как поликлональные сыворотки, так и моноклональные антитела. Учет результатов реакции осуществляется с помощью люминесцентного микроскопа, в оптическую систему которого устанавливается набор светофильтров, обеспечивающих освещение препарата ультрафиолетовым или сине-фиолетовым светом с заданной длиной волны.
Метод ПЦР был разработан сотрудником фирмы Cetus K. Mullis в 1983 г. Существуют различные модификации этой реакции. В настоящее время используют ПЦР с обратной транскрипцией в режиме реального времени (ОТ-ПЦР), суть которой заключается в амплификации определенных участков ДНК в процессе повторяющихся температурных циклов [8, 9].
|
|
Настоящее исследование посвящено сравнительному анализу диагностического значения методов прямой ИФ и ОТ-ПЦР с целью оптимизации диагностических подходов в тактике ведения больных острыми респираторными заболеваниями и гриппом.
Материалы и методы
Всего в исследование включен 81 мужчина и 59 женщин (140 пациентов), поступавших в отделения острых респираторных вирусных инфекций ГКУЗ ИКБ № 1 Департамента здравоохранения г. Москвы в состоянии средней тяжести с направительным диагнозом: "ОРВИ" либо "Грипп". Средний возраст больных - 35,5 ± 1,6 года (от 15 до 87 лет). Критериями включения пациентов в исследование были: наличие симптомов гриппа и ОРВИ (повышение температуры тела, симптомы интоксикации и катарального воспаления дыхательных путей); обследование двумя методами для подтверждения гриппа (прямая ИФ и ПЦР) в первые двое суток от момента поступления больного в стационар. При этом материал, взятый от больного для проведения этих исследований, должен был содержать достаточное количество клеток эпителия носоглотки для анализа. Критериями исключения из исследования были: наличие хронической обструктивной болезни легких, беременность.
Всем пациентам, включенным в исследование, проводилось стандартное общеклиническое обследование: сбор анамнеза заболевания, объективный осмотр, анализ клинической картины в сопоставлении с данными лабораторно-инструментальных методов исследования (общие анализы крови и мочи, рентгенологическое исследование органов грудной клетки). Для оценки степени дыхательной недостаточности больным проводилась пульсоксиметрия. При наличии у пациента пневмонии по данным рентгенологического исследования органов грудной клетки дополнительно назначался биохимический анализ крови (определение уровней аланинаминотрансферазы (АлАТ), аспартатаминотрансферазы (АсАТ), мочевины, креатинина, креатининфосфокиназы), а также анализ крови для оценки кислотно-основного состояния и электролитов.
|
|
Молекулярно-генетическое исследование осуществлялось при помощи ОТ-ПЦР с гибридизационно-флуоресцентной детекцией продуктов амплификации для выявления генетического материала вирусов гриппа А (сезонного), гриппа А (H1N1) pdm09, гриппа В в эпителии носоглотки/ротоглотки при помощи тест-систем "АмплиСенс®" с аналитической чувствительностью - 1000 микроорганизмов в 1 мл биологического материала.
Иммунологическое исследование выполнялось при помощи метода прямой ИФ. Диагностикум представляет собой специфические моноклональные антитела (иммуноглобулины), меченые флуоресцеинизотиоцианатом. В работе использовались серии диагностикумов производства ФГБУ НИИ гриппа (г. Санкт-Петербург), рабочее разведение диагностикумов было не ниже 1:16. Анализ мазков-отпечатков из носоглотки проводился с помощью люминесцентного микроскопа "Биомед-6" (Россия).
Результаты
Для проведения сравнительного анализа методов прямой ИФ и ОТ-ПЦР группа больных (n = 140), в которой были применены одновременно эти две методики с целью уточнения этиологии основного заболевания, была разделена на три подгруппы: 1-я подгруппа - пациенты, у которых диагностика гриппа двумя методиками проводились в один день; 2-я подгруппа - пациенты, которым ПЦР было выполнено раньше метода ИФ на 1-2 суток; 3-я подгруппа - пациенты, которым метод прямой ИФ был проведен раньше ПЦР на 1-2 суток. Результаты исследования эпителия носоглотки методами прямой ИФ и ОТ-ПЦР у 140 больных, включенных в исследование, представлены в табл. 1-3.
Выполнено сравнение частоты регистрации четырех комбинаций (профилей) результатов тестов прямой ИФ и ОТ-ПЦР: ИФ"+"/ПЦР"+", ИФ"-"/ПЦР"+", ИФ"+"/ПЦР"-", ИФ"-"/ПЦР"-".
При сравнительном анализе результатов лабораторного исследования в группе пациентов (n = 20), которым ОТ-ПЦР и исследование методом прямой ИФ проводили в один день и в первые 3 дня от начала заболевания, частота выявления профиля ИФ"-"/ПЦР"+" была самой высокой и достоверно отличалась от частоты выявления профилей ИФ"+"/ПЦР"+" и ИФ"+"/ПЦР"-" (p = 0,0005 и p = 0,0019 соответственно).
При сравнительном анализе результатов лабораторного исследования в группе пациентов (n = 37), которым ОТ-ПЦР и исследование методом прямой ИФ проводили в один день и на 4-5 сутки от начала заболевания, частота выявления профиля ИФ"-"/ПЦР"+" была также самой высокой и достоверно отличалась от частоты выявления профилей ИФ"+"/ПЦР"+" и ИФ"+"/ПЦР"-" (p = 0,0001 и p = 0,0001 соответственно).
При сравнительном анализе результатов лабораторного исследования в группе пациентов (n = 11), которым ОТ-ПЦР и исследование методом прямой ИФ проводили в один день и позже 5 суток от начала заболевания, частота выявления профиля ИФ"-"/ПЦР"+" была также самой высокой, но достоверно отличалась только от частоты выявления профиля ИФ"+"/ПЦР"-" (p = 0,0078), в то время как достоверной разницы с частотой выявления профиля ИФ"+"/ПЦР"+" не выявлено (p = 0,0868).
Как видно из табл. 1, в группе больных (n = 20), которым ОТ-ПЦР и исследование методом прямой ИФ проводили в один день и в первые 3 дня от начала заболевания, грипп был лабораторно подтвержден тем или иным методом у 17 (85%) пациентов, при этом большая часть (82%, 14/17) положительных результатов получена при использовании метода ОТ-ПЦР. Совпадение результатов исследований методов прямой ИФ и ОТ-ПЦР регистрировалось только в 11,8% (2/17) случаев, в то время как в 70,6% (12/17) случаев методом прямой ИФ антигены вируса гриппа выявить не удалось.
В группе больных, которым ОТ-ПЦР и исследование методом прямой ИФ проводили в один день и на 4-5 сутки от начала заболевания, грипп был лабораторно подтвержден тем или иным методом у 28 (75,7%) пациентов, при этом большая часть положительных результатов (92,9%, 26/28) также была получена при использовании метода ОТ-ПЦР. Совпадение результатов исследований методов прямой ИФ и ОТ-ПЦР регистрировалось в 10,7% (3/28) случаев, а в 82,1% (23/28) выявить антигены вируса гриппа методом прямой ИФ не удалось.
В группе больных (n = 11), которым ОТ-ПЦР и исследование методом прямой ИФ проводили в один день и позже 5 суток от начала заболевания, грипп был лабораторно подтвержден тем или иным методом у всех пациентов. При использовании метода ОТ-ПЦР этиология была установлена у 90,9% (10/11) больных, совпадение результатов двух методик регистрировалось в 3 (27,3%) случаях.
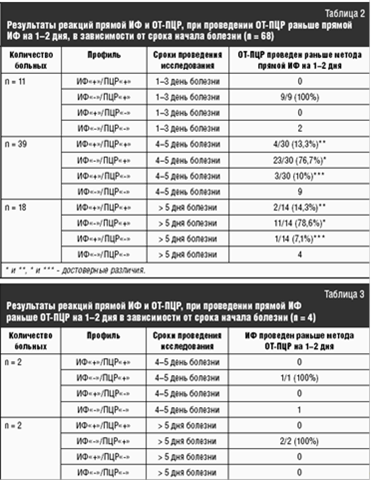
При сравнительном анализе результатов лабораторного исследования в группе пациентов (n = 11), которым исследование ОТ-ПЦР было выполнено на 1-2 дня раньше прямой ИФ и в 1-3 дня от начала болезни, грипп был подтвержден у 9 пациентов, и только методом ОТ-ПЦР в 100% случаев (профиль ИФ"-"/ПЦР"+").
При сравнительном анализе результатов лабораторного исследования в группе пациентов (n = 40), которым ОТ-ПЦР было проведено раньше исследования методом прямой ИФ на 1-2 дня и на 4-5 сутки от начала заболевания, частота выявления профиля ИФ"-"/ПЦР"+" была самой высокой и достоверно отличалась от частоты выявления профилей ИФ"+"/ПЦР"+" и ИФ"+"/ПЦР"-" (p = 0,0001 и p = 0,0001 соответственно).
При сравнительном анализе результатов лабораторного исследования в группе пациентов (n = 18), которым ОТ-ПЦР было проведено раньше исследования методом прямой ИФ на 1-2 дня и позже 5 суток от начала заболевания, частота выявления профиля ИФ"-"/ПЦР"+" была также самой высокой и достоверно отличалась от частоты выявления профилей ИФ"+"/ПЦР"+" и ИФ"+"/ПЦР"-" (p = 0,0006 и p = 0,0002 соответственно).
Как видно из табл. 2, в группе пациентов (n = 11), которым ОТ-ПЦР было проведено раньше исследования методом прямой ИФ на 1-2 дня и на 1-3 сутки от начала заболевания, при помощи последнего выявить антигены вируса гриппа не удалось ни у одного пациента, в то время как при использовании метода ОТ-ПЦР генетический материал вируса гриппа был выявлен у 9 (81,8%) больных.
В группе больных (n = 39), которым ОТ-ПЦР было проведено раньше исследования методом прямой ИФ на 1-2 дня и на 4-5 сутки от момента заболевания, грипп был лабораторно подтвержден тем или иным методом в 76,9% случаев, при этом большинство положительных результатов (90%, 27/30) получено при использовании метода ОТ-ПЦР. Совпадение результатов исследований методов прямой ИФ и ОТ-ПЦР регистрировалось лишь в 4 (13,3%) случаях.
В группе пациентов (n = 18), которым ОТ-ПЦР было проведено раньше исследования методом прямой ИФ на 1-2 дня и позже 5 суток от начала заболевания, грипп лабораторно подтвержден тем или иным методом у 77,8% (14/17) больных, при этом большинство положительных результатов также было получено при использовании метода ОТ-ПЦР. Совпадение результатов исследований методов прямой ИФ и ОТ-ПЦР регистрировалось в 14,3% (2/14) случаев.
В табл. 3 представлены результаты пациентов, у которых исследование методом прямой ИФ было сделано раньше ОТ-ПЦР и обследованных позже 3-го дня болезни. Из трех пациентов, обследованных на 4-й день и позже, грипп был подтвержден в 100% случаев только методом ОТ-ПЦР (профиль ИФ"-"/ПЦР"+").
В целом, среди всех обследованных, независимо от дня болезни, на который выполнялось исследование, были пациенты (n = 10), у которых при помощи метода прямой ИФ выявлялись антигены вируса гриппа, в то время как методом ОТ-ПЦР выделить генетический материал вируса не удавалось (профиль ИФ"+"/ПЦР"-"). Такое расхождение результатов обследования наблюдалось в 7,1-17,6% случаев, не прослеживалось связи указанного профиля с днем болезни, на который проводилось обследование, однако в группе больных, у которых обследование методом прямой ИФ применялось раньше ОТ-ПЦР, таких пациентов не было.
Заключение
Среди всех больных с диагностированным гриппом доля положительных результатов ОТ-ПЦР-исследования составляет от 77,8% до 100%. При этом основную группу (78,9%, 90/114) составили пациенты, у которых методом ОТ-ПЦР был выявлен генетический материал вируса гриппа, в то время как антигены вируса гриппа при проведении прямой ИФ идентифицировать не удавалось. Доля лабораторно-подтвержденных случаев гриппа методом прямой ИФ (среди всех подтвержденных случаев как методом прямой ИФ, так и ОТ-ПЦР) составила 21,1%. Полученные результаты свидетельствуют о больших диагностических возможностях метода ОТ-ПЦР у больных гриппом, и что немаловажно, независимо от дня болезни при наличии клинической картины острого заболевания.
Меньшие диагностические возможности метода прямой ИФ объясняются самим механизмом реакции. Антитела взаимодействуют с антигеном в местах их локализации. Эти места выявляют при помощи метки, связанной с антителами. Это наиболее простой метод визуализации, однако чувствительность его крайне низкая, так как на одну молекулу искомого антигена будет приходиться одно меченое антитело. Достоинством метода ОТ-ПЦР является необязательность условия наличия большого количества возбудителя в клетках эпителия, так как сам метод предусматривает увеличение количества копий ДНК/РНК возбудителя (амплификация) с последующей его детекцией. Так как оба метода используются преимущественно для ранней диагностики гриппа, что принципиально для своевременного назначения противовирусной терапии, то, безусловно, клиницист отдаст свое предпочтение тому методу, который позволяет это сделать с наибольшей вероятностью.
Также необходимо учитывать, что большая разница в частоте лабораторного подтверждения гриппа, свидетельствующая о низкой диагностической возможности метода прямой ИФ, может быть объяснена вероятностью перекрестных реакций, быстрым разрушением флуоресцентной метки, субъективностью оценки результатов реакции. Последний фактор зависит непосредственно от квалификации врача-лаборанта, проводящего исследование. Помимо этого проведение прямой ИФ - весьма трудоемкий неавтоматизированный процесс, требующий больших временных затрат от специалиста. По сравнению с методом прямой ИФ ОТ-ПЦР является автоматизированным высокочувствительным методом, дающим возможность выявлять даже единичные копии ДНК/РНК возбудителя на поздних сроках от начала заболевания. ОТ-ПЦР обладает высокой специфичностью, что обусловлено определением участка гена, характерного только для данного возбудителя.
Оптимальные сроки обследования - первые 5 дней болезни, однако при наличии клинической симптоматики гриппа метод ОТ-ПЦР информативен и на более поздних сроках заболевания. Работа выполнена в рамках гранта Президента Российской Федерации для государственной поддержки ведущих научных школ Российской Федерации (протокол № 1 от 19 марта 2010 г.) по соглашению № 16.120.11.5354-НШ от 01.02.2012 г.
Литература
. Салтыкова Т. С. Заболеваемость гриппом и отсроченная смертность у лиц старше 60 лет. Автореф. дис. … канд. мед. наук. М., 2010.
. Климова Е. А., Ющук Н. Д., Кареткина Г. Н.и др. Исходы тяжелого течения пандемического гриппа А/H1N1/2009 // Терапевтический архив. 2010. № 11, с. 15-18.
. Петров В. И., Ленева И. А., Недогода С. В. Применение отечественного противовирусного препарата с позиций доказательной медицины // Лечащий Врач. 2011. № 1, с. 71-79.
. Теоретические основы полимеразной цепной реакции. Методическое пособие. "НПФ ДНК-технология". М., 2010. Режим доступа: https://www.twirpx.com/file/454057/. Дата обращения: 01.11.14г
5. Heid C. A.Real-time quantitative PCR // Genome Res. 2012. № 6, p. 986-994.
6. Екимов А. Н., Шипулин Г. А., Бочкарев Е. Г., Рюмин Д. В.Новейшие технологии в генодиагностике: полимеразная цепная реакция в реальном времени (Real-Time PCR) Режим доступа: https://www.pcr.ru/bibliogr/articles/article_18.htm. Дата обращения: 21.10.14г
7. Статьи. ПЦР-анализ. Режим доступа: https://mirzdorovja.by/articles/77-prc-analis. Дата обращения: 04.11.14г
. Глик Б., Пастренак Дж. Молекулярная биотехнология. Принципы и применение - Москва: Мир, 2009.
. Анализ ПЦР. Полимеразно-цепная реакция. Метод ДНК-Диагностики. Режим доступа: https://www.pcr.su. Дата обращения: 21.10.14г
. Щербо С.Н., Макаров В.Б. Клиническая лабораторная диагностика. - 2010.
. Гинцбург А.Л. Микробиология, иммунология и вирусология. - 2009.
12. Падутов В.Е., Баранов О.Ю., Воропаев Е.В. Методы молекулярно - генетического анализа. - Мн.: Юнипол, 2010. - 176 с.
13. ПЦР "в реальном времени"/ Ребриков Д.В., Саматов Г.А., Трофимов Д.Ю. и др.; под ред. д. б. н. Д.В. Ребрикова; предисл. Л.А. Остермана и акад. РАН и РАСХН Е.Д. Свердлова; 2-е изд., испр. и доп. - М.: БИНОМ. Лаборатория знаний, 2009. - 223 с.
..Патрушев Л.И. Искусственные генетические системы. - М.: Наука, 2009. - В 2 т
. Б. Глик, Дж. Пастернак Молекулярная биотехнология. Принципы и применение 589 стр., 2009 г.
. Методические рекомендации по проведению работ в диагностических лабораториях, использующих метод полимеразной цепной реакции от 22.06 2011г.
. Щербо С.Н. ПЦР в клинической лабораторной диагностике: реальности и перспективы //Справочник заведующего КДЛ 2010. №10 с. 45-48
. Тарасенко И.М. Правила организации работы КДЛ с патогенными биологическими агентами // Справочник заведующего КДЛ 2010. №6 с.37-40.
. Херсонская А.М. Современные методы клинической диагностики: ПЦР в режиме реального времени // Справочник заведующего КДЛ 2010. №11 с.31-36
. 5. Чухловин.А.Б. Метод ПЦР в клинической лабораторной диагностике // Справочник заведующего КДЛ. 2011. №4 с.46-50
. 6. Херсонская А.М., Амон Е.П. Типовые ошибки при диагностике методом ПЦР // Справочник заведующего КДЛ 2010. №5 с.30-36
Приложение

Рисунок 3. ДНК-полимераза.

Рисунок 4. Схематическое изображение первого цикла ПЦР. (1) Денатурация при 94-96 °C. (2) Отжиг при 68 °C (например). (3) Элонгация при 72 °C (P=полимераза). (4) Закончен первый цикл. Две получившиеся ДНК-цепи служат матрицей для следующего цикла, поэтому количество матричной ДНК в ходе каждого цикла удваивается.