Кондуктометрия – электрохимический метод анализа, связывающий электропроводность раствора с его составом. Электрическая проводимость растворов обусловлена наличием в них носителей электрического заряда – ионов. Все растворимые соли диссоциируют на ионы, поэтому проводимость ионных раствором значительно выше молекулярных.
Для определения хлоридов в объектах окружающей среды прямая кондуктометрия применяться не может. Прямая кондуктометрия заключается в определении электропроводности раствора содержащего определяемый компонент. Линейный характер носит только электропроводность индивидуальных растворов, либо смесей с точно известными концентрациями. Объекты окружающей среды кроме хлорид-ионов, содержат и другие, влияющие на электропроводность раствора. По этой причине для определения хлоридов используется метод кондуктометрического титрования.
Кондуктометрическое титрование используется при определении индивидуальных веществ и анализе разнообразных смесей. Точку эквивалентности при кондуктометрическом титровании определяют по изменению электропроводности раствора. Электропроводность измеряют после добавления каждой порции титранта. Зависимость электропроводности раствора от количества добавленного титранта изображают графически. Полученный график называют кривой кондуктометрического титрования. Кондуктометрические кривые имеют излом, соответствующий точке эквивалентности.
Кривые подобного типа могут быть использованы для аналитических целей только в том случае, если перед точкой зквивалентности наблюдается линейное изменение проводимости.
При титровании следует проводить большое число измерений электропроводности. Для определения точки эквивалентности используют близкие к ней участки кривых.
В методе кондуктометрического титрования могут применяться реакции осаждения:
Ag+ +NО3- + Na+ + Cl- → ↓AgCI + Na+ + NO3-
Изменение состава ионов приводит к изменению электропроводности раствора.
Поскольку реакции осаждения часто протекают не мгновенно, измерение сопротивления раствора при титровании следует проводить после достижения постоянной проводимости.
При кондуктометрическом титровании необходимо, прежде всего, чтобы излом кондуктометрической кривой позволял устанавливать точку эквивалентности с достаточной точностью. Чем острее угол излома, тем выше точность. Когда угол излома очень тупой, установление точки эквивалентности затруднено.
Для кондуктометрического определения хлорид ионов широко применяется титрование нитратом серебра. Однако этот реагент осаждает также Br-, I-, SCN-, СгО4 – С2О42-, тартрат, цитрат и другие анионы. Титрование сопровождается образованием малорастворимых солей серебра. Изменение проводимости растворов при титровании до точки эквивалентности, зависит от сравнительной подвижности осаждаемых анионов и заменяющих их в растворе NO3 ионов. При титровании С1 – (λ0= 76,4), Вr – (λ0=78,1), I – (λ0=78,8) и CrO42 – (λ0= 85) проводимость понижается, так как подвижности этих ионов выше подвижности NO3 – (λ0=71,5). Однако при титровании SCN – (λ0=57,4), наоборот, происходит небольшое повышение проводимости, так как его подвижность ниже подвижности NO3-.
В зависимости от растворимости солей серебра изменяются концентрации титруемых растворов, при которых удается проводить определения с достаточно высокой точностью. Так, титрование хлоридов можно проводить и в очень разбавленных растворах при концентрации С1 – 0,025 мг/мл и меньше. Это титрование используется для определения С1- в питьевой воде. Между тем I – можно титровать, в растворах, концентрация которых больше 0,005 н., а цитраты только при концентрации не ниже 0,1 н.

Z1, Z2, Z3, Z4 – плечи мостика, С – переменная ёмкость, 1 – генератор звуковой частоты, 2 – гальванометр, 3 – электролитическая ячейка.
Рисунок 2.4 – Мостик Уитстона
Электропроводность растворов может быть найдена, если измерить сопротивление электролитической ячейки. Для измерения сопротивления используют переменный ток звуковой частоты, так как постоянный вызывает разложение веществ находящихся в растворе.
Сопротивление раствора определяют путём сравнения с эталонным сопротивлением. Для этого служит мостик Уитстона (рисунок 2.4). Сопротивления Z1, Z2, Z3, Z4 можно подобрать так, чтобы ток в диагонали моста отсутствовал, т.е. сопротивления каждой ветви были пропорциональны. Измеряемое сопротивление определяют по формуле:
Z4= 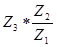
Где Z – сопротивления соответствующих плечей мостика.
3. Анализы объектов на содержание хлорид-иона
1 Определение массовой доли хлоридов в отложениях парового оборудования электростанций
Навеску отложений от 0,5 до 0,8 г, взвешенную на аналитических весах, помещают в химический стакан. Обрабатывают материал 20–30 см3 горячей дистиллированной воды, кислоты и отфильтровывают не растворившийся осадок на плотный беззольный фильтр, собирая фильтрат в мерную колбу вместимостью 100 или 250 см3. Осадок на фильтре промывают горячей дистиллированной водой, собирая промывные воды в ту же колбу. Промывание ведут до исчезновения в фильтрате положительной реакции на присутствие хлорид-иона (проба с AgNO3: несколько капель фильтрата смешивают с раствором, содержащим 1% AgNO3). Из мерной колбы, содержащей фильтрат отбирают пипеткой от 10 до 100 см3 жидкости в зависимости от предполагаемого содержания хлоридов в анализируемом материале.
Аликвоту осветлившегося раствора, отобранную пипеткой, помещают в коническую колбу, приливают 2 см3 концентрированной азотной кислоты и дистиллированной воды до общего объема примерно 100 см3. Затем вводят на кончике ножа несколько кристаллов нитропруссида натрия и три капли раствора метилоранжа. Кристаллы нитропруссида натрия растворяют и титруют окрашенную в оранжево-красный цвет жидкость раствором нитрата ртути II такой концентрации, чтобы каждый миллилитр раствора отвечал 1 мг хлор-иона. Титрование ведут до появления мути в жидкости, которая хорошо заметна при прибавлении одной капли ртутного раствора на фоне черной глянцевой бумаги. Массовую долю хлоридов (%) в пересчете на хлористый натрий получают по формуле:
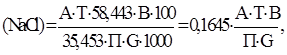 (.1)
(.1)
где А – расход титранта, т.е. раствора азотнокислой ртути, см3;
Т – содержание хлор-ионов, которому соответствует 1 см3 ртутного раствора, мг/см3;
58,443 и 35,453 – молекулярные веса хлористого натрия и хлор-иона.
П – объём аликвотной порции, отобранной для определения, см3;
G – навеска, г;
В-объем мерной колбы, в которую собран фильтрат после отделения кремнекислоты, см3.
2 Определение ионов хлора в нефтяном буровом растворе
Данный тест предназначен для измерения суммарной концентрации растворимых хлоридов в буровом растворе. Источниками ионов хлора в растворе служат хлористый натрий, хлористый кальций и хлористый калий. Для получения правильных результатов титрования фильтрат должен иметь слегка щелочную реакцию – рН ≈ 8,3. В процессе титрования одновременно протекают две химические реакции.
1. Аg+ + Сl-→AgCl
2. 2Аg+ + СгО42-→ Аg2СгO4
Результатом первой реакции (образование хлористого серебра) служит появление белых вкраплений или молочное окрашивание раствора. Образование красного хромата серебра начинается лишь после того, как все ионы хлора оказываются связанными в хлористое серебро. После этого нитрат серебра вступает в реакцию с индикаторным раствором хромата калия, в результате чего образуется хромат серебра. Таким образом, для нормального протекания обеих реакций фильтрат должен иметь слабощелочную реакцию, (рН = 8.3). При высоком рН происходит выпадение осадка окиси серебра.
Оборудование
Шприц со стеклянным наконечником, 5 мл; мерный стакан, 400 мл, стеклянный; магнитная мешалка с «микромешалками»
Реактивы:
Дистиллированная вода, раствор хромата калия, индикаторный раствор фенолфталеина, раствор серной кислоты 0,1 N, раствор нитрата серебра, растворитель Arcosolv PNP.
Методика определения
Для начала определите щелочность цельного бурового раствора:
1. Внесите 100 мл растворителя Arcosolv PNP в 400-мл мерный стакан.
2. Наберите в 5-мл шприц не менее 3 мл цельного бурового раствора и введите 2 мл в мерный стакан.
3. Взбалтывайте смесь круговыми движениями до достижения однородности.
4. Добавьте 200 мл дистиллированной воды. Добавьте 15 капель индикаторного раствора фенолфталеина.
5. Перемешивая смесь магнитной мешалкой, медленно титруйте 0,1N серной кислотой до начала исчезновения розовой окраски. Продолжайте перемешивать смесь в течение еще одной минуты и, если розовая окраска не появится вновь, прекратите перемешивание. Иногда бывает необходимо прекратить перемешивание, чтобы обеспечить разделение обеих фаз и возможность более четкого визуального определения цвета водной фазы.
6. Оставьте образец на 5 минут, и если розовая окраска не появится вновь, то это будет свидетельствовать о достижении конечной точки титрования. В случае возобновления розовой окраски проведите повторное титрование серной кислотой. Если розовая окраска окончательно не исчезает, оттитруйте смесь в третий раз, однако в случае возобновления окраски после третьего титрования следует прекратить дальнейшие попытки и принять полученный результат за конечную точку.
7. Закончив определение щелочности, обеспечьте наличие кислой реакции (рН < 7) у смеси, которую предполагается титровать на содержание хлоридов, путем добавления 10–20 капель 0,1 Н серной кислоты.
8. Добавьте 3,0 мл индикаторного раствора хромата калия.
9. Перемешивая смесь с помощью магнитной мешалки, медленно титруйте ее 0.282N раствором нитрата серебра до появления оранжево-розовой окраски, сохраняющейся на протяжении как минимум одной минуты. Иногда бывает необходимо прекратить перемешивание, чтобы обеспечить разделение обеих фаз и возможность более четкого визуального определения цвета водной фазы. 10. Расчет содержания хлоридов в цельном буровом растворе основывается на суммарном количестве миллилитров 0.282N нитрата серебра, потребовавшемся для достижения конечной точки титрования.
Расчет содержания хлоридов осуществляется по формуле:
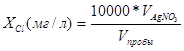 (.2)
(.2)
3 Методика количественного химического анализа мясных продуктов на содержание хлоридов методом ионной хроматографии
Проба экстрагируется по ГОСТ 9957–73 дистиллированной водой. Отделение анионов хлоридов производится хроматографически на ионообменной колонке с последующим кондуктометрическим детектированием. Относительная погрешность определения хлорид-иона в диапазоне 1–5% составляет 0.1%(2% отн.).
Оборудование: хроматограф жидкостный ионный «Цвет-3006М» ТУ 5Е1.550.186 или другой жидкостный ионный хроматограф; весы аналитические ВЛА-200г-М, ГОСТ 24104–89; колбы мерные на 50, 100, 200 и 1000 см3, ГОСТ 1770–74; пипетки мерные вместимостью 1, 2, 5, 10 и 25 см3, ГОСТ 20292–74; колбы конические вместимостью 100 или 200 см3, ГОСТ 10394–72; электромясорубка бытовая по ГОСТ 20469–81; насос вакуумный типаВМ-461; водяная баня; воронки стеклянные, ГОСТ 8613–75; фильтры беззольные бумажные; стакан химический вместимостью 200–250 мл по ГОСТ 10394–72.
Реактивы и материалы.
1. Калий хлористый, х.ч., по ГОСТ 4234–77.
2. Сорбент катионообменный КРС-8п ТУ 6–09–10–151–79.
3. Натрий углекислый кислый, хч, по ГОСТ 4201–79.
4. Натрий углекислый, хч, по ГОСТ 83–79.
5. Кислота азотная, хч, по ГОСТ 4461–77.
6. Вода бидистиллированная, ГОСТ 6709072 или деионизованная.
7. Сорбент анионообменный КанК-Аст ВТУ 881202–89.