Тема: «Обобщение знаний о качественных реакциях на органические вещества».
«Не в количестве знаний заключается образование, а в полном понимании и искусном применении всего того, что знаешь». А. Дистерверг
Цель: обобщить знания учащихся по распознаванию органических веществ с помощью качественных реакций, уметь решать экспериментальные задачи.
Задачи:
Образовательные:
1. Повторить понятия качественные реакции.
2. Сформировать знания о качественных реакциях на органические вещества.
Развивающие:
1. Формировать умение анализировать, сравнивать, делать выводы на основе полученной информации;
2. Развивать навыки познавательной деятельности, логическое мышление посредством ответов на проблемные и поставленные вопросы;
3. Развивать умения выделять главное, сравнивать.
Воспитательные:
1. Осуществлять умения высказывать свои взгляды и суждения;
2. Формировать научное мировоззрение;
3. Актуализировать умение работать в коллективе.
Средства обучения:
1. Эмоциональные: интерес;
2. Интеллектуальные: анализ, сравнение, сопоставление.
Методы обучения:
1. Словесный: объяснительная беседа, рассказ;
2. Наглядно-образный.
Оборудование: рисунки учебника, книги.
Тип урока: обобщение и проверка знаний учащихся по данной теме.
План урока:
1) организационный момент
2) актуализация знаний
3) изучение нового материала
5) домашнее задание
Ход урока
1. Организационный момент (приветствие, проверка отсутствующих, подготовка учащихся к работе на уроке.)
Актуализация знаний
Ребята, на прошлом уроке вы проходили тему «Белки и свойства белков». Сейчас я задам несколько вопросов по пройденному материалу.
1. Дайте определение понятию белкам.
2. Назовите элементный состав белков.
3. Перечислите функции белков.
4. Перечислите свойства белков.
5. Как образуется пептидная связь?
Запись белков, состоящих из аминокислот – несколько примеров.
Общее закрепление знаний:
Сегодня на уроке мы вспомним все качественные реакции, которые изучали в этом учебном году, научимся решать экспериментальные задачи.
Какие реакции называются качественными?
В качественном анализе используют легко выполнимые, характерные химические реакции, при которых наблюдается появление или исчезновение окрашивания, выделение или растворение осадка, образование газа и др. Реакции должны быть как можно более селективны и высокочувствительны. Это означает, что качественные реакции – это реакции с ощутимым эффектом – цвет, запах, изменение состояния вещества.
"Селективность" – означает, что желательно, чтобы такая реакция на данный класс веществ или на данное вещество была уникальна. Высокая чувствительность – даже очень небольшое количество вещества должно проявляться в такой реакции.
С уникальностью в органической химии немного проблематично, но тем не менее, есть достаточно много реакций для определения того или иного вещества.
Непредельные углеводороды.
1. Обесцвечивание бромной воды при пропускании через неё этилена.
2.Обесцвечивание перманганата калия в водной и кислой среде при пропускании через неё алкена.
3.Окисление алкинов и получение ацетилена.
Кислородосодержащие органические вещества.
1.Взаимодействие одноатомных предельных спиртов с натрием и окисление спиртов.
2. Внутримолекулярная дегидратация одноатомных спиртов - получение алкенов.
3. Многоатомные спирты.
4. Качественные реакции на фенол - взаимодействие с бромной водой и хлоридом железа (III).
5. Окисление альдегидов. Реакции «серебряного и медного зеркала».
6. Распознавания предельных одноосновных карбоновых кислот. Реакции на индикаторы, взаимодействие с карбонатами и хлоридом железа (III).
7. Качественные реакции на муравьиную кислоту. Обесцвечивание перманганата калия в кислой среде и реакция «серебряного зеркала».
8. Распознавание высших непредельных карбоновых кислот и раствора мыла (стеарата натрия) - обесцвечивание бромной воды олеиновой кислотой и выпадение в осадок стеариновой кислоты при действии на мыло минеральной кислоты.
9. Распознавание глюкозы. Реакции с гидроксидом меди (II), реакции «серебряного и медного зеркала».
10. Действие раствора йода на крахмал.
Азотосодержащие органические соединения.
1. Распознавание первичных и вторичных аминов.
2. Обесцвечивание бромной воды анилином.
3. Качественные реакции на аминокислоты.
4. Цветные реакции белков.
Алканы. У алканов нет качественных реакций. Их определяют методом исключения
Алкены. 1. Обесцвечивание бромной воды:

2. Изменение окраски раствора перманганата калия:
3СH2=CH2 + 2KMnO4 + 4H2O → 3C2H4(OH)2 + 2MnO2 + 2KOH

Циклоалканы. Обесцвечивание бромной воды:

Алкины. 1. Обесцвечивание бромной воды,
2. Образование ацетиленидов серебра и меди:
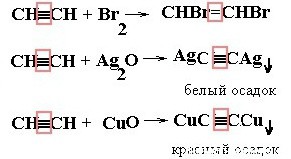
3. Изменение окраски перманганата калия: (KMnO4 → MnO2)
C2H2 → HOOC-COOH
Алкадиены. Т.к. алкадиены содержат 2 двойные связи, то они так же как и алкены, обесцвечивают бромную воду.
Арены. 1. Обесцвечивание бромной воды

2. реакция с аммиачным раствором цианида никеля (II).Выпадает осадок комплексного соединения бензоцианоаммината никеля Ni(CN)2NH3(C6H6).
Качественная реакция на бензол - реакция с аммиачным раствором цианида никеля (II). Выпадает осадок комплексного соединения бензоцианоаммината никеля Ni(CN)2NH3(C6H6).
При действии на анилин раствора хлорной извести обнаруживают фиолетовое окрашивание.
При диазотировании с последующим азосочетанием с бета-нафтолом или другой азосоставляющей образуются азокрасители.
Спирты. Реакция с оксидом меди - в осадок выпадает медь:

В прибор для окисления спиртов нальем немного этилового спирта. Присоединим к газоотводной трубке прибор для подачи воздуха. Раскалим в горелке медную спираль и поместим ее в прибор. Подадим в прибор ток воздуха. Медная спираль в приборе продолжает быть раскаленной, так как начинается окисление спирта. Продукт окисления спирта - уксусный альдегид.
Многоатомные спирты. С гидрокисдом меди (II) - Cu(OH)2 образуется комплекс синего цвета. С увеличением числа гидроксильных групп в молекуле вещества возрастает подвижность атомов водорода, т.е. увеличиваются кислотные свойства. Поэтому атомы водорода в многоатомных спиртах могут замещаться не только щелочными металлами, но и менее активными металлами. Получим гидроксид меди (II), путем сливания растворов гидроксида натрия и сульфата меди (II). Прильем полученный осадок к глицерину. Осадок гидроксида меди растворяется и образуется темно-синий раствор глицерата меди (II). Осадок гидроксида меди прильем к раствору этиленгликоля. Также образуется темно-синий раствор. Реакция с гидроксидом меди (II) является качественной реакцией на многоатомные спирты.


Альдегиды. Реакция "серебряного зеркала" и реакция "медного зеркала":

Альдегид обнаруживаем, пропуская через фуксинсернистую кислоту выходящие из прибора газы. Под действием альдегида фуксинсернистая кислота приобретает фиолетовую окраску. Покажем, что медная спираль раскалена. Извлечем спираль из прибора и поднесем к ней спичку. Спичка загорается. Мы убедились в том, что при окислении одноатомных спиртов образуются альдегиды. Однако чаще в результате этой реакции образуется красный осадок оксида меди (I).
Фенол. Качественной реакцией на фенол является реакция с хлоридом железа (III). К сильно разбавленному раствору фенола добавляем раствор хлорида железа. Жидкость в пробирке окрашивается в темно-фиолетовый цвет за счет образования комплексных фенолятов. С помощью этой реакции можно определить фенол даже при очень малых его концентрациях. При добавлении синильной кислоты окраска исчезает.
При добавлении фенола к бромной воде происходит обесцвечивание и выпадение белого осадка трибромфенола.
Кислоты органические. Дают окрашенные соли тяжелых металлов.
Амины. Качественных реакций нет (только анилин - имеет характерный запах)
Глюкоза. Качественная реакция глюкозы с гидроксидом меди (II). Глюкоза содержит в своем составе пять гидроксильных групп и одну альдегидную группу. Поэтому она относиться к альдегидоспиртам. Ее химические свойства похожи на свойства многоатомных спиртов и альдегидов. Реакция с гидроксидом меди (II) демонстрирует восстановительные свойства глюкозы. Прильем к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет. В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт. Нагреем раствор. Цвет раствора начинает изменяться. Сначала образуется желтый осадок Cu2O, который с течением времени образует более крупные кристаллы CuO красного цвета. Глюкоза при этом окисляется до глюконовой кислоты.
СН2ОН – (СНОН)4 – СОН + Сu(ОН)2 = СН2ОН – (СНОН)4 – СООН + Сu2О↓+ Н2О
Качественная реакция глюкозы с аммиачным раствором оксида серебра (I). Доказать наличие альдегидной группы в глюкозе можно с помощью аммиачного раствора оксида серебра. К аммиачному раствору оксида серебра добавим раствор глюкозы и подогреем смесь на водяной бане. Вскоре на стенках колбы начинает осаждаться металлическое серебро. Эта реакция называется реакцией серебряного зеркала. Ее используют как качественную для открытия альдегидов. Альдегидная группа глюкозы окисляется до карбоксильной группы. Глюкоза превращается в глюконовую кислоту.
СН2ОН – (СНОН)4 – СОН + Ag2O = СН2ОН – (СНОН)4 – СООН + 2Ag↓
Реакцию серебряного зеркала используют в промышленности для серебрения зеркал, изготовления колб для термосов, елочных украшений.
Белок. Ксантопротеиновая реакция на белки. Ксантопротеиновая реакция проводят для обнаружения белков, содержащих в своем составе ароматические аминокислоты. К раствору белка прибавляем концентрированную азотную кислоту. Белок свертывается. При нагревании белок желтеет. При добавлении избытка аммиака окраска переходит в оранжевую. Появление окрашивания свидетельствует о наличии ароматических аминокислот в составе белка.
Биуретовая реакция белков. Наличие белков в растворе можно обнаружить цветными реакциями. Наиболее универсальной качественной реакцией на белки является биуретовая реакция. Эта реакция характерна для групп атомов, образующих пептидную связь. К раствору белка приливаем немного раствора щелочи и несколько капель слабого раствора сульфата меди. Жидкость окрашивается в фиолетовый цвет, что указывает на присутствие белка в растворе.