Гонорея
Гонорея - инфекционное заболевание, вызываемое гонококком (Neisseria gonorrhoeae), с преимущественным поражением мочеполовых органов. Ежегодно заболевание регистрируется у 200 млн человек. Перенесенная гонорея нередко становится причиной как женского, так и мужского бесплодия.
Этиология и патогенез. Гонококк представляет собой парный кокк (диплококк) бобовидной формы, не окрашиваемый по Граму; располагается обязательно внутриклеточно (в цитоплазме лейкоцитов). Гонококки высокочувствительны к факторам внешней среды: погибают при температуре выше 55 °C, при высыхании, обработке растворами антисептиков, под влиянием прямых солнечных лучей. Гонококк сохраняет жизнеспособность в свежем гное до высыхания. В связи с этим заражение происходит в основном половым путем (от инфицированного партнера). Контагиоз-ность инфекции для женщин составляет 50-70%, для мужчин - 25-50%. Гораздо реже встречается заражение бытовым путем (через грязное белье, полотенца, мочалки), в основном у девочек. Возможность внутриутробного инфицирования остается спорной. Гонококк неподвижен, не образует спор, посредством тонких трубчатых нитей (пилей) закрепляется на поверхности эпителиальных клеток, сперматозоидов, эритроцитов. Снаружи гонококки покрыты капсулоподобной субстанцией, затрудняющей их переваривание. Возбудитель может переживать внутри лейкоцитов, трихо-монад, эпителиальных клеток (незавершенный фагоцитоз), что осложняет лечение. При неадекватном лечении могут образовываться L-формы, которые нечувствительны к препаратам, вызвавшим их образование, антителам и комплементу в результате утраты части антигенных свойств. Персистен-ция L-форм затрудняет диагностику и лечение, способствует выживанию инфекции в организме. В связи с широким использованием антибиотиков появилось множество штаммов гонококка, вырабатывающих фермент β-лактамазу и, соответственно, устойчивых к действию антибиотиков, содержащих β-лактамное кольцо.
Гонококки поражают преимущественно отделы мочеполовой системы, выстланные цилиндрическим эпителием, - слизистую оболочку церви-кального канала, маточных труб, уретры, парауретральных и больших вестибулярных желез. При генитально-оральных контактах могут развиваться гонорейный фарингит, тонзиллит и стоматит, при генитально-анальных - гонорейный проктит. При попадании инфекции на слизистую оболочку глаз, в том числе при прохождении плода через инфицированные родовые пути, появляются признаки гонорейного конъюнктивита.
Стенка влагалища, покрытая многослойным плоским эпителием, устойчива к гонококковой инфекции. Однако, если эпителий истончается или становится рыхлым, возможно развитие гонорейного вагинита (при беременности, у девочек, у женщин в постменопаузе).
Гонококки быстро фиксируются на поверхности эпителиальных клеток с помощью пилей, а затем проникают вглубь клеток, межклеточные щели и подэпителиальное пространство, вызывая деструкцию эпителия и воспалительную реакцию.
Гонорейная инфекция распространяется чаще по протяжению (канали-кулярно) из нижних отделов мочеполового тракта в верхние. Продвижению нередко способствуют адгезия гонококка к поверхности сперматозоидов и энтеробиоз внутри трихомонад, являющихся активными переносчиками инфекции.
Иногда гонококки попадают в кровяное русло (обычно они гибнут из-за бактерицидных свойств сыворотки), приводя к генерализации инфекции и появлению экстрагенитальных очагов поражения, в первую очередь суставов. Реже развиваются гонорейный эндокардит и менингит.
В ответ на внедрение гонорейной инфекции в организме вырабатываются антитела, но иммунитет при этом не развивается. Человек может заражаться и болеть гонореей многократно; это объясняется антигенной вариабельностью гонококка. Инкубационный период гонореи колеблется от 3 до 15 дней, реже - до 1 мес.
Различают следующие виды гонорейной инфекции: гонорею нижних отделов мочеполовой системы, верхних отделов мочеполовой системы и органов малого таза и гонорею других органов. К гонорее нижних отделов мочеполовой системы относят поражение уретры, парауретральных желез, желез преддверия влагалища, слизистой оболочки цервикального канала, влагалища, к гонорее верхних отделов мочеполовой системы (восходящей) - поражение матки, придатков и брюшины.
Выделяют также свежую гонорею (длительность до 2 мес), которая подразделяется на острую, подострую, торпидную (малосимптомную или бессимптомную со скудным экссудатом, в котором обнаруживаются гонококки), и хроническую (продолжительностью более 2 мес или неустановленной давности). Хроническая гонорея может протекать с обострениями. Возможно гонококконосительство, когда возбудитель не вызывает появления экссудата и субъективных расстройств нет.
Клинические проявления. Гонорея нижнего отдела мочеполовой системы часто бывает бессимптомной. Выраженные проявления болезни включают симптомы дизурии, зуд и жжение во влагалище, гноевидные сливкообраз-ные выделения из цервикального канала. При осмотре обнаруживают гиперемию и отечность устья уретры и цервикального канала.
Гонорея верхнего отдела (восходящая) обычно вызывает нарушение общего состояния, жалобы на боли внизу живота, повышение температуры тела до 39 °C, тошноту, иногда рвоту, озноб, жидкий стул, учащенное и болезненное мочеиспускание, нарушения менструального цикла. Распространению инфекции за пределы внутреннего зева способствуют артифициаль-ные вмешательства - аборты, выскабливания слизистой оболочки матки, зондирование полости матки, взятие аспирата эндометрия, биопсии шейки матки, введение ВМК. Острому восходящему воспалительному процессу нередко предшествуют менструация, роды. При объективном исследовании отмечаются гнойные или сукровично-гнойные выделения из цервикального
канала, увеличенная, болезненная, мягковатой консистенции матка (при эндомиометрите), отечные болезненные придатки (при сальпингоофори-те), болезненность при пальпации живота, симптомы раздражения брюшины (при перитоните). Острый воспалительный процесс в придатках матки осложняется развитием тубоовариальных воспалительных образований вплоть до возникновения абсцессов (особенно у женщин, использующих
ВМК).
В настоящее время гонорейный процесс не имеет типичных клинических признаков, поскольку почти во всех наблюдениях выявляется микст-инфекция. Смешанная инфекция удлиняет инкубационный период, способствует более частому рецидивированию, затрудняет диагностику и лечение.
Хронизация воспалительного процесса приводит к нарушению менструального цикла, развитию спаечного процесса в малом тазу, что может привести к бесплодию, внематочной беременности, невынашиванию беременности, синдрому хронических тазовых болей.
Основные методы лабораторной диагностики гонореи - бактериоско-пический и бактериологический, направленные на выявление возбудителя. При бактериоскопическом исследовании гонококк идентифицируют по парности, внутриклеточному расположению и грамнегативности (рис. 12.20). В связи с высокой изменчивостью под влиянием окружающей среды гонококк не всегда можно обнаружить при бактериоскопии. Для выявления стертых и бессимптомных форм гонореи, а также инфекции у детей и беременных более подходит бактериологический метод. Посев материала производят на искусственные питательные среды. При загрязненности материала посторонней сопутствующей флорой выделение гонококка становится затруднительным, поэтому используют селективные среды с добавлением антибиотиков. При невозможности произвести посев незамедлительно материал для исследования помещают в транспортную среду. Выросшие на питательной среде культуры подвергают микроскопии, определяют их свойства и чувствительность к антибиотикам. Материал для микроскопии и посева берут из цервикального канала, влагалища, уретры.
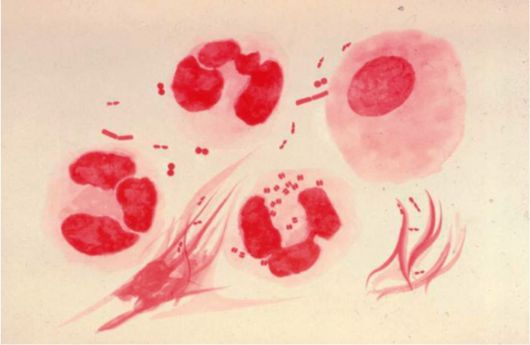
Рис. 12.20. Микроскопия влагалищного мазка. Гонококк внутри нейтрофилов
Лечение. Лечению подлежат половые партнеры при обнаружении гонококков бактериоскопическим или культуральным методом. Основное место отводится антибиотикотерапии, при этом следует учитывать рост штаммов гонококка, устойчивых к современным антибиотикам. Причиной неэффективности лечения может служить способность гонококка образовывать L-формы, вырабатывать β-лактамазу, сохраняться внутри клеток. Лечение назначают с учетом формы заболевания, локализации воспалительного процесса, осложнений, сопутствующей инфекции, чувствительности возбудителя к антибиотикам.
Этиотропное лечение свежей гонореи нижних отделов мочеполовой системы без осложнений заключается в однократном применении одного из антибиотиков: цефтриаксона, азитромицина, ципрофлоксацина, спекти-номицина, офлоксацина, амоксиклав♠, цефиксима. Для лечения гонореи нижних отделов мочеполовой системы с осложнениями и гонореи верхних отделов и органов малого таза предлагают использовать те же антибиотики в течение 7 дней.
На время лечения исключают алкоголь и половые контакты. В период диспансерного наблюдения настоятельно рекомендуется использовать презерватив. При смешанной инфекции следует выбирать препарат, дозу и длительность его применения с учетом выделенной микрофлоры. После окончания лечения антибактериальными препаратами целесообразно назначать эубиотики интравагинально (вагилак♠, лактобактерин♠, бифидум-бактерин♠, ацилакт♠).
Лечение гонореи у детей сводится к назначению цефтриаксона или спек-тиномицина однократно.
При свежей острой гонорее нижних отделов мочеполовой системы достаточно этиотропного лечения. В случае торпидного или хронического течения заболевания при отсутствии симптоматики лечение антибиотиками рекомендуется дополнить иммунотерапией, физиотерапией.
Иммунотерапия гонореи подразделяется на специфическую (гоновак-цина*) и неспецифическую (пирогенал♠, продигиозан♠, аутогемотерапия). Иммунотерапия проводится после стихания острых явлений на фоне продолжающейся антибиотикотерапии либо до начала лечения антибиотиками (при подостром, торпидном или хроническом течении). Детям до 3 лет иммунотерапия не показана. В целом в настоящее время использование им-муномодулирующих средств при гонорее ограничено и должно быть строго обоснованным.
Принципы терапии острых форм восходящей гонореи аналогичны таковым при лечении воспалительных заболеваний внутренних половых органов.
Критериями излеченности гонореи (через 7-10 дней после окончания терапии) служат исчезновение симптомов заболевания и элиминация гонококков из уретры, цервикального канала и прямой кишки по данным бактериоскопии. Возможно проведение комбинированной провокации, при которой мазки берут через 24, 48 и 72 ч и делают посев выделений через 2 или 3 сут. Провокацию подразделяют на физиологическую (менструация), химическую (смазывание уретры 1-2% раствором нитрата серебра, церви-кального канала - 2-5% его раствором), биологическую (внутримышечное
введение гоновакцина* в дозе 500 млн микробных тел), физическую (ин-дуктотермия), алиментарную (острая, соленая пища, алкоголь). Комбинированная провокация сочетает все виды провокации.
Второе контрольное исследование проводят в дни ближайшей менструации. Оно заключается в бактериоскопии отделяемого из уретры, цервикаль-ного канала и прямой кишки, взятого 3 раза с интервалом 24 ч.
При третьем контрольном обследовании (после окончания менструации) делают комбинированную провокацию, после чего производят бактерио-скопическое (через 24, 48 и 72 ч) и бактериологическое (через 2 или 3 сут) исследование. При отсутствии гонококков пациентку снимают с учета.
При неустановленном источнике инфицирования целесообразно провести серологические реакции на сифилис, ВИЧ, гепатит B и C (до лечения и через 3 мес после его окончания).
Многие специалисты оспаривают целесообразность провокаций и многократных контрольных обследований и предлагают сократить сроки наблюдения за женщинами после полноценного лечения гонококковой инфекции, поскольку при высокой эффективности современных препаратов теряется клинический и экономический смысл рутинных мероприятий. Рекомендуется, по крайней мере, один контрольный осмотр после окончания лечения с целью определения адекватности терапии, отсутствия симптомов гонореи, а также выявления партнеров. Лабораторный контроль проводят только в случае продолжающегося заболевания, при возможности повторного заражения или устойчивости возбудителя.
К обследованию и лечению привлекают половых партнеров, если половой контакт произошел за 30 дней до появления симптомов заболевания, а также лиц, бывших в тесном бытовом контакте с больной. При бессимптомной гонорее обследуют половых партнеров, имевших контакт в течение 60 дней до установления диагноза. Обследованию подлежат дети матерей, больных гонореей, а также девочки при обнаружении гонореи у лиц, осуществляющих уход за ними.
Профилактика заключается в своевременном выявлении и адекватном лечении больных гонореей. С этой целью проводят профилактические осмотры, особенно работников детских учреждений, столовых. Обязательному обследованию подлежат беременные, взятые на учет в женской консультации или обратившиеся для прерывания беременности. Личная профилактика сводится к соблюдению личной гигиены, исключению случайных половых связей, пользованию презервативом. Профилактика гонореи у новорожденных проводится сразу после рождения: в конъюнктивальный мешок закапывают 1-2 капли 30% раствора сульфацетамида (сульфацил натрия*).
Урогенитальный хламидиоз
Урогенитальный хламидиоз - одна из самых частых инфекций, передаваемых половым путем. Число заболевших хламидиозом неуклонно возрастает; ежегодно в мире регистрируется 90 млн случаев заболевания. Широкая распространенность хламидиоза обусловлена стертостью клинической
симптоматики, сложностью диагностики, появлением резистентных к антибиотикам штаммов, а также социальными факторами: увеличением частоты внебрачных половых отношений, проституцией и др. Хламидии часто являются причиной негонококкового уретрита, бесплодия, воспалительных заболеваний органов малого таза, пневмонии и конъюнктивита новорожденных.
Этиология и патогенез. Хламидии представляют собой грамотрицатель-ные бактерии сферической формы, небольших размеров, относящиеся к семейству Chlamidiaceae рода Chlamidia. Для человека наиболее значимы С. trachomatis (возбудитель урогенитального хламидиоза, трахомы, венерической лимфогранулемы), С. psittaci (вызывает атипичную пневмонию, артрит, пиелонефрит), С. pneumoniae (возбудитель ОРЗ, пневмонии). Возбудитель имеет все основные микробиологические признаки бактерий, размножается простым бинарным делением, но для воспроизводства нуждается в клетках организма хозяина (внутриклеточное паразитирование), что делает его похожим на вирусы. Уникальньгй цикл развития хламидии включает две формы существования: элементарные тельца (инфекционная форма, адаптированная к внеклеточному существованию) и ретикулярные тельца (вегетативная форма, обеспечивающая внутриклеточное размножение). Элементарные тельца фагоцитируются клеткой организма хозяина, но не перевариваются (неполный фагоцитоз), а превращаются в ретикулярные тельца и активно размножаются. Цикл развития хламидий составляет 48-72 ч и заканчивается разрывом клетки хозяина с выходом элементарных телец в межклеточное пространство (рис. 12.21).
Хламидии неустойчивы во внешней среде, легко погибают при воздействии антисептиков, ультрафиолетовых лучей, кипячении, высушивании.
Заражение происходит в основном при половых контактах с инфицированным партнером, трансплацентарно и интранатально, редко - бытовым
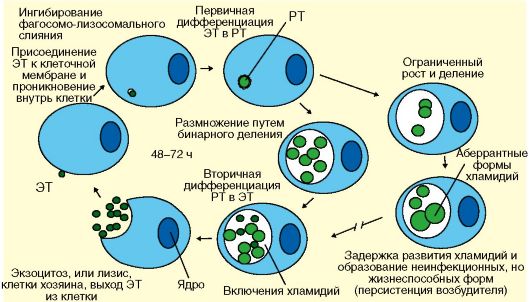
Рис. 12.21. Жизненный цикл хламидий: ЭТ - элементарные тельца; РТ - ретикулярные тельца
путем через предметы туалета, белье, общую постель. Возбудитель заболевания проявляет высокую тропность к клеткам цилиндрического эпителия (эндоцервикс, эндосальпинкс, уретра). Кроме того, хламидии, поглощаясь моноцитами, разносятся с током крови и оседают в тканях (суставы, сердце, легкие и др.), обусловливая многоочаговость поражения. Основным патогенетическим звеном хламидиоза является развитие рубцово-спаечного процесса в пораженных тканях как следствие воспалительной реакции.
Хламидийная инфекция вызывает выраженные изменения как клеточного, так и гуморального звена иммунитета. Следует учитывать способность хламидий под влиянием неадекватной терапии трансформироваться в L-формы и (или) изменять свою антигенную структуру, что затрудняет диагностику и лечение заболевания.
Классификация. Выделяют свежий (давность заболевания до 2 мес) и хронический (давность заболевания более 2 мес) хламидиоз; отмечены случаи носительства хламидийной инфекции. Кроме того, заболевание подразделяется на хламидиоз нижних отделов мочеполовой системы, верхних ее отделов и органов малого таза, хламидиоз другой локализации.
Клиническая симптоматика. Инкубационный период при хламидиозе колеблется от 5 до 30 дней, составляя в среднем 2-3 нед. Урогенитально-му хламидиозу свойственны полиморфизм клинических проявлений, отсутствие специфических признаков, бессимптомное или малосимптомное длительное течение, склонность к рецидивам. Острые формы заболевания отмечены при смешанной инфекции.
Наиболее часто хламидийная инфекция поражает слизистую оболочку цервикального канала. Хламидийный цервицит чаще остается бессимптомным. Иногда больные отмечают появление серозно-гнойных выделений из половых путей, а при присоединении уретрита - зуд в области уретры, болезненное и учащенное мочеиспускание, гнойные выделения из мочеиспускательного канала по утрам (симптом "утренней капли").
Восходящая урогенитальная хламидийная инфекция определяет развитие сальпингоофорита, пельвиоперитонита, перитонита, которые не имеют специфических признаков, кроме затяжного "стертого" течения при хрони-зации воспалительного процесса. Последствиями перенесенного хламидио-за органов малого таза становятся спаечный процесс в области придатков матки, бесплодие, внематочная беременность.
К экстрагенитальному хламидиозу следует отнести болезнь Рейтера, включающую триаду: артрит, конъюнктивит, уретрит.
Хламидиоз новорожденных проявляется вульвовагинитом, уретритом, конъюнктивитом, пневмонией.
Ввиду скудной и (или) неспецифической симптоматики распознать заболевание на основании клинической картины невозможно. Диагноз хла-мидиоза ставят только по результатам лабораторных методов исследования. Лабораторная диагностика хламидиоза заключается в выявлении самого возбудителя или его антигенов. Материалом для исследования служат со-скобы из цервикального канала, уретры, с конъюнктивы. Микроскопия мазков, окрашенных по Романовскому-Гимзе, позволяет выявить возбудитель в 25-30% случаев. При этом элементарные тельца окрашиваются в крас-
ный, ретикулярные - в синий и голубой цвета. Более чувствительны методы иммунофлюоресценции и иммуноферментного анализа с использованием меченых моноклональных антител, а также молекулярно-биологический метод (ПЦР). Золотым стандартом для выявления внутриклеточных паразитов остается культуральный метод (выделение на культуре клеток).
С целью уточнения диагноза и определения фазы заболевания используют выявление хламидийных антител классов А, М, G в сыворотке крови. В острой фазе хламидийной инфекции повышается титр IgM, при переходе в хроническую фазу увеличиваются титры IgA, а затем IgG. Снижение титров хламидийных антител классов A, G в процессе лечения служит показателем его эффективности.
Лечение. Обязательному обследованию и при необходимости лечению подлежат все половые партнеры. В период лечения и диспансерного наблюдения следует воздерживаться от половых контактов или использовать презерватив.
Терапия хламидиоза должна быть комплексной. Трудности и неудачи лечения объясняются биологическими свойствами возбудителя (внутриклеточное паразитирование, способность к образованию L-форм), сочетанием хламидиоза с другими генитальными инфекциями, особенностями иммунитета (незавершенный фагоцитоз).
При неосложненном хламидиозе мочеполовых органов рекомендуется один из антибиотиков: азитромицин, рокситромицин, спирамицин, джоза-мицин, доксициклин, офлоксацин, эритромицин в течение 7-10 дней.
При хламидиозе органов малого таза применяют те же препараты, но не менее 14-21 дня. Предпочтительно назначение азитромицина - по 1,0 г внутрь 1 раз в неделю в течение 3 нед.
Новорожденным и детям с массой тела до 45 кг назначают эритромицин в течение 10-14 дней. Детям до 8 лет с массой тела более 45 кг и старше 8 лет эритромицин и азитромицин применяют по схемам лечения взрослых.
В связи со снижением иммунного и интерферонового статуса при хла-мидиозе наряду с этиотропным лечением целесообразно включать препараты интерферона (виферон♠, реаферон♠, кипферон♠) или индукторы синтеза эндогенного интерферона (циклоферон*, неовир*, рибонуклеат натрия - ридостин♠, тилорон). Кроме того, назначают антиоксиданты, витамины, физиотерапию, проводят коррекцию вагинального микробиоценоза эубио-тиками.
Критериями излеченности считаются разрешение клинических проявлений и эрадикация Chlamidia trachomatis по данным лабораторных исследований, проводимых через 7-10 дней, а затем через 3-4 нед.
Профилактика урогенитального хламидиоза заключается в выявлении и своевременном лечении больных, исключении случайных половых контактов.
Генитальный герпес
Герпес относится к самым распространенным вирусным инфекциям человека. Инфицированность вирусом простого герпеса (ВПГ) составляет 90%; у 20% населения земного шара имеются клинические проявления ин-
фекции. Генитальный герпес - передаваемое половым путем хроническое рецидивирующее вирусное заболевание.
Этиология и патогенез. Возбудителем заболевания является вирус простого герпеса серотипов ВПГ-1 и ВПГ-2 (чаще - ВПГ-2). Вирус герпеса достаточно крупный, ДНК-содержащий, неустойчив во внешней среде и быстро погибает при высыхании, нагревании, действии дезинфицирующих растворов.
Заражение происходит при половых контактах от инфицированных партнеров, не всегда знающих о своей инфицированности. В последнее время большое эпидемиологическое значение имеет орально-генитальный путь инфицирования. Контагиозность для женщин достигает 90%. Бытовой путь передачи инфекции (через предметы туалета, белье) маловероятен, хотя и не исключается. Герпетическая инфекция может передаваться от больной матери плоду трансплацентарно и интранатально.
Вирус проникает в организм через поврежденные слизистые оболочки половых органов, уретры, прямой кишки и кожные покровы. В месте внедрения появляются пузырьковые высыпания. ВПГ, попадая в кровяное русло и лимфатическую систему, может оседать во внутренних органах, нервной системе. Вирус может также проникать через нервные окончания кожи и слизистых оболочек в ганглии периферической и центральной нервной системы, где сохраняется пожизненно. Периодически мигрируя между ганглиями (при генитальном герпесе это ганглии поясничного и сакрального отделов симпатической цепочки) и поверхностью кожи, вирус вызывает клинические признаки рецидива заболевания. Проявлению герпетической инфекции способствуют снижение иммунореактивности, переохлаждение или перегревание, хронические заболевания, менструация, оперативные вмешательства, физические или психические травмы, прием алкоголя. ВПГ, обладая нейродермотропизмом, поражает кожу и слизистые оболочки (лицо, половые органы), ЦНС (менингит, энцефалит) и периферическую нервную систему (ганглиолиты), глаза (кератит, конъюнктивит).
Классификация. Клинически различают первый эпизод заболевания и рецидивы генитального герпеса, а также типичное течение инфекции (с герпетическими высыпаниями), атипичное (без высыпаний) и вирусоно-сительство.
Клиническая симптоматика. Инкубационный период составляет 3-9 дней. Первый эпизод заболевания протекает более бурно, чем последующие рецидивы. После короткого продромального периода с местным зудом и гиперестезией развертывается клиническая картина. Типичное течение гениталь-ного герпеса сопровождается экстрагенитальными симптомами (вирусемия, интоксикация) и генитальными признаками (местные проявления заболевания). К экстрагенитальным симптомам относятся головная боль, повышение температуры тела, озноб, миалгии, тошнота, недомогание. Обычно эти симптомы исчезают с появлением пузырьковых высыпаний на промежности, коже наружных половых органов, во влагалище, на шейке матки (генитальные признаки). Везикулы (размером 2-3 мм) окружены участком гиперемированной отечной слизистой оболочки. После 2-3 дней существования они вскрываются с образованием язв, покрытых серовато-желтым
гнойным (из-за вторичного инфицирования) налетом. Больные жалуются на боль, зуд, жжение в месте поражения, тяжесть внизу живота, дизурию. При выраженных проявлениях болезни отмечаются субфебрильная температура, головная боль, увеличение периферических лимфатических узлов. Острый период герпетической инфекции длится 8-10 дней, после чего видимые проявления заболевания исчезают.
В настоящее время частота атипичных форм генитального герпеса достигла 40-75%. Эти формы заболевания стертые, без герпетических высыпаний, и сопровождаются поражением не только кожи и слизистых оболочек, но и внутренних половых органов. Отмечаются жалобы на зуд, жжение в области поражения, бели, не поддающиеся антибиотикотерапии, рецидивирующие эрозии и лейкоплакии шейки матки, привычное невынашивание беременности, бесплодие. Герпес верхнего отдела половых путей характеризуется симптомами неспецифического воспаления. Больных беспокоят периодические боли в нижних отделах живота; общепринятая терапия не дает нужного эффекта.
При всех формах заболевания страдает нервная система, что проявляется в нервно-психических расстройствах - сонливости, раздражительности, плохом сне, подавленном настроении, снижении работоспособности.
Частота рецидивов зависит от иммунобиологической резистентности макроорганизма и колеблется от 1 раза в 2-3 года до 1 раза каждый месяц.
Диагностика генитального герпеса основывается на данных анамнеза, жалобах, результатах объективного исследования. Распознавание типичных форм заболевания обычно не представляет трудностей, поскольку везику-лезная сыпь имеет характерные признаки. Однако следует отличать язвы после вскрытия герпетических пузырьков от сифилитических язв - плотных, безболезненных, с ровными краями. Диагностика атипичных форм генитального герпеса чрезвычайно сложна.
Применяют высокочувствительные и специфичные лабораторные методы диагностики: культивирование вируса на культуре клеток куриного эмбриона (золотой стандарт) или выявление вирусного антигена методами ИФА; иммунофлюоресцентным методом, с помощью ПЦР. Материалом для исследования служит отделяемое из герпетических пузырьков, влагалища, цервикального канала, уретры. Простое определение антител в сыворотке крови к вирусу не является точным диагностическим критерием, поскольку отражает лишь инфицированность ВПГ, в том числе не только генитальным. Диагноз, установленный только на основании серологических реакций, может быть ошибочным.
Лечение. Половых партнеров пациента с генитальным герпесом обследуют на ВПГ и проводят лечение при клинических признаках инфекции. До исчезновения проявлений заболевания рекомендуют воздерживаться от половых контактов или использовать презервативы.
Поскольку в настоящее время не существует методов элиминации ВПГ из организма, цель лечения заключается в подавлении размножения вируса в период обострения заболевания и формировании стойкого иммунитета для профилактики рецидивов герпетической инфекции.
Для терапии первого клинического эпизода и при рецидиве генитально-го герпеса рекомендуют противовирусные препараты (ацикловир, валаци-кловир) в течение 5-10 дней.
Комплексный подход подразумевает применение неспецифической (Т-активин, тималин♠, тимоген♠, инозин пранобекс - гроприносин♠), мие-лопид* по стандартным схемам и специфической (противогерпетический γ-глобулин, герпетическая вакцина) иммунотерапии. Чрезвычайно важным звеном в лечении герпеса является коррекция нарушений системы интерферона как главного барьера на пути внедрения вирусной инфекции в организм. Хороший эффект дают индукторы синтеза эндогенного интерферона: полудан♠, циклоферон♠, неовир♠, тилорон. В качестве заместительной терапии используют препараты интерферона - виферон♠, кипферон♠ в ректальных свечах, реаферон♠ внутримышечно и др.
Кроме того, рекомендуют местное применение антисептиков для профилактики вторичной гнойной инфекции.
С целью предупреждения рецидивов используют герпетическую вакцину, интерфероногены, а также противовирусные и иммунные препараты. Длительность терапии определяется индивидуально.
Критериями эффективности лечения считают исчезновение клинических проявлений заболевания (рецидива), положительную динамику титра специфических антител.
Генитальный туберкулез
Туберкулез - инфекционное заболевание, вызываемое микобактерией (бактерией Коха). Генитальный туберкулез, как правило, развивается вторично, в результате переноса инфекции из первичного очага поражения (чаще из легких, реже - из кишечника). Несмотря на прогресс медицины, заболеваемость туберкулезом в мире увеличивается, особенно в странах с низким уровнем жизни. Поражение мочеполовых органов стоит на первом месте среди внелегочных форм туберкулеза. Вероятно, поражение туберкулезом половых органов происходит значительно чаще, чем регистрируется, поскольку прижизненная диагностика не превышает 6,5%.
Этиология и патогенез. Из первичного очага при снижении иммунной резистентности организма (хронические инфекции, стрессы, недостаточное питание и др.) микобактерии попадают в половые органы. Инфекция распространяется в основном гематогенным путем, чаще при первичной дис-семинации в детстве или в период полового созревания. При туберкулезном поражении брюшины возбудитель попадает на маточные трубы лимфогенно или контактным путем. Прямое заражение при половых контактах с больным генитальным туберкулезом возможно только теоретически, поскольку многослойный плоский эпителий вульвы, влагалища и влагалищной порции шейки матки устойчив к микобактериям.
В структуре генитального туберкулеза первое место по частоте занимает поражение маточных труб, второе - эндометрия. Реже встречается туберкулез яичников и шейки матки, крайне редко - туберкулез влагалища и наружных половых органов.
В очагах поражения развиваются типичные для туберкулеза морфогисто-логические изменения: экссудация и пролиферация тканевых элементов, казеозные некрозы. Туберкулез маточных труб часто заканчивается их облитерацией, экссудативно-пролиферативные процессы могут привести к образованию пиосальпинкса, а при вовлечении в специфический пролифера-тивный процесс мышечного слоя маточных труб в нем образуются туберкулы (бугорки), что носит название нодозного воспаления. При туберкулезном эндометрите также преобладают продуктивные изменения - туберкулезные бугорки, казеозный некроз отдельных участков. Туберкулез придатков матки нередко сопровождается вовлечением в процесс брюшины с асцитом, петель кишечника с образованием спаек, а в некоторых случаях и фистул. Гениталь-ный туберкулез часто сочетается с поражением мочевых путей.
Классификация. В соответствии с клинико-морфологической классификацией различают:
• хронические формы - с продуктивными изменениями и нерезко выраженными клиническими симптомами;
• подострую форму - с экссудативно-пролиферативными изменениями и значительными поражениями;
• казеозную форму - с тяжелыми и острыми процессами;
• законченный туберкулезный процесс - с инкапсулированием обыз-вествленных очагов.
Клиническая картина. Первые симптомы заболевания могут появиться уже в период полового созревания, но в основном генитальным туберкулезом болеют женщины 20-30 лет. В редких случаях заболевание встречается у пациенток более старшего возраста или в постменопаузе.
Генитальный туберкулез имеет в основном стертую клиническую картину с большим разнообразием симптомов, что объясняется вариабельностью патологоанатомических изменений. Снижение генеративной функции (бесплодие) является основным, а иногда и единственным симптомом заболевания. К причинам бесплодия, чаще первичного, следует отнести эндокринные нарушения, поражения маточных труб и эндометрия. Более чем у половины пациенток нарушается менструальная функция: возникают аменорея (первичная и вторичная), олигоменорея, нерегулярные менструации, альгоменорея, реже мено- и метроррагии. Нарушения менструальной функции связаны с поражением паренхимы яичника, эндометрия, а также туберкулезной интоксикацией. Хроническое заболевание с преобладанием экссудации обусловливает субфебрильную температуру и тянущие, ноющие боли внизу живота из-за спаечного процесса в малом тазу, поражения нервных окончаний, склероза сосудов и гипоксии тканей внутренних половых органов. К другим проявлениям болезни относятся признаки туберкулезной интоксикации (слабость, периодическая лихорадка, ночной пот, снижение аппетита, похудение), связанные с развитием экссудативных или казеозных изменений во внутренних половых органах.
У молодых пациенток генитальный туберкулез может начаться с признаков "острого живота", что нередко приводит к оперативным вмешательствам в связи с подозрением на острый аппендицит, внематочную беременность, апоплексию яичника.
Ввиду отсутствия патогномоничных симптомов и стертости клинической симптоматики диагностика генитального туберкулеза затруднена. На мысль о туберкулезной этиологии заболевания может навести правильно и тщательно собранный анамнез с указаниями на контакт пациентки с больным туберкулезом, перенесенные в прошлом пневмонию, плеврит, наблюдение в противотуберкулезном диспансере, наличие экстрагенитальных очагов туберкулеза в организме, а также возникновение воспалительного процесса в придатках матки у молодых пациенток, не живших половой жизнью, особенно в сочетании с аменореей, и длительная субфебрильная температура. При гинекологическом исследовании иногда выявляют острое, подострое или хроническое воспалительное поражение придатков матки, наиболее выраженное при преобладании пролиферативных или казеозных процессов, признаки спаечного процесса в малом тазу со смещением матки. Данные гинекологического исследования обычно неспецифичны.
Для уточнения диагноза используют туберкулиновую пробу (проба Коха). Туберкулин* вводят подкожно в дозе 20 или 50 ТЕ, после чего оценивают общую и очаговую реа