СЕВЕРО-ЗАПАДНЫЙ ГОСУДАРСТВЕННЫЙ МЕДИЦИНСКИЙ УНИВЕРСИТЕТ ИМЕНИ И.И. МЕЧНИКОВА
Кафедра патологической физиологии
В.И. Николаев, М.Д. Денисенко
ПАТОФИЗИОЛОГИЯ ПОЧЕК
Учебно-методическое пособие
Санкт-Петербург
2015 г.
УДК 616 – 092.18
ББК 52.5
В.И. Николаев, М.Д. Денисенко Патофизиология почек. Учебно-методическое пособие. – СПб.: Издательство ГБОУ ВПО СЗГМУ им. И.И. Мечникова, 2015. – 54 с.
Рецензент: заведующий кафедрой медицинской биологии д.м.н. профессор Костюкевич С.В.
В учебно-методическом пособии рассматриваются вопросы нарушения функции почек, анализируются механизмы развития патологии почек, описываются основные синдромы, связанные с заболеваниями почек.
Учебно-методическое пособие предназначено для студентов третьего курса обучающихся по ФГОС ВПО по направлению подготовки (специальности) 060101 лечебное дело
Утверждено
в качестве учебно-методического пособия Методическим
советом ГБОУ ВПО СЗГМУ им. И.И. Мечникова
протокол № _2 от «05» декабря 2014 г.
© В.И.Николаев, М.Д.Денисенко
© Издательство СЗГМУ им. И. И. Мечникова, 2015
1. Тема «Патофизиология почек»
2. Контингент учащихся – студенты, обучающиеся по ФГОС ВПО по направлению подготовки (специальности) 060101 лечебное дело.
3. Продолжительность занятий – 4 часа (в академических часах).
4. Структура практического занятия
1. Функции почек. Роль почек в поддержании гомеостаза.
2. Характеристика процессов, лежащих в основе работы почек:
· механизмы процесса фильтрации в норме и при патологии;
· механизмы процесса реабсорбции в норме и при патологии;
· механизмы процесса секреции в норме и при патологии.
3. Основные ренальные симптомы нарушения функции почек:
· изменение суточного объема мочи;
· изменение удельного веса мочи;
· изменение ритма мочеиспускания;
· изменение состава мочи.
4. Протеинурия: виды, механизмы развития.
5. Гематурия: виды, механизмы развития.
6. Цилиндрурия: виды, механизмы развития.
7. Этиопатогенетическая классификация заболеваний почек.
8. Основные патогенетические синдромы заболеваний почек:
· нефритический синдром: этиология, патогенез, клинические проявления, осложнения;
· нефротический синдром: этиология, патогенез, клинические проявления, осложнения;
· острая почечная недостаточность: виды, этиопатогенез, исходы;
· хроническая почечная недостаточность: этиология, патогенез, исход. Уремия.
9. Хроническая болезнь почек.
10. Принципы патогенетической коррекции заболеваний почек.
11. Лабораторная диагностика патологии почек:
· исследование очистительной функции почек (клиренс);
· проба Реберга-Тареева;
· проба по Зимницкому;
· проба по Нечипоренко;
· проба Аддиса-Каковского.
5. Содержание практического занятия
Почки, являясь жизненно важным органом, играют немаловажную роль в сохранении постоянства внутренней среды организма. Поддержание гомеостаза реализуется как за счет непосредственно экскреторной (выделительной) функции почек, так и за счет выполнения почками других – неэкскреторных – функций. Почки участвуют в процессах:
1. регуляции водно-солевого обмена (поддержание объема циркулирующей крови (ОЦК), интерстициальной и внутриклеточной жидкости, концентрации Na+, K+, Mg2+, Cl-, Ca2+ и других электролитов путем влияния на размер экскреции воды и электролитов);
2. регуляции кислотно-щелочного равновесия (за счет реакций ацидогенеза, аммониогенеза, реабсорбции или выведения бикарбонатов, выделения слабых органических кислот в неизмененном виде);
3. регуляции системного артериального давления (за счет регуляции ОЦК, за счет активации ренин-ангиотензин-альдостероновой системы (РААС), влияющей не только на внутрисосудистый объем жидкости, но и (посредством ангиотензина) на общее периферическое сопротивление сосудов (ОПСС), за счет синтеза простагландинов, также изменяющих сосудистый тонус);
4. регуляции гемопоэза (за счет синтеза эритропоэтинов, лейко- и тромбопоэтинов);
5. витаминного обмена (за счет синтеза vitD3);
6. обмена гормонов (за счет синтеза ренина).
И, естественно, почки осуществляют процесс удаления из плазмы крови токсичных продуктов, в том числе лекарственных препаратов, конечных продуктов обмена, но препятствуют выделению с мочой белков и глюкозы.
Функциональной единицей почек является нефрон (представляющий собой клубочек, канальцы – проксимальные и дистальные – и собирательные трубочки), в котором благодаря процессам фильтрации, реабсорбции и секреции и осуществляется образование мочи.
Процесс фильтрации осуществляется в начальной части нефрона – почечных клубочках, где образуется первичная моча, представляющая собой ультрафильтрат плазмы в объеме 180-200 л/сутки.
Движущей силой, обусловливающий процесс фильтрации, является фильтрационное давление (ФД). ФД создается в результате разности между гидростатическим давлением в капиллярах клубочка (ГДкл. = 50-55 мм рт. ст.), способствующим прохождению элементов плазмы крови через трехслойную мембрану в просвет капсулы Боумена, и противоположно действующими силами, создаваемыми онкотическим давлением плазмы крови (ОД = 20-28 мм рт. ст.) и давлением в капсуле Боумена (Дкапс. = 12 мм рт. ст.).
Гидростатическое давление в капиллярах клубочка является величиной, зависящей главным образом от мышечного тонуса стенок приводящей и отводящей артериол. Онкотическое давление плазмы крови зависит от содержания в ней белков. Давление в полости капсулы Боумена определяется проходимостью почечных канальцев и мочевыводящих путей; кроме того, оно зависит от внутрипочечного давления. В среднем фильтрационное давление составляет 18 мм рт.ст.
Фильтрующая мембрана состоит из трех слоев: эндотелия капилляров, базальной мембраны и эпителиальных клеток внутренней части капсулы (подоцитов). Она способна пропускать почти все имеющиеся в плазме крови вещества с молекулярным весом ниже 70 000 Д, а также небольшую часть альбуминов.
Кроме фильтрационного давления, на объем образующегося ультрафильтрата влияет площадь фильтрации, зависящая от количества функционирующих нефронов, а также проницаемость фильтрующей мембраны.
Нарушение фильтрации может выражаться в ее уменьшении или увеличении независимо от объема поступившей в организм жидкости.
К уменьшению объема фильтрации могут приводить как почечные, так и внепочечные факторы.
К почечным причинам снижения фильтрации относятся:
· уменьшение числа функционирующих клубочков вследствие замещения их фиброзной тканью или вследствие деструктивных процессов в почках;
· снижение проницаемости фильтрующей мембраны в связи с прорастанием соединительной тканью, осаждением на ней иммунных комплексов, аутоантител;
· склеротические изменения в приносящих артериолах;
· увеличение давления в полости капсулы Боумена по причине повышения внутрипочечного давления при отеке интерстиция или нарушения проходимости канальцев и мочевыводящих путей.
Внепочечными причинами уменьшения фильтрации могут быть:
· снижение системного кровяного давления (например, в связи с сердечной недостаточностью, шоком любой этиологии, обезвоживанием). При падении систолического артериального давления ниже 50 мм рт.ст. фильтрация прекращается полностью;
· повышение онкотического давления плазмы крови в результате увеличения концентрации белков, что может произойти при повышенном их синтезе (например, при миеломной болезни), введении белковых препаратов или сгущении крови.
Критическое уменьшение объема клубочковой фильтрации может произойти внезапно (например, при острой почечной недостаточности) или явиться результатом длительно развивающейся болезни, приводящей к гибели клубочков.
Несмотря на большой объем первичной мочи, у человека за сутки выделяется около 1,5 литров окончательной мочи. Такое резкое уменьшение объема выделяемой почками жидкости объясняется тем, что в канальцах нефрона происходит процесс усиленной реабсорбции воды, а также электролитов, глюкозы, аминокислот и др. Поступление этих веществ через стенку канальцев в интерстиций и затем в околоканальцевые капилляры осуществляется с помощью разных механизмов:
1) активный транспорт веществ с затратой энергии против электрохимического или концентрационного градиента специфическими переносчиками;
2) пассивный транспорт веществ по концентрационному, осмотическому или электрохимическому градиентам (таким образом транспортируются вода, бикарбонаты, мочевина, ионы Cl-);
3) транспорт белков, осуществляемый главным образом путем пиноцитоза.
Наиболее интенсивно процессы реабсорбции происходят в проксимальном канальце. Здесь всасывается 60-65% воды и натрия, а также высокий процент К+, Са2+, Mg2+, SO42-, HPO42-, Cl-, HCO3-; практически полностью реабсорбируются белки, витамины, аминокислоты, глюкоза, в значительном количестве – мочевина и мочевая кислота (рис. 1).
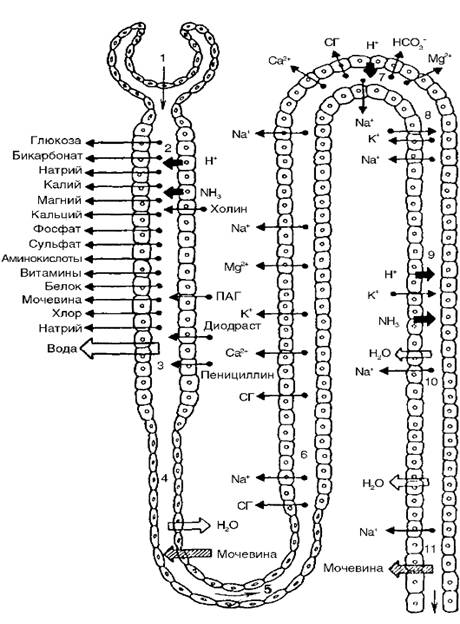
Рисунок 1. Процессы реабсорбции и секреции в нефроне (по Е.М. Тарееву): 1 – клубочек; 2 – проксимальный извитой каналец; 3 – проксимальный прямой каналец; 4 – тонкое нисходящее колено петли Генле; 5 – изгиб петли Генле; 6 – толстое восходящее колено петли Генле; 7 – дистальный извитой каналец; 8 – связующий отдел; 9 – собирательная трубка наружного мозгового вещества; 10 – собирательная трубка внутреннего мозгового вещества почки; 11 – Беллини проток. Стрелка, обращенная из просвета канальца, – реабсорбция вещества, в просвет канальца – секреция.
В проксимальном канальце всасывание электролитов и других веществ происходит с эквивалентным количеством воды, и поэтому содержимое канальца остается изотоничным плазме.
Процессы реабсорбции продолжаются в дистальном канальце и собирательной трубочке. Здесь всасываются Na+, Cl-, Са2+, Н2О и мочевина. Особенностью функционирования этих отделов является то, что здесь процессы реабсорбции и секреции регулируются различными гормонами и зависят от потребностей организма. Такой вид всасывания называется факультативным в отличие от облигатного типа реабсорбции в проксимальном отделе нефрона.
Наряду с реабсорбцией в канальцах осуществляются процессы секреции, т.е. активного выделения ряда веществ в канальцевую жидкость, при этом одни из выделяемых веществ образуются в самом почечном эпителии (Н+ и NH3), а другие извлекаются эпителием из внеклеточной жидкости с помощью специфических транспортных систем. В проксимальном отделе нефрона секретируются в канальцевую жидкость Н+, NH3, щавелевая, мочевая и желчные кислоты, адреналин, ацетилхолин, гистамин, серотонин, тиамин, а также парааминогиппуровая кислота, различные лекарственные вещества (например, пенициллин, индометацин, салициловая кислота, фуросемид и др.).
Нарушение процессов реабсобрцбии, экскреции и секреции в канальцах может быть связано с:
· изолированным повреждением ферментных систем (что имеет место при наследственных и приобретенных тубулопатиях);
· дистрофическими изменениями канальцевого эпителия;
· структурными изменениями в окружающем интерстиции;
· расстройствами гуморальной регуляции.
Тубулопатии – это заболевания, обусловленные нарушением транспортных функций эпителия почечных канальцев в связи с отсутствием или качественными изменениями белков-переносчиков, тех или иных ферментов, рецепторов для гормонов или дистрофическими процессами в стенке канальцев.
По этиологии различают первичные(наследственные) и вторичные(приобретенные) тубулопатии. К первичным тубулопатиям относится, например, нефрогенная форма несахарного диабета. Вторичные тубулопатии могут развиться под действием лекарственных препаратов; при отравлении солями лития, висмута, ртути, свинца, кадмия; при обширных ожогах; гиперпаратиреозе; злокачественных опухолях различных органов; миеломной болезни и др.
В зависимости от локализации дефекта различают проксимальные и дистальные тубулопатии.
Основные ренальные симптомы нарушения функции почек.
Суточный объем мочи при обычной водной нагрузке равен около 1,5 литров. Относительная плотность колеблется в пределах от 1002 до 1035. Реакция мочи кислая (рН от 5,0 до 7,0). В составе мочи могут присутствовать единичные эритроциты и лейкоциты, клетки плоского эпителия, гиалиновые цилиндры.
Заболевания почек сопровождаются нарушениями образования и выделения мочи, что может выражаться в виде изменения количества мочи, ее относительной плотности и состава (мочевой синдром).
Количество выделяемой за сутки мочи может быть повышенным (полиурия), пониженным (олигурия) или крайне низким, вплоть до полного отсутствия мочи (анурия).
Полиурия (polys – много, uron – моча) характеризуется увеличением объема суточного диуреза свыше 2000 мл независимо от объема выпитой жидкости. В механизме развития полиурии играют роль увеличение клубочковой фильтрации плазмы крови и/или уменьшение реабсорбции жидкости в канальцах. Последнее имеет место на полиурической стадии острой и хронической почечной недостаточности, а также при прекращении секреции АДГ.
Олигурия (olygos – малый) характеризуется снижением суточного диуреза до 500-200 мл. Причинами этого могут являться уменьшение объема клубочкового фильтрата, усиление реабсорбции воды в канальцах почек или затруднение оттока мочи.
Анурия (an – отсутствие, uron – моча) характеризуется прекращением мочеотделения или выделением мочи в количестве менее 100 мл/сутки. По механизму развития различают анурию преренальную, ренальную и постренальную.
Наряду с объемом суточной мочи могут изменяться частота и ритм мочеиспускания.
Частота мочеиспускания может увеличиваться (поллакиурия, от греч. рollakis – часто) или снижаться (оллакизурия, от греч. оllakis – редко).
При ряде заболеваний почек и некоторых нарушениях в мочевыводящих путях наблюдается превалирование ночного диуреза над дневным – никтурия (от nictos – ночь), тогда как у здорового человека объем дневного диуреза составляет 65-80% от общего объема суточной мочи.
Показателем концентрационной способности почек является относительная плотность мочи (удельный вес). Нормальные значения относительной плотности мочи колеблются от 1002 до 1035 в зависимости от количества поступившей в организм жидкости, причем обязательно должны быть выражены колебания относительной плотности в течение суток, с более высокими значениями утром.
При заболеваниях почек удельный вес мочи может увеличиваться (гиперстенурия), уменьшаться (гипостенурия) или соответствовать относительной плотности клубочкового фильтрата без существенных суточных колебаний (изостенурия).
Гиперстенурия (hyper – много, sthenos – сила) характеризуется увеличением относительной плотности мочи более 1030 вследствие усиления процесса реабсорбции воды в дистальном отделе.
Гипостенурия (hypo – мало, sthenos – сила) означает снижение относительной плотности мочи (1002-1012); при пробе с сухоядением относительная плотность мочи не достигает 1026.
Изостенурия (isos – равный) – относительная плотность мочи остается фиксированной в разных порциях мочи без колебаний в течение суток («монотонный диурез») и соответствует относительной плотности клубочкового фильтрата (1010).
Гипо- и изостенурия характерны для ренальной формы острой почечной недостаточности, хронической почечной недостаточности (в полиурическую стадию), гипофункции надпочечников, несахарного диабета и др.
Изменения состава мочи характеризуются появлением в ней:
· белка (протеинурия);
· глюкозы (глюкозурия);
· аминокислот (аминоацидурия);
· кетоновых тел (кетонурия);
· эритроцитов (гематурия);
· лейкоцитов (лейкоцитурия, при большом их количестве – пиурия);
· цилиндров (цилиндрурия),
· кристаллов различных солей (кристаллурия);
· микроорганизмов (бактериурия) и др.
Протеинурия. В норме проникновению белков плазмы крови в клубочковый фильтрат препятствуют гломерулярный фильтр (эндотелий, базальная мембрана, подоциты) и электростатический заряд этих структур, который отталкивает отрицательно заряженные молекулы, в том числе молекулы альбумина. Заряд клубочкового фильтра обусловлен присутствием в нем сиалогликопротеина и гликозаминогликанов.
У здорового человека в клубочках из плазмы крови фильтруется 0,5 г белка/сутки (преимущественно альбумина). Значительная часть поступившего в клубочковый фильтрат белка реабсорбируется в проксимальных канальцах посредством пиноцитоза. Количество белка, выделяющегося с мочой, в норме не должно превышать 0,033 г/л. Выделение большего количества белка называется протеинурией.
По количеству белка в моче выделяют микропротеинурию (до 1 г/сутки) и макропротеинурию (более 3 г/сутки).
По качеству выделяемого с мочой белка определяют селективную (исключительно низкомолекулярные белки, т.е. прежде всего альбумины) и неселективную (и низко-, и высокомолекулярные белки) протеинурию. Развитие селективной протеинурии связано с утратой клубочковым фильтром способности отталкивать отрицательно заряженные молекулы белка и, таким образом, препятствовать их прохождению в ультрафильтрат. Поскольку диаметр пор фильтра (70 нм) превышает размер молекул альбумина и трансферрина, то эти белки свободно проходят через незаряженный фильтр. Неселективная протеинуриявозникает при утрате гломерулярным фильтром способности регулировать прохождение молекул белка в зависимости от их размера. В связи с этим в ультрафильтрат поступают не только альбумины и трансферрин, но и крупнодисперсные белки плазмы, например иммуноглобулины G1, а2-макроглобулин и β-липопротеины.
По механизмам протеинурию подразделяют на функциональную (периодическую) и патологическую.
Функциональная протеинурия встречается при отсутствии заболеваний почек. К ней относят:
· ортостатическую (постуральную / лордотическую) протеинурию;
· протеинурию при интенсивной физической нагрузке (рабочая / маршевая протеинурия);
· при эмоциональном стрессе
· при переохлаждении и др.
Ортостатическая протеинурия наблюдается у 12-40% детей и подростков; характеризуется выявлением белка в моче при длительном нахождении в вертикальном положении. Появляется ортостатическая протеинурия вследствие нарушения почечной гемодинамики, развивающегося за счет лордоза, сдавливающего нижнюю полую вену в положении стоя, или выброса ренина (с последующей активацией системы РААС) в ответ на изменения объема циркулирующей крови при ортостатизме.
Рабочая (маршевая) протеинурия связана с гемолизом эритроцитов и гемоглобинурией при интенсивной физической нагрузке, а также с действием катехоламинов, выделяющихся за счет активации симпатоадреналовой системы, на юкстагломерулярный аппарат, что в свою очередь вызывает активацию системы РААС. Протеинурия в этом случае выявляется в первой после физической нагрузки порции мочи.
Общей особенностью всех видов функциональной протеинурии являются ее преходящий характер (никогда не бывает постоянной) и малое количество выделяемого белка (функциональная протеинурия всегда микропротеинурия).
Патологическая протеинурия связана с наличием заболеваний – как почек, так и других органов. К патологической протеинурии относят:
· канальцевую;
· клубочковую;
· секреторную;
· гистурию;
· протеинурию переполнения.
Клубочковая протеинурия связана с повышенной проницаемостью почечного фильтра вследствие нарушения механического (повреждение базальной мембраны клубочка) или электрического (нейтрализация заряда мембраны клубочка) барьера. Повреждение почечного фильтра может быть обусловлено:
1. токсическим действием флогогена;
2. цитолитическим действием ферментов комплемента или лейкоцитов при развитии воспаления.
В случае воспалительного повреждения клубочков развивается, как правило, микропротеинурия.
Потеря отрицательного заряда компонентов почечного фильтра происходит вследствие нейтрализации клубочковых полианионов катионами крови, прежде всего Н+. Вторично происходит слияние подоцитов и вакуолизация эпителиальных клеток проксимальных канальцев, что приводит к развитию макропротеинурии.
Канальцевая протеинурия развивается при нарушении реабсорбции белка в проксимальном канальце. Данный механизм протеинурии характерен для тубулоинтерстициальных поражений почек различной этиологии.
Протеинурия переполнения наблюдается при повышенном содержании в плазме низкомолекулярных белков (например, легких цепей иммуноглобулинов – белок Бенс-Джонса при миеломной болезни), что делает невозможной полную реабсорбцию всего отфильтровавшегося в клубочке белка: белки фильтруются в количествах, превышающих возможности реабсорбции канальцевого аппарата.
Секреторная протеинурия связана с поражением мочевыводящих путей, когда белок при разрушении клеток эпителия мочевыводящих путей (как, например, при уретрите) попадает в мочу при прохождении последней через участки повреждения.
Гистурия (тканевая протеинурия) – повышенная экскреция с мочой тканевых изоантигенов, (например, при опухолевых поражениях паренхиматозных органов).
Гематурия – присутствие крови в моче. Различают микрогематурию (до 50-70 эритроцитов в поле зрения) и макрогематурию (более 70 эритроцитов в поле зрения). Микрогематурия не изменяет цвета мочи, ее можно выявить только при микроскопии осадка или с помощью индикаторной полоски. Макрогематурия придает моче цвет «мясных помоев».
Причины развития гематурии можно разделить на две большие группы:
1) заболевания почек (гломерулонефрит, тубулоинтерстициальный нефрит, поликистоз, поражение почек при системной красной волчанке, болезни Шенлейна-Геноха и др.);
2) повреждения мочевыводящих путей (при мочекаменной болезни, травмах, опухолях мочевыводящих путей и др.).
В зависимости от этиологии гематурии качество присутствующих в моче эритроцитов будет различным: при поражении почек в моче обнаруживаются гемолизированные («выщелоченные») эритроциты, а при патологии мочевыводящих путей (нижних их отделов) в моче присутствуют «свежие» (неразрушенные) эритроциты.