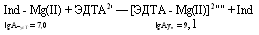стадия. Упаковка, укупорка, маркировка.
На конвеере
5) ФХ это ион магния (магния сульфат) 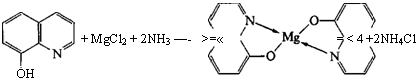
Реакция с 8-оксихинолином в присутствии аммиака и хлорида аммония (аммиачный буфер) приводит к образованию зелено-желтого кристаллического осадка внутрикомплексного оксихинолината магния
MgCl2 + Na2HP04 + NH3 — NH4MgP044 + 2NaCl мелкокристаллич осадок двойного фосфата аммония и магния – это осн офиц реакция
- Испытания на подлинность можно осуществлять, используя микрокристаллоскопическую реакцию капельным методом на предметном стекле. При быстрой кристаллизации образуется кристаллогидрат MgNH4P04 • 6Н20 характерной формы. - Ион магния Mg2+ можно также обнаружить, осаждая его избытком гидроксида натрия. Образующийся Mg(OH)2 представляет собой белый студенистый осадок, не растворимый в избытке раствора гидроксида натрия. При добавлении нескольких капель йода осадок приобретает темно-коричневую окраску.
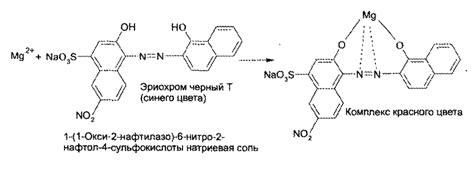
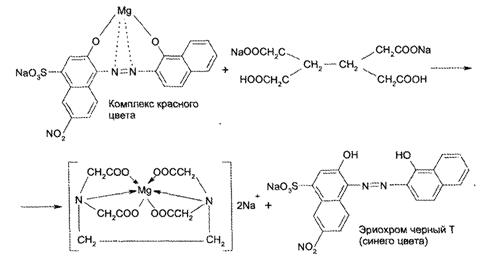
Количеств опре-е: Официнальным методом количественного определения ЛС магния является комплексонометрический. При этом в качестве индикатора используется чаще всего кислотный хромовый черный специальный (эриохром черный Т). Его обычно применяют в кристаллическом виде. Кислотный хромовый черный специальный взаимодействует с Mg + при рН 9,5 — 10 с образованием винно-красного комплекса Ind- Mg: При титровании трилоном Б в точке эквивалентности цвет раствора меняется из красного на синий (цвет индикатора), так как протекает конкурирующая реакция образования более прочного координационного соединения иона металла с 6-дентатным лигандом — этилендиаминтетраацетат-ионом (ЭДТА): 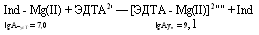
6)БИОТЕХ Для ауксотрофов типа продуцента лизина чрезвычайно важ-
ным параметром является начальная дозировка в среде источни-
ков ростовых факторов (тех аминокислот, которые штамм не мо-
жет синтезировать самостоятельно). Их избыток приводит к угне-
тению биосинтеза; при их дефиците концентрация клеток проду-
цента в ферментере будет недостаточна для обеспечения высокой
скорости накопления аминокислоты. Поэтому у продуцентов, ана-
логичных продуценту лизина, существует оптимальная концент-
рация ростовых факторов. Эта величина не постоянна. Она может
варьировать в зависимости от сырья, аэрационных возможностей
аппаратуры, температуры культивирования. Эффективность использования субстрата при биосинтезе целевой аминокислоты зависит также от продуктивности биомассы.
Если синтез аминокислоты разобщен с ростом биомассы (как у
продуцента лизина), то эффективность использования субстрата
будет тем выше, чем дольше культура будет работать после оста-
новки роста. Если же синтез идет параллельно росту (как у проду-
цента треонина), то продуктивность биомассы можно увеличить,
перераспределив потоки субстратов внутри клетки, расширяя по-
ток предшественников на биосинтез аминокислоты, одновремен-
но сужая все остальные потоки.
| 55. СЕННЫЛИСТЬЯ (в лабораторию заводу..)
Cassia Acutifolia остролистная сенна
Семейство Бобовые- Fabaceae
Листья сенны – Folia Sennae.
Многолетний полукустарник. Дикорастущее растение. Распространение: в районах Северной Африки и Аравии, в Средней Азии. Собр в фазу цветения и плодоношения.Сушка 50-56C? воздушно-теневая
Внешние признаки:
| Строение
| Сложный парноперистый
| Виз на сух с
| | Форма
| ланцетовидные
| --------
| | Размер
|
| По ланейке
| | Нал черешка
| черешковые
| Виз на сух с
| | Хар жилкован
| Перистое
| ----------
| | Хаар края
| цельнокрайние
| --------------
| | Опушение
| Неопушены
| Впроходящем своте
| | Цвет свеху
| желтовато - зеленый
| При дн осв на бел фоне
| | Цвет снизу
| Серо-зел
| ----------
| | Запах
| слабый
| При растирани
| | Вкус
| горький
| При разжев
| Химический состав: Антраценпроизводные – сеннозид А и Б, флавонойды, гликозиды – глюкоалоэмодин, глюкореин, смолистые вв
Числовые показатели:
Суммы агликонов антраценового ряда в пересчете на хризофановую кислоту не менее 1,35%; влажность не более 12%; золы общей не более 12%; кусочков стеблей толще 2 мм не более 3%; листочков и плодов не менее 70%, в том числе побуревших, почерневших листочков не более 3%; органической примеси не более 3%; минеральной примеси не более 1%.
Качественные реакции:
1 Рц Борнтрегера со щелочью
1)Экстракция NaOH с одновременным гидролизом при t
(наиб. полное извлечение А. из ЛРС в виде фенолятов и окисление А. до антрахинонов)
2) Доб. НС1 (для разрушения фенолятов)
3)Сумму А извлекают в эфирный слой, он становится желтым
4)эф извлечение взбалтывают с рр аммиака: аммиачный слой вишнево-красный(эмодины)), а эфирный слой остается окрашенным в желтый цвет (хризофановая кислота - антрахиноны) 2) ТСХ, БХ
Количественное определение: Суммы агликонов антраценового ряда в пересчете на хризофановую кислоту
| Этап
| Методика
| Обоснование
| | 2. Экстракция
| а) нагрев с водой
| а) сеннозиды переходят в гликозидированную форму
| | б) доб хлороформ
| б) удаление хлорофилл и смол. в-в
| | в) доб. хлорид железа
| в) восст-е окисл. форм
| | г) доб. серную к-ту
| г) для кислотн. гидролиза гликозидов
| | д) доб. эфир
| д) для экстракции агликонов
| | 3. Очистка
| а) доб. щелочно-амм. р-р
| а) для образования окраш. фенолятов
| | 4. КО
| СФМ
| Образов.окраш.соед.
| Применение:
Слабительное средство. Водный настой, сухой экстракт, порошок – из листьев. Препараты – СЕНАДЕ, ГЛАКСЕН, КАФИОЛ Хранение: 3 года по общ списку
2) ТЛФ: Коэф Водопоглощ 1.8 (табл данные) м сенны=1.8(коэф водопогл) * 15=27
магния сульфат растворяем в уже готовом водном извлечении, общий объем будет увеличен на прирост объем от сухого вещества (масса * КУО = 45,0 * 0,5 = 22,5 мл). т.е.общий объем равен 177,5 мл
объем воды получается 155-(1.8*15)=128 мл
ППК: Воды очищен 128,
травы сенны 27.0
магния сульфата 45.0 (КУО 0.5)
V общ 177.5 мл № откл 2%
Концетраты магния сульфата использовать нельзя, так как водные извлечения пр № 308
3) ОЭФ а) Уровень КТ – 2. Тип КТ - сложный: Прямые (нет посредников) и сложные(с посредн.) в) ∑тн=ОЦп*%ТН/100% ТНпрям пост=35%, ТН ч/з опт орг =25%; ∑НДС=(ОЦп+∑тн)*%НДС/100%; РЦ=ОЦп+∑тн+∑НДС На ИМН %ТН устан аптекой самост, НДС на парафарм 18% На ЛС изгот в апт РЦ=Ингрид+апт пос и всп мат+тариф на изгот+∑НДС г) брошюры в аптеке, предлагать посетителям оповестить ЛПУ
4)ТГЛС Драже – твердая дозированная ЛФ для внутреннего применения, получаемая путем многократного наслаивания (дражирования) лекарственных и вспомогательных веществ на сахарные гранулы (крупку). Драже имеют шаровидную форму, масса 0,1 – 0,5г. В виде драже выпускают трудно таблетируемые лекарственные вещества. Драже позволяет скрыть неприятный вкус лекарственного вещества, уменьшить их раздражающее действие, предохранить от воздействия внешних факторов. Однако в этой ЛФ трудно обеспечить точность дозирования, распадаемость в требуемые сроки, быстрое высвобождение лекарственных веществ. Драже не рекомендуется детям. Учитывая выше изложенное, эта ЛФ не относится к перспективным. Технология: промышленное производство драже осуществляется в дражировочных котлах (обдукторах). Процесс получения драже аналогичен технологии покрытия таблеток дражировочными оболочками. В качестве вспомогательных веществ применяют сахар, крахмал, пшеничную муку, магния карбонат, этилЦ, ацетилЦ, NaKМЦ, тальк, гидрогенизированные жиры, кислоту стеариновую, какао, шоколад, пищевые красители и лаки. Гранулы (сахарная крупка) просеивают через сито с расчетом, чтобы в 1 г их содержалось около 40, загружают во вращающийся котел и производят последовательное наращивание до тех пор, пока не израсходуются все материалы. Обдуктор представляет собой вращающийся котел овальной формы, укрепленный на наклонном валу. Скорость вращения котла от 20 до 60 об/мин. Загрузка обдуктора должна составлять 1/5 – 1/6 объема. При большей загрузке таблетки могут разрушаться под тяжестью вращающейся массы, при меньшей истираться за счет интенсивного перемешивания внутри котла. Для нанесения каждого последующего слоя поверхность драже увлажняют сахарным сиропом и равномерно обсыпают сначала мукой, а через несколько минут – магния карбонатом. После 25 - 30' в котел подают профильтрованный воздух, подогретый до t = 40 - 50ºC. Масса высыхает через 30 – 40 мин. Операцию повторяют 2 – 3 р.Готовят тестообразную массу, состоящую из муки и сиропа сахарного (1 кг муки на 2 л сиропа), сюда добавляют лекарственные вещества. Поливают послойно, обсыпают магия карбонатом. Подают горячий воздух на 30-40 мин. Операцию повторяют 2 – 3 раза. В конце процесса котел вращают без наращивания и получают драже с блестящей гладкой поверхностью. Для глянцевания добавляют воск.
5)БИОТЕХ При получении каллусных культур сначала готовят эксплант —
маленькие (2 — 4 мм) кусочки растительной ткани, не утратив-
шие способность к репродукции. Этот растительный материал
тщательно моют, стерилизуют 96 % спиртом или 0,1% сулемой,
а затем снова тщательно промывают дистиллированной водой и
помещают на синтетическую агаризованную питательную среду.
Сосуды закрывают ватно-марлевыми тампонами. Для образования
каллуса и роста ткани сосуды переносят в темное помещение, где
поддерживают определенную температуру (24—26 °С) и влажность
(65 — 70 %), при этом через 2 — 3 нед на раневой поверхности об-
разуется первичный каллус. Каллусная клетка развивается анало-
гично другим клеткам, проходя соответственно такие циклы, как
деление, растяжение, дифференцировка, старение и отмирание.
Кривая роста каллусной ткани имеет 8-образный характер и включает пять фаз разной длительности у разных растений
Кривая роста каллусной ткани. Фазы:
/ — латентная (лаг-фаза — клетки адаптируются и готовятся к делению); 2 —
линейная (рост каллусной ткани идет с постоянной скоростью); 3 — экспонен-
циальная (время максимальной митотической активности; рост клетки ускорен,
масса каллуса увеличивается); 4 — стационарная (интенсивность деления резкоснижается); 5 — отмирания
Нет однозначного ответа на вопрос, как связан синтез вторич-
ных метаболитов с ростовыми процессами. У большого числа куль-
тур вторичные метаболиты синтезируются и накапливаются в зна-
\ читальных количествах либо во время экспоненциальной фазы,
\когда ростовые процессы особенно активны, либо в период ста-
ционарной фазы роста культуры клеток, когда прирост клеточ-
ной массы прекращается. Однако есть культуры, у которых синтез вторичных метаболитов
сопровождает весь период роста
6)ФАРМХИМИЯ ФХ это ион магния (магния сульфат) 
Реакция с 8-оксихинолином в присутствии аммиака и хлорида аммония (аммиачный буфер) приводит к образованию зелено-желтого кристаллического осадка внутрикомплексного оксихинолината магния
MgCl2 + Na2HP04 + NH3 — NH4MgP044 + 2NaCl мелкокристаллич осадок двойного фосфата аммония и магния – это осн офиц реакция
- Испытания на подлинность можно осуществлять, используя микрокристаллоскопическую реакцию капельным методом на предметном стекле. При быстрой кристаллизации образуется кристаллогидрат MgNH4P04 • 6Н20 характерной формы. - Ион магния Mg2+ можно также обнаружить, осаждая его избытком гидроксида натрия. Образующийся Mg(OH)2 представляет собой белый студенистый осадок, не растворимый в избытке раствора гидроксида натрия. При добавлении нескольких капель йода осадок приобретает темно-коричневую окраску.
Количеств опре-е: Официнальным методом количественного определения ЛС магния является комплексонометрический. При этом в качестве индикатора используется чаще всего кислотный хромовый черный специальный (эриохром черный Т). Его обычно применяют в кристаллическом виде. Кислотный хромовый черный специальный взаимодействует с Mg + при рН 9,5 — 10 с образованием винно-красного комплекса Ind- Mg: При титровании трилоном Б в точке эквивалентности цвет раствора меняется из красного на синий (цвет индикатора), так как протекает конкурирующая реакция образования более прочного координационного соединения иона металла с 6-дентатным лигандом — этилендиаминтетраацетат-ионом (ЭДТА): 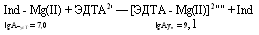


|